细胞外囊泡(EV)是有效的信号传导介质。尽管对EV转化的兴趣不断增加,但由于无法可靠地评估EV及其RNA货物的吸收,开发工作受到了阻碍。近日,来自美国西奈山医学中心的研究人员在JEV杂志上发表文章,建立了一种新的基于qPCR的方法,用于使用RNA示踪剂(DUST)检测未修饰的EV。
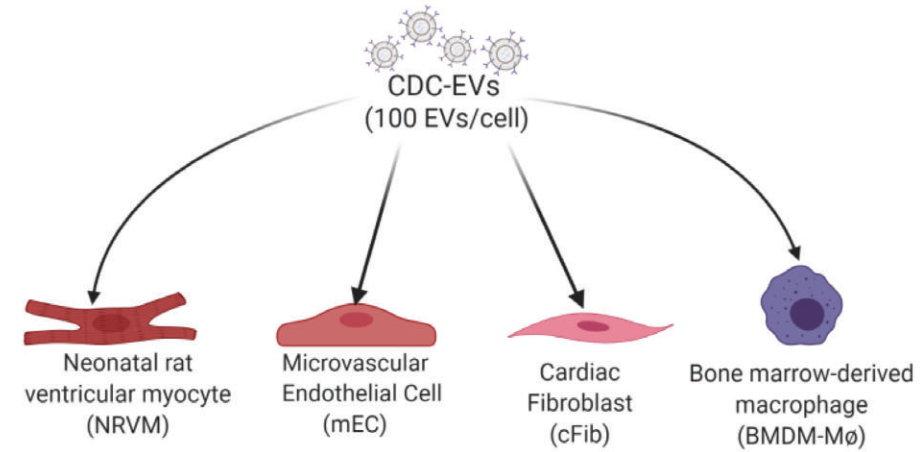
在这项概念验证研究中,使用了一种人类特异性Y RNA衍生的小RNA(YsRNA),作者称之为“NT4”,它富含心肌球衍生的细胞小EV(CDC-sEV)。该检测方法稳健、灵敏且可重复。以每毫克计,静脉注射的CDC-sEV主要在心脏中积累。心脏损伤增强了心脏、肝脏和大脑对EV的摄取。肝素对EV对接的抑制不同程度地抑制了摄取,而对内吞作用的抑制减弱了所有器官的摄取。在体外,与心肌细胞相比,巨噬细胞、内皮细胞和心脏成纤维细胞更有效地摄取EV。这些发现证明了DUST可用于评估EV在体内和体外的吸收。
细胞外囊泡(EVs)包含几类脂质双层颗粒,它们要么来自晚期内体,要么从质膜被动脱落。EV在包括癌症和缺血性损伤在内的疾病中发挥着关键作用,并且正如最近所认识到的那样,它介导了细胞疗法的再生作用。EV含有有效的生物活性物质,包括改变受体组织的转录组和表观基因组的小RNA、蛋白质和脂质。心肌球衍生细胞(Cardiosphere-DerivedCells, CDC)是一组具有免疫调节、抗纤维化、血管生成和组织修复特性的心脏基质祖细胞。CDC分泌小型EV(CDC-sEV)参与细胞的益处。因此,CDC-sEV代表了有吸引力的下一代无细胞疗法。事实上,EVs规避了细胞疗法固有的关键挑战。作为非活体,它们不需要细胞保持活力所需的放大和处理措施。EV的免疫原性也低于细胞,再加上它们的小尺寸,允许更大和重复的剂量。
EV生物学的持久挑战之一是在体内可靠地跟踪RNA货物的生物分布。了解EV货物的生物分布对于了解药代动力学和推进临床转化至关重要。亲脂性染料用于示踪充满挑战,包括缺乏特异性。EV标记-报告系统操作仅限于表面标记,并引入了标记排他性以及无法标记生物体液(如血清)。最后,EV跟踪方法无法确认货物的交付,这在信号和转化应用中特别有用。RNA是EV中最具生物活性的信号传导介质之一。因此,评估这一类关键EV货物的生物分布对于研究EV信号转导很有用。
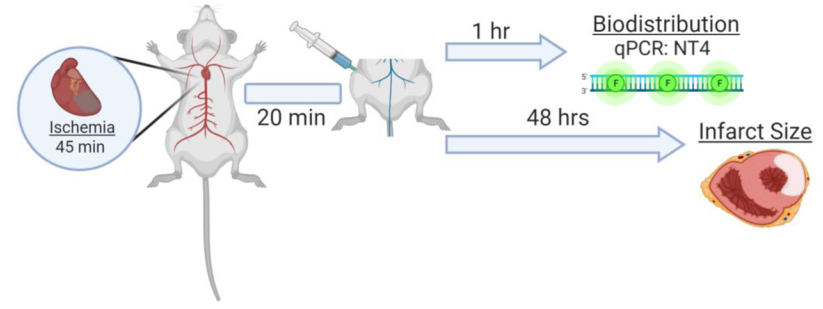
该研究开发了一种新的基于qPCR的方法,作者称之为使用RNA示踪剂(DUST)检测未修饰的EV,用于测量来自未改变的EV的RNA货物的生物分布和驻留。通过识别小鼠组织中具有低背景的天然丰富的小RNA物种,为可以适应其他未经处理的EV种群的方法建立了概念验证。使用DUST来评估CDC-sEV在健康动物和缺血再灌注损伤的动物中的生物分布。
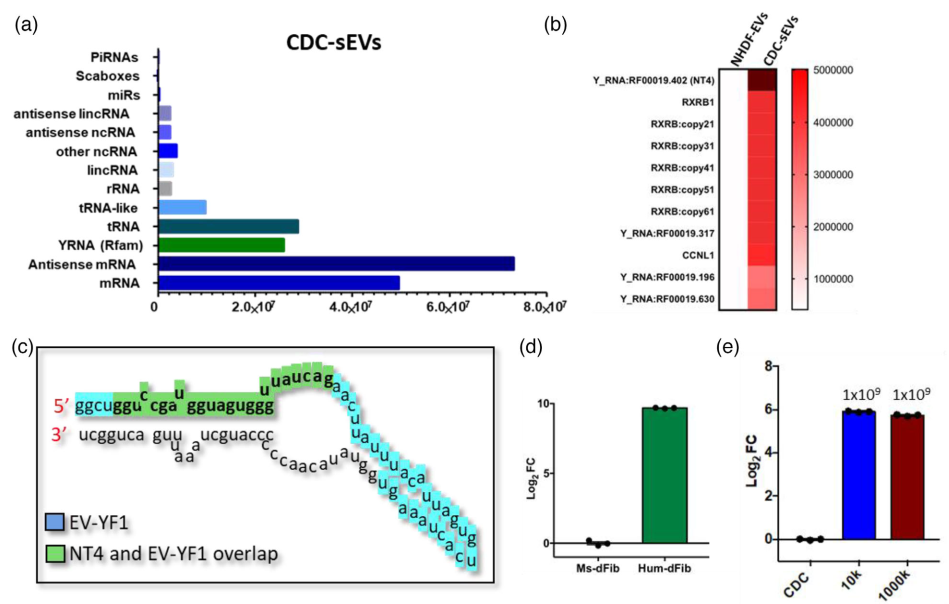
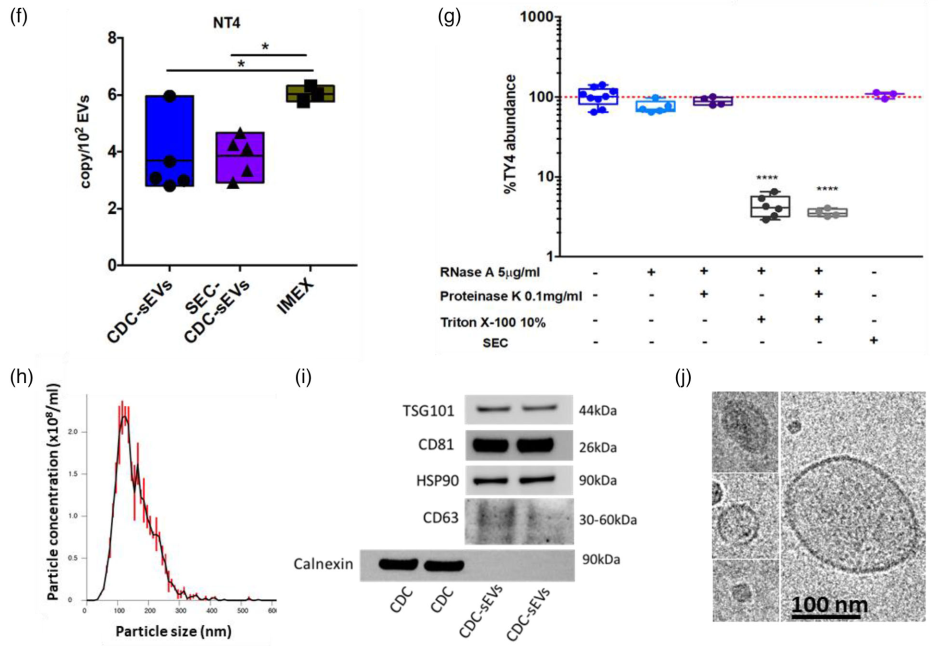
天然hY4f示踪剂(NT4)在小鼠组织中不存在,在人类CDC-sEV中高度富集
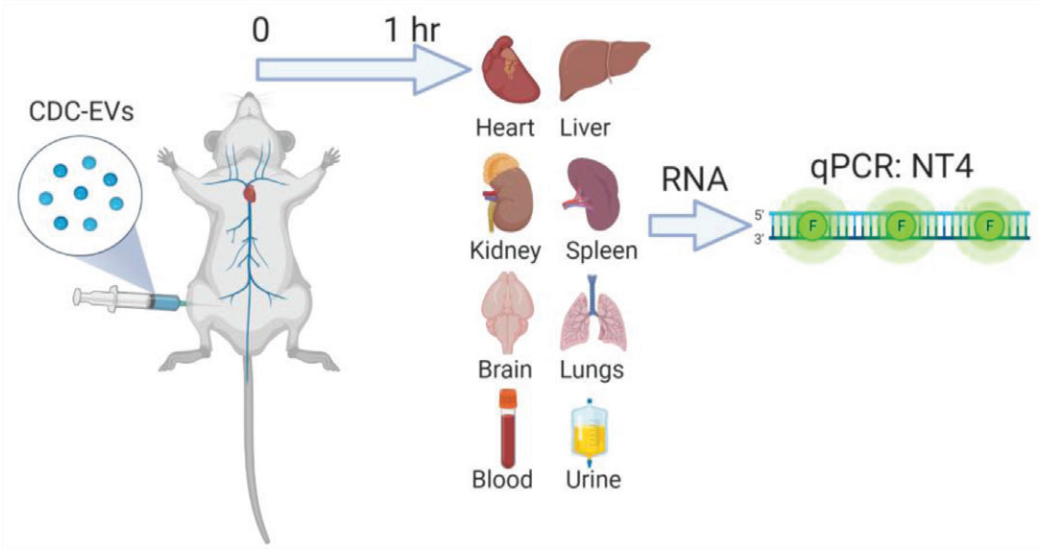
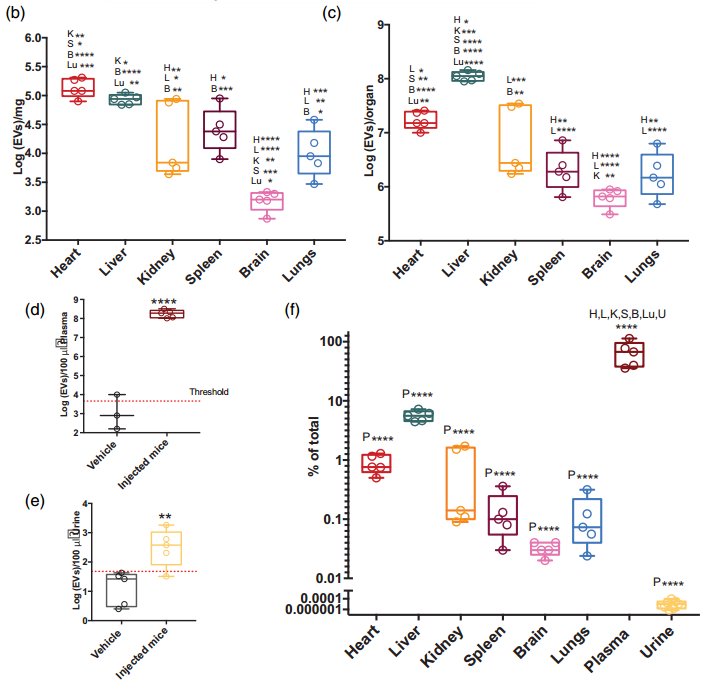
股静脉注射后CDC-sEVs在健康动物体内的生物分布
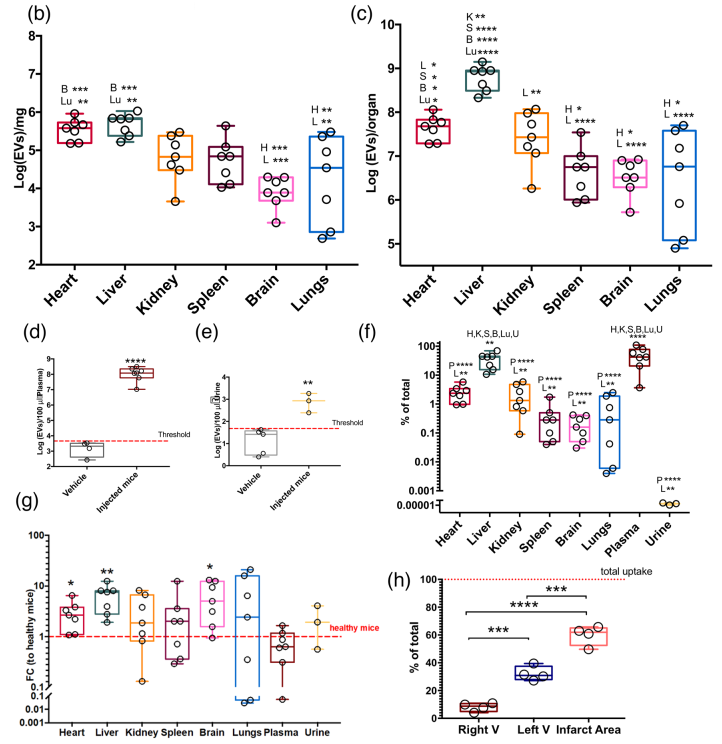
CDC-sEV在健康和受伤动物之间的分布不同
参考文献:
Ciullo A, Li C, Li L, Ungerleider KC, Peck K, Marbán E,Ibrahim AGE. Biodistribution of unmodified cardiosphere-derived cellextracellular vesicles using single RNA tracing. J ExtracellVesicles. 2022 Jan;11(1):e12178. doi: 10.1002/jev2.12178. PMID:35005847; PMCID: PMC8743874.
外泌体资讯网 JEV:单一RNA可示踪未修饰的胞外囊泡的生物分布