肾脏缺氧是急性肾损伤和慢性肾病的显著特征,已被广泛认为是慢性肾病进展为终末端肾病的最终共同途径。肾脏缺氧很可能成为各种肾脏疾病治疗的全新靶点。
近日,南开大学医学院王悦冰副教授和南开大学化学院郭东升教授合作,在国际知名杂志Journal of Nanobiotechnology上发表了题为“Coassemblyof hypoxia-sensitive macrocyclic amphiphiles and extracellular vesicles fortargeted kidney injury imaging and therapy”的文章(2021 Dec27;19:451)。在此项工作中,作者利用分子识别和自组装,构建了全新纳米级缺氧敏感共组装体系,为精确的肾脏缺氧诊断和有效的肾脏损伤治疗提供了一种全新策略。该工作提出的将内源性细胞衍生膜结构与外源性大环受体共组装的策略,有望为解决多种临床需求提供一个功能平台。
肾脏特殊的生理结构使其对缺氧非常敏感,极易遭受缺氧性损伤。肾脏缺氧是急性肾损伤和慢性肾病的显著特征,在其发生和进展中起关键调节作用。缺氧使肾小管上皮细胞(TECs)转化为病理性分泌表型并产生多种促炎因子,招募巨噬细胞从而引发肾小管间质性肾炎。TECs 持续缺氧会导致缺氧诱导因子-1α (HIF-1α) 的过度激活,从而刺激部分上皮间质转化和间质纤维化,最终导致肾衰竭。缺氧是慢性肾病进展为终末端肾病的最终共同途径,对肾缺氧进行无创和特异性成像,将有助于识别缺氧区域,预测肾功能衰退,监测治疗反应,进而达到更好的治疗效果。
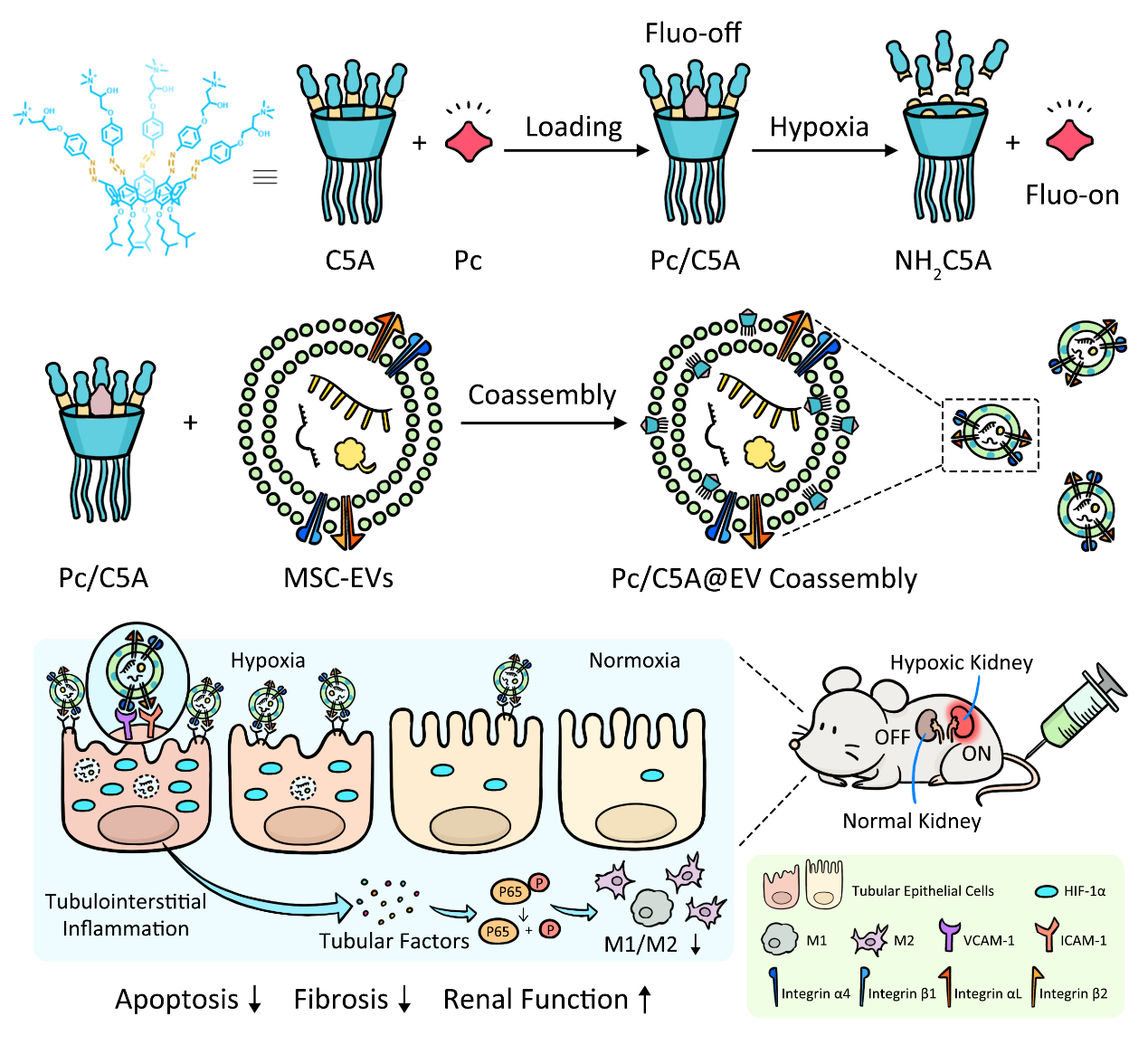
间充质干细胞分泌的细胞外囊泡 (MSC-EVs) 对损伤肾脏具有良好趋向性,并可有效促进肾脏再生。MSC-EVs本身特有的免疫逃逸和降低脱靶效应的特性,可以有效提高其作为载体递送药物的效率。基于MSC-EVs特殊的生理功能和目前肾脏缺氧成像手段的局限性,该文作者开发出一种全新的纳米级缺氧响应性共组装体系Pc/C5A@EVs,由大环两亲化合物 (C5A)、商业染料磺化铝酞菁 (Pc) 和MSC-EVs组成。将近红外染料Pc封装在C5A的空腔中,形成缺氧敏感的主客体复合物Pc/C5A。络合诱导的荧光猝灭赋予 Pc/C5A 复合物缺氧敏感的成像特性。由于C5A 正电性和两亲性,可以与MSC-EVs形成Pc/C5A@EVs共组装体,该共组装体克服了共价缺氧成像模态分子设计复杂、合成分离耗时昂贵等问题,并且通过MSC-EVs的靶向递送,实现了精准的肾脏损伤成像与治疗一体化。
在肾损伤小鼠体内,MSC-EVs表面整合素α4β1/αLβ2与缺氧损伤TECs表面高表达的血管细胞粘附分子-1 (VCAM-1)/细胞间细胞粘附分子-1 (ICAM-1) 之间相互作用,介导了Pc/C5A@EVs共组装体在缺氧肾脏中特异性的富集,缺氧肾脏中高表达的偶氮还原酶触发Pc染料释放,从而实现了实时精准的缺氧敏感成像。同时,Pc/C5A@EVs 通过抑制TECs中HIF-1α的表达,抑制了促炎因子的分泌,进而诱导 M1型到M2型巨噬细胞的转变,减轻了肾脏组织的炎症浸润,进一步抑制了肾脏细胞凋亡和纤维化进程,实现了理想的肾脏修复。这项研究提出的诊断和治疗一体化纳米体系为肾脏疾病治疗提供了全新思路。
参考文献:
Coassembly of hypoxia-sensitive macrocyclic amphiphiles and extracellularvesicles for targeted kidney injury imaging and therapy. Journal of Nanobiotechnology.2021 Dec 27;19(1):451.