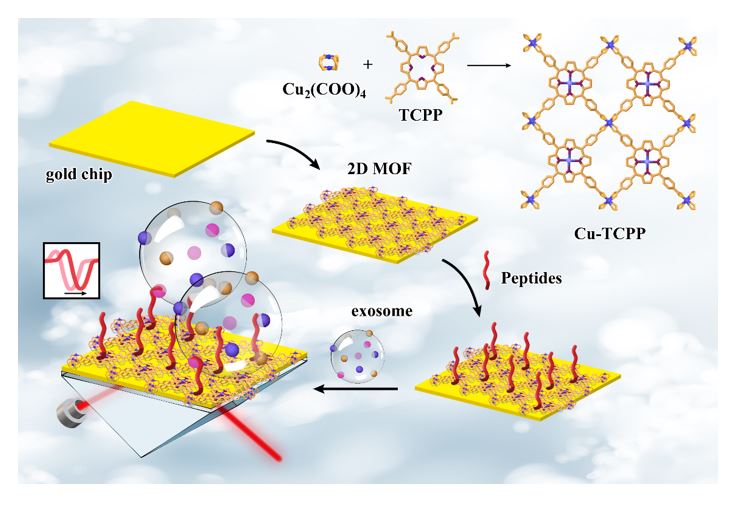
PD-L1外泌体作为潜在的癌症生物标志物,已被发现可以用于癌症发展和转移的诊断。乳腺癌、非小细胞肺癌、头颈部鳞状细胞癌、胶质母细胞瘤和黑色素瘤等不同类型的肿瘤细胞均能分泌出在其质膜上表达程序性死亡配体-1(PD-L1)的外泌体。因此,PD-L1外泌体有望成为一种极具吸引力的癌症诊断和预后的新型生物标志物,其检测对于临床诊断和精准医疗具有重要意义。表面等离子共振 (SPR) 光谱是一种通过监测折射率 (RI) 的变化来检测传感界面的分子相互作用的光学技术。为了满足痕量疾病生物标志物超灵敏检测的需求,迫切需要研究出可用于改变传感界面等离子体性质的二维纳米材料,从而提高SPR的检测灵敏度。 Cu-TCPP二维金属有机框架(2D MOF)具有厚度超薄、结构高度有序、表面活性位点多、比表面积大、电子迁移率和光吸收性能优异、生物相容性良好、合成方法简单快速等多种优点,在SPR增敏方面具有巨大的应用潜力,有望成为一种良好的光学传感材料。近日,上海大学生命科学学院陈红霞团队以“Rapid and sensitive detection of PD-L1 exosomes using Cu-TCPP 2D MOFas a SPR sensitizer”为题在Biosensors and Bioelectronics(2022Jan 5;201:113954)上发表论文,报道了使用 Cu-TCPP 2D MOF 作为 SPR 传感界面增敏层快速灵敏检测 PD-L1 外泌体的方法。上海大学生命科学学院的陈红霞教授、胡晓君博士为文章的共同通讯作者,硕士研究生王音典为文章的第一作者。研究者采用简单水热法合成的 2DMOF 直接沉积在金芯片表面,构建了基于 2D MOF 的SPR 生物传感器,以提高微量癌症生物标志物的检测灵敏度。相比于传统金基传感器,2D MOF修饰后的SPR传感器的RI灵敏度(S)、检测精度(DA)和品质因数(FOM)三个关键参数得到了显著的提高。这可能归因于:第一,2D MOF具有优异的导电性、电荷迁移率和高效的光生载流子,可以增强传感界面的激发电场和表面等离子体共振。第二,作为一种优良的光电材料,2D MOF可以增强对入射光的吸收,从而增强信号输出。第三,2D MOF为层状结构,排列高度有序,其自身的SPW与金膜的SPR耦合。最后,作为二维材料,2D MOF具有较大的比表面积,TCPP配体的苯环结构可以更好地与碳基生物分子结合,为识别分子提供更多的活性位点,从而增强信号分子捕获能力。研究者使用了一种新设计的多功能肽(该肽包含四个域:防污域、组装域、结合域和识别域)作为探针,进行PD-L1外泌体传感实验。SPR传感器对PD-L1外泌体的检出限为16.7 particles /mL。通过分析人血清样本中的PD-L1外泌体进一步验证了该传感器的可靠性和实用性,回收率在93.43 %-102.35%范围内。研究提示鉴于其出色的信号放大能力,Cu-TCPP2D MOF可以作为一种理想的 SPR 增敏剂,用于快速、灵敏地检测微量癌症疾病标志物PD-L1外泌体。Rapid and sensitive detection of PD-L1 exosomes using Cu-TCPP 2D MOF as aSPR sensitizer. Biosens Bioelectron. 2022,5;201:113954.外泌体资讯网 Biosensors and Bioelectronics |上海大学陈红霞团队:快速灵敏检测外泌体PD-L1的新技术策略