从肠道泄漏的各种微生物产物会加剧肥胖症中的组织炎症和代谢紊乱。Vsig4+巨噬细胞是防止细菌及其产物渗入宿主组织的关键因素。然而,在肥胖相关胰岛异常的发病机制中,胰岛Vsig4+巨噬细胞在微生物群和β细胞之间的通讯中的作用尚不清楚。近日,Nature Communications杂志上的一篇文章报道发现细菌DNA在肥胖个体的β细胞中富集。含有肠道微生物DNA的细胞外囊泡(mEV)很容易通过肥胖者的肠道屏障并将微生物DNA传递到β细胞中,通过触发cGAS/STING激活导致炎症升高和胰岛素分泌受损。
作为肥胖的标志,低度组织炎症表现在各种器官中,包括脂肪组织、肝脏、肌肉和胰岛。慢性胰岛炎症存在于各种肥胖和2型糖尿病(T2DM)小鼠模型以及肥胖/T2DM患者的胰岛中。这种肥胖引起的胰岛炎症会导致2型糖尿病的β细胞异常。然而,肥胖引起的胰岛炎症的机制尚不完全清楚。
健康受试者的特点是肠道微生物群的多样化组成和正常的功能性肠道屏障。相比之下,肥胖者的肠道微生物群表现出深刻的功能和组成变化,统称为生态失调。此外,肠道屏障破坏是肥胖的一个公认特征,导致微生物群衍生产物泄漏到宿主的循环和远处器官中。更重要的是,新出现的证据表明,在肥胖的情况下,微生物代谢物会加剧组织炎症和代谢紊乱。先前的研究表明,微生物群衍生物可能会泄漏到胰岛中并有助于T1DM的发展。最近的研究还表明,肥胖伴随着人类和小鼠循环和代谢组织中微生物DNA的富集。此外,循环微生物DNA可能是预测代谢疾病发展的特征。有明确的证据表明,细胞外囊泡(EV)可以将各种货物(包括RNA、DNA、蛋白质和脂质)从一种细胞类型运输到其他相邻或远处的细胞。新出现的证据表明,EV介导的细胞通讯对肥胖相关的代谢反应具有深远的调节作用。多种微生物可以产生释放到宿主循环中的EV。因此,作者假设,微生物群衍生的EVs包裹着微生物DNA(mEVs),在肥胖的情况下,在介导胰岛炎症和β细胞功能障碍中发挥作用。
巨噬细胞是存在于胰岛的主要免疫细胞类型。几项研究观察到,与瘦个体相比,肥胖患者和肥胖动物模型的胰岛巨噬细胞数量显著增加。最近的研究还表明,胰岛巨噬细胞的扩增和功能转换有助于胰岛炎症的发展,这种炎症在肥胖的情况下介导β细胞增殖和胰岛素分泌。在正常状态下,胰岛巨噬细胞是平衡胰岛炎症微环境的关键角色。例如,免疫球蛋白家族的补体受体(Vsig4+)胰岛巨噬细胞是一组用于吞噬循环病原体的补体系统的先天免疫细胞,可以在胰岛周围建立保护屏障,以防止自身免疫反应和T1DM的发生。此外,肝脏中的Vsig4+Kupffer细胞可以有效清除门静脉引流肠道的细菌及其产物。Vsig4+巨噬细胞捕获异物的能力主要取决于补体蛋白C3介导的调理作用。然而,胰岛Vsig4+巨噬细胞在预防肥胖相关胰岛炎症和β细胞异常发展中的作用仍然未知。
该研究表明肠道mEV可以转移到宿主循环中,并将微生物DNA转移到肥胖的胰腺β细胞中,导致胰岛炎症和β细胞异常增加。胰岛Vsig4+巨噬细胞可以通过C3介导的机制阻止肠道mEVs浸润到β细胞中,而肥胖症患者长期肥胖会导致Vsig4+巨噬细胞数量显著减少,从而允许肠道mEVs的扩散和肥胖小鼠和β细胞内的微生物DNA富集。微生物DNA的去除减弱了肠道mEV的致病作用。细菌DNA的积累可通过触发cGAS/STING通路的激活来引发炎症反应并损害β细胞的胰岛素分泌。
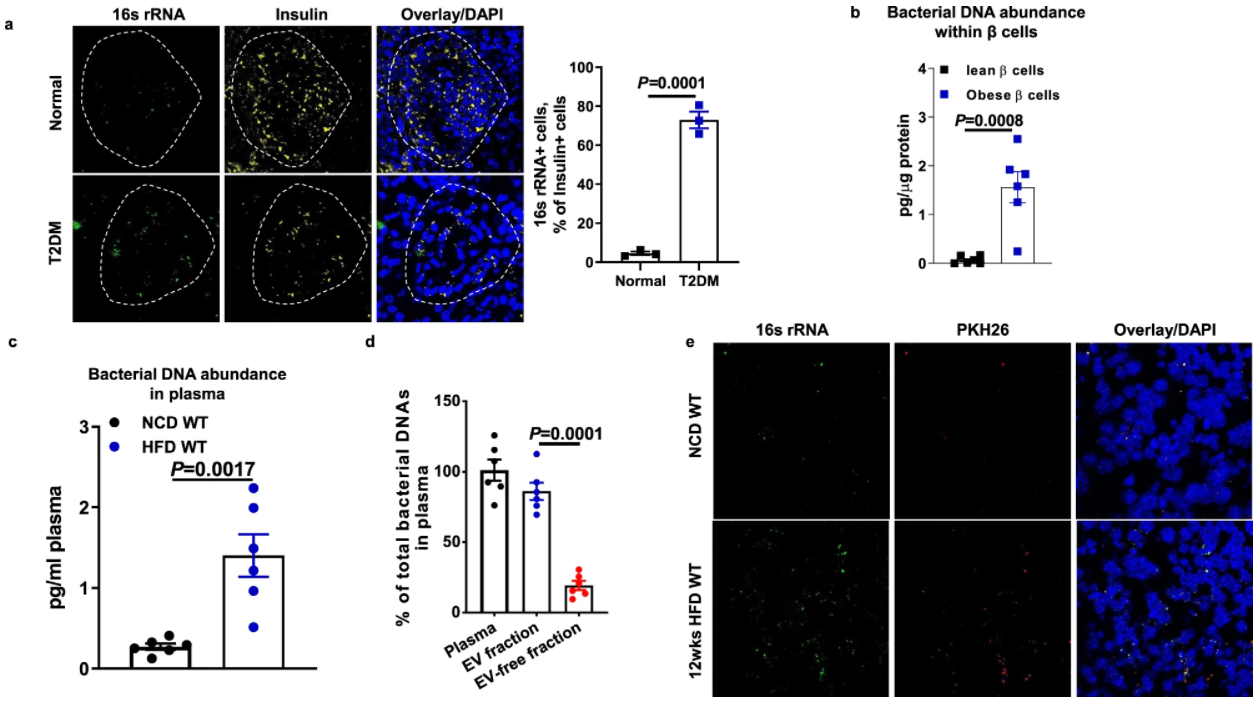
肥胖会导致含有细胞外囊泡(mEV)的微生物DNA从肠腔泄漏到胰腺β细胞中
参考文献:
Gao H,Luo Z, Ji Y, Tang K, Jin Z, Ly C, Sears DD, Mahata S, Ying W. Accumulation ofmicrobial DNAs promotes to islet inflammation and β cell abnormalities inobesity in mice. Nat Commun. 2022 Jan 28;13(1):565. doi:10.1038/s41467-022-28239-2. PMID: 35091566; PMCID: PMC8799656.