腹主动脉瘤(abdominal aortic aneurysm, AAA)是指腹主动脉的永久性和不可逆性局部扩张,破裂后患者的死亡率高达65-85%。巨噬细胞参与细胞外基质的重塑、炎症的促进与消退等过程,在AAA的发生过程中起关键作用。AAA发生过程中,在组织损伤产生的趋化因子和细胞因子、细胞外基质降解产物和微环境条件等的影响下,大量外周血单核细胞迁移至血管壁。但除了微环境中外在因素的影响,调控巨噬细胞迁移的细胞内潜在机制仍需进一步研究。
近日,来自北京大学基础医学院和北京大学第三医院介入血管外科的合作研究发现,糖酵解过程中的关键酶M2型丙酮酸激酶(pyruvate kinase muscle isozyme 2,PKM2)介导T淋巴细胞释放细胞外囊泡(extracellularvesicles, EVs)促进巨噬细胞迁移而加重AAA发病,并且此结果在AAA相关临床样本中也得到了部分验证。以上研究结果以“Tlymphocyte-derived extracellular vesicles aggravate abdominal aortic aneurysmby promoting macrophage lipid peroxidation and migration via pyruvate kinasemuscle isozyme 2”为题发表在Redox Biology上(2022,4;50:102257)。该研究受到国家自然科学基金委“血管稳态与重构的调控机制”重大研究计划的支持。
葡萄糖代谢失调与AAA密切相关。在这项研究中,研究人员首先发现在弹力蛋白酶诱导的小鼠AAA模型中,血管损伤处CD4+ T淋巴细胞糖酵解途径的限速酶PKM2表达增高;AAA患者外周血T淋巴细胞PKM2表达也升高;T淋巴细胞特异性敲除PKM2后,小鼠AAA发病率和严重程度减轻;血管壁浸润的免疫细胞尤其是巨噬细胞减少;提示PKM2可能介导T淋巴细胞与巨噬细胞的相互作用而参与AAA发生。
EVs作为细胞间信使,介导细胞间通讯。在这项研究里,通过荧光细胞动态分析实验和Transwell实验,研究人员发现PKM2激活的T淋巴细胞释放EVs可增加巨噬细胞铁累积和脂质过氧化,进而促进细胞迁移。高通量脂质代谢组学测定结果显示,PKM2激活的T淋巴细胞释放的EVs中含多不饱和脂肪酸的磷脂(如20:4 PE和22:6 PE)增多;这些EVs被巨噬细胞吞噬后进入巨噬细胞内,从而为靶细胞提供更多的脂质过氧化底物。从AAA患者血浆中提取的EVs同样能通过增强巨噬细胞铁蓄积和脂质过氧化而促进其迁移能力。最后,通过给小鼠腹腔注射外泌体抑制剂GW4869可减轻AAA的发生,进一步验证了包括外泌体在内的EVs在AAA中起着重要的作用。
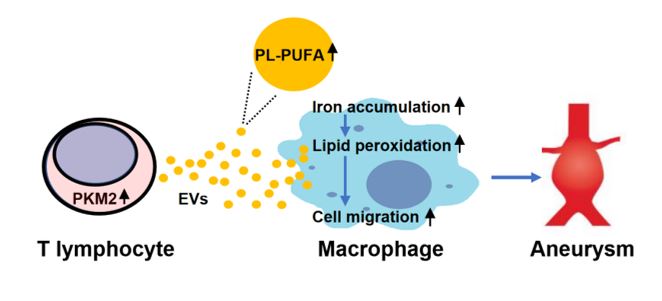
这项研究结果从细胞间对话和细胞代谢的角度,揭示PKM2激活的T淋巴细胞可产生富含脂质的EVs,通过促进巨噬细胞氧化还原失衡和迁移来驱动AAA发生。因此,靶向T淋巴细胞-EVs-巨噬细胞轴可能是预防和治疗AAA的潜在策略。
参考文献:
T lymphocyte-derivedextracellular vesicles aggravate abdominal aortic a 1 neurysm by promoting macrophagelipid peroxidation and migration via pyruvate kinase muscle isozyme 2. Redox Biol. 2022, 50:102257.doi: 10.1016/j.redox.2022.102257.
外泌体资讯网 Redox Biology | 北京大学医学部冯娟/王宪团队:T淋巴细胞释放富含脂质的细胞外囊泡促进巨噬细胞迁移而加重腹主动脉瘤





