骨质疏松症(Osteoporosis, OP)和血管钙化(Vascular calcification, VC)常在老年人中伴随发生。OP是一种严重危害骨骼健康的慢性疾病,其导致的骨质疏松性骨折是老年患者致残和致死的主要原因之一;VC会造成动脉弹性降低,引起血流动力学改变,显著增加心血管事件风险。这种一方面是骨骼成骨不足、另一方面是血管壁异位骨化增加的现象称为骨与血管“钙化矛盾”。骨髓间充质干细胞(BMSC)分化命运改变(成骨减少、成脂增加)和血管平滑肌细胞(VSMC)成骨转分化分别是导致骨质疏松症和血管钙化的主要细胞学基础,其同时发生的具体调控机制仍有待深入阐明。
2022年3月18日,中南大学湘雅医院谢辉教授团队在Nature Communications上发表题为“Aged bone matrix-derived extracellular vesicles as amessenger for calcification paradox”的原创性研究成果 (2022, 18;13(1):1453)。该研究揭示了衰老骨基质胞外囊泡(AB-EV)能进入骨髓腔和血管组织促进BMSC成脂分化和VSMC成骨转分化,进而诱导骨——脂失衡和加剧血管钙化。
骨骼约占人体总重量的五分之一,是人体中最大的器官之一。骨骼是一种代谢高度活跃的器官,在整个生命过程中不断地重塑。随着旧骨被破骨细胞移除并被成骨细胞合成新骨取代,成人骨骼每10年就会完全翻新一次,这注定骨骼终生持续释放大量无机物与有机物。骨细胞存在于骨基质中,数量多(占骨骼细胞的90-95%)、寿命长(达数十年)、辐射广(其表面大量向外延伸的树状突触长度总和达到约17.5万公里),彼此之间以及与骨表面上的成骨细胞和破骨细胞相互连接,形成广泛的神经元样细胞投射网络。骨细胞发挥重要的旁分泌与内分泌代谢调控作用。譬如,谢辉教授团队前期也发现了骨细胞神经肽Y参与“神经-骨轴”介导自主神经信号通过调控骨髓微环境影响骨代谢。胞外囊泡(Extracellularvesicles,EV)是细胞、组织与器官间通过“囊泡运输”进行信息传递的关键信使,广泛影响机体的病理生理过程。
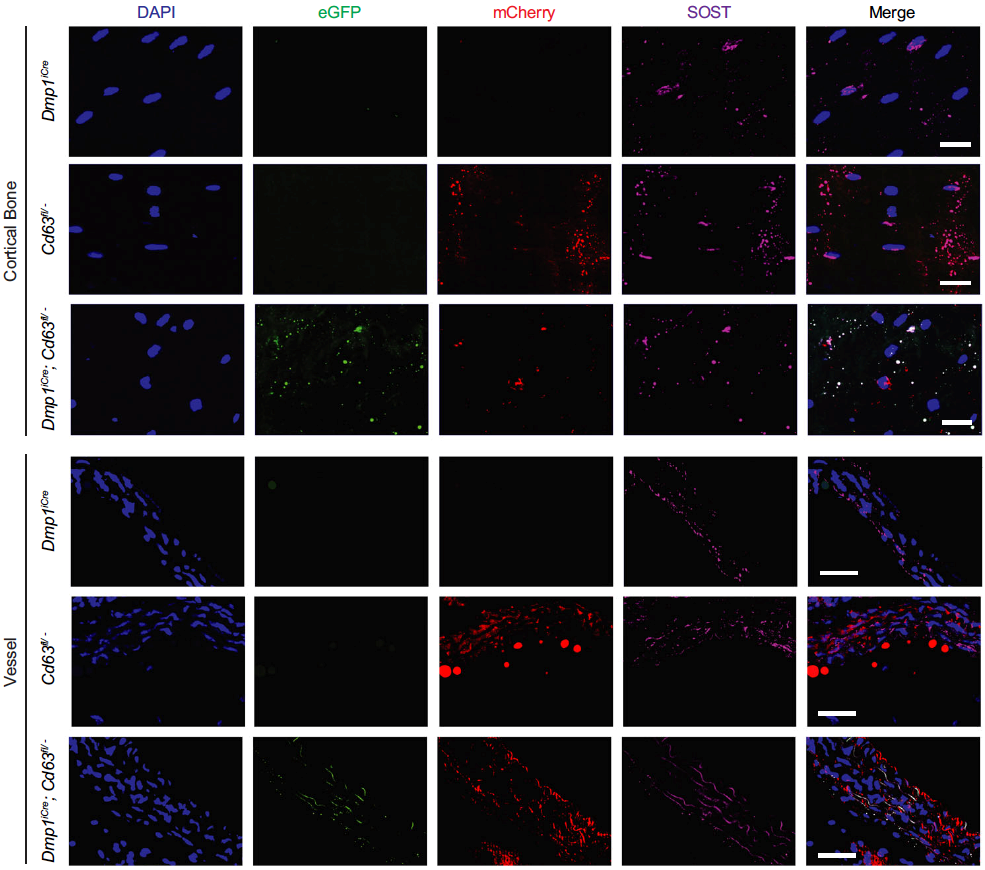
为了探索骨基质胞外囊泡(B-EV)的来源细胞及其在体内的分布,谢辉教授团队自主构建了CD63(EV表面标志蛋白)条件性基因敲入的Cd63em(loxp-mCherry-loxp-eGFP)3小鼠(简称Cd63fl/−小鼠)。将该小鼠与牙本质基质蛋白1(Dentin matrix protein 1,DMP1;骨细胞标志蛋白)阳性细胞特异性表达Cre酶的工具鼠Dmp1Cre小鼠杂交,获得了骨细胞EV示踪小鼠(Dmp1Cre;Cd63fl/−)。利用该示踪小鼠确证了骨基质胞外囊泡(B-EV)主要由骨细胞分泌,并且可转运到主动脉血管壁(图1)。
图1骨细胞EV在骨基质和主动脉血管壁的示踪分析
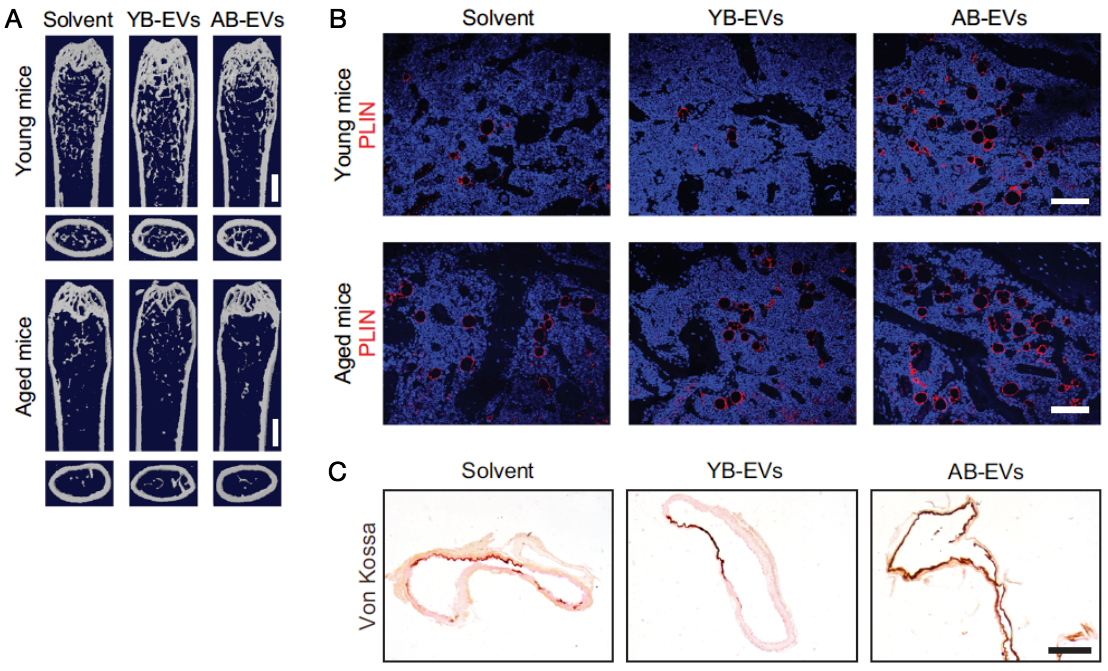
来源于衰老机体的B-EV(AB-EV)能显著促进BMSC成脂分化和VSMC成骨转分化;将其经骨髓腔注射到小鼠体内,导致骨量减少(图2A)和骨髓腔脂肪增多(图2B),并加剧血管钙化(图2C)。然而,来源于年轻机体的B-EV(YB-EV)则无上述功能。
图2 AB-EV导致小鼠骨量减少(A)和骨髓腔脂肪增多(B),并加剧血管钙化(C)
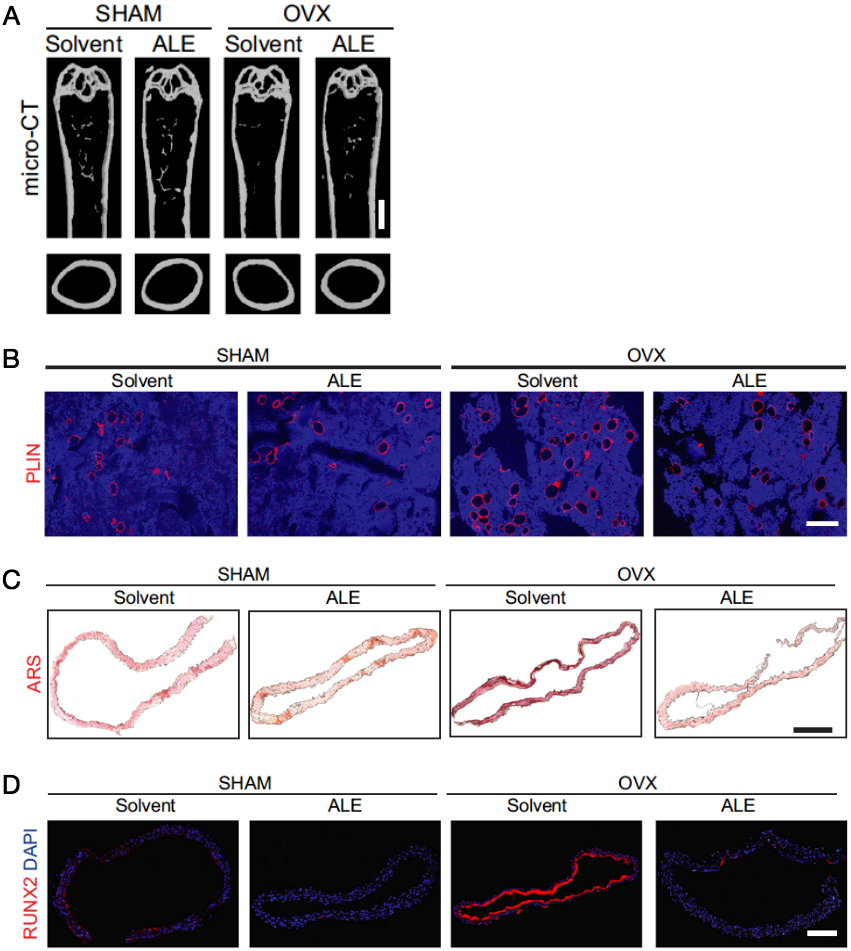
在破骨细胞骨吸收的过程中,B-EV被释放到骨髓腔中,并能随血液循环转运到血管组织。骨吸收抑制剂阿仑膦酸钠(目前临床上应用最广的一线骨质疏松症治疗药物)能明显抑制AB-EV的释放,显著减轻老年去卵巢小鼠(绝经后骨质疏松症模型)骨量减少和骨髓腔脂肪堆积,并能明显缓解去卵巢(因雌激素缺乏引起破骨细胞骨吸收增加)引起的小鼠血管钙化加剧(图3)。
图3阿仑膦酸钠(ALE)缓解老年OVX小鼠的骨脂失衡(A、B)与血管钙化(C、D)
机制研究表明,AB-EV富集miR-483-5p和miR-2861,其中miR-483-5p介导AB-EV促进BMSC成脂分化和骨-脂失衡,miR-2861则介导AB-EV诱导VSMC成骨转分化从而促进血管钙化。
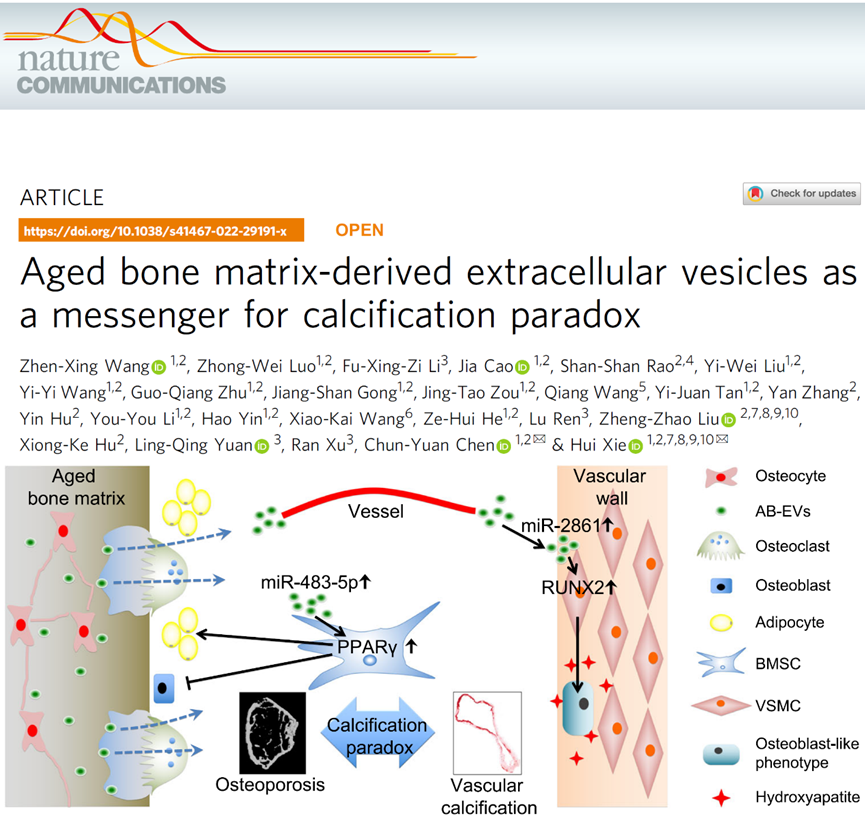
综上所述,该研究揭示了AB-EV在骨内调控骨代谢和跨器官影响血管钙化进程这一新型“骨-血管轴”调控模式(图4),还发现阿仑膦酸钠通过抑制骨吸收同时改善老年机体骨质疏松和血管钙化,为老年骨质疏松症和血管钙化的防治提供了新思路。
图4衰老骨基质来源胞外囊泡参与骨与血管“钙化矛盾”形成的机制模式图
参考文献:
Aged bone matrix-derived extracellularvesicles as a messenger for calcification paradox, Nat Commun.2022,18;13(1):1453. doi: 10.1038/s41467-022-29191-x.
中南大学湘雅医院谢辉教授和陈春媛特聘副研究员为该论文共同通讯作者,王振兴助理研究员为该论文第一作者,罗忠伟博士、李付杏子博士和曹加助理研究员等为该论文的重要参与作者。中南大学湘雅医院为该论文的第一作者兼通讯作者单位。该研究得到了国家自然科学基金委、中国医学科学院、湖南省科技厅、中国博士后科学基金会等的资助。
外泌体资讯网 Nature Communication | 中南大学湘雅医院谢辉教授团队:骨基质胞外囊泡介导衰老机体骨与血管“钙化矛盾”