外泌体是由人体组织分泌并反映代谢状态的血浆转运囊泡。外泌体的特征(尤其是 microRNA 含量)在代谢疾病中发生了改变。来自波士顿大学医学院的研究人员在NatureReviews Endocrinology杂志上发表评论文章,阐述了在2型糖尿病中,血浆中循环的外泌体诱导与肿瘤进展相关的转录变化和靶向癌细胞的转移前表型,可能将肥胖与癌症进展和转移联系起来[1]。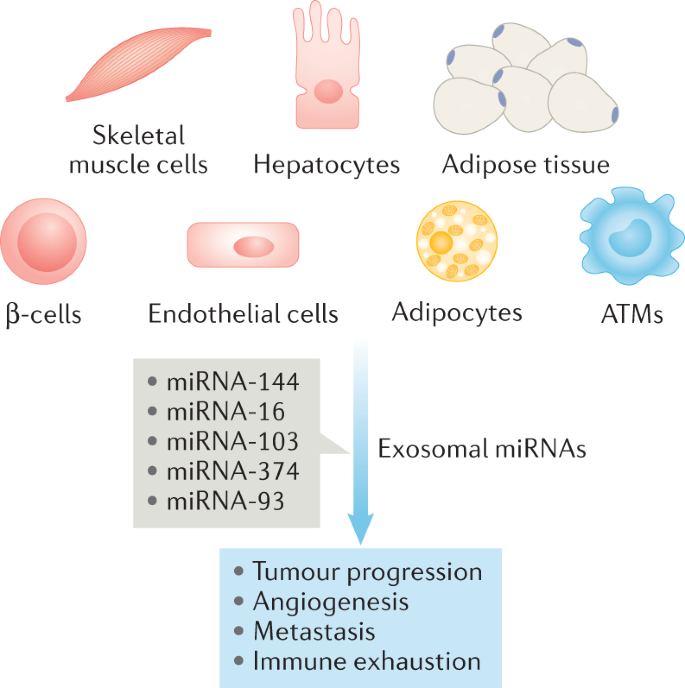
图:代谢紊乱患者的循环外泌体可诱导肿瘤进展
40年前,外泌体首次通过电子显微镜观察为由含有酶活性的培养细胞脱落的囊泡。在接下来的20年里,研究人员在很大程度上忽略了外泌体,认为它们只不过是废物处置系统。然而,2007年一篇突破性论文描述了人和小鼠细胞系和原代细胞中的外泌体mRNA 和 microRNA (miRNA),这表明这些潜在的基因调控物质可以被转运到新的组织以重新编程细胞。胶质母细胞瘤细胞和星形胶质细胞分泌的外泌体线粒体DNA的研究引起了进一步的兴趣。外泌体现在被认为是大小为 50-200nm 的细胞外囊泡,由大多数或所有体细胞释放,并承担比垃圾处理更多的功能。重要的是,它们可以包含受原细胞代谢状态影响的生物活性分子。外泌体在血液和淋巴液中循环的能力表明,这些代谢信号可以在全身传播,将指令传递给目标组织。过去15年的发现突出了这种新的细胞间通讯机制的潜在重要性。该研究团队在尚未经过同行评审的预印本论文[2]中发表的初步工作表明,来自 2 型糖尿病 (T2DM) 成人的血浆外泌体将前列腺癌细胞系DU145重新编程为更具侵袭性和促转移性体外表型。引人注目的是,来自不同T2DM的血浆外泌体在DU145细胞中产生了变化,RNA测序数据的主成分分析鉴定了不同的外泌体种类,每种外泌体具有独特作用。从患有T2DM的成年人获得的血浆中外泌体的miRNA谱也不同于没有糖尿病的对照个体。这些初步研究结果表明,在T2DM患者的外泌体中上调的miRNA-374和miRNA-93,上调了DU145细胞中与免疫耗竭和与肿瘤转移相关的间充质表型有关的重要基因的转录。研究团队的另一项研究[3]报告了一个证据,证明来自胰岛素抵抗或T2DM个体脂肪细胞的外泌体如何在体外重编程上皮样乳腺癌细胞系,使其变得更具侵袭性、变成间充质样细胞。这些发现表明,外泌体不仅反映了患者的代谢状态,而且还携带可能不同地驱动肿瘤进展的功能指令。这一假设可以解释为什么癌症合并肥胖或代谢疾病的患者比代谢正常的癌症患者表现出更多的晚期癌症和更差的结果。患有代谢并发症和相关炎症的乳腺癌和肥胖患者的脂肪微环境可能参与细胞因子、趋化因子、代谢物和外泌体与恶性癌细胞间的通讯。研究团队认为,与代谢正常的患者的脂肪微环境相比,这种微环境可能会引发更多的转录可塑性和促转移行为。体重指数BMI和T2DM与外泌体浓度和有效货物含量的改变有关。来自T2DM个体的循环外泌体可以被单核细胞内化,并且由于它们不同的有效货物,改变了与细胞存活、氧化应激、炎症和免疫功能相关的信号通路。这种机制可以将脂肪组织和肿瘤细胞与免疫微环境和肥胖相关癌症中的特定白细胞浸润联系起来(如图所示)。最后,妊娠期糖尿病 (GDM) 的发病率正在上升,GDM被定义为发生在妊娠中期或晚期的葡萄糖耐受不良。几项研究已经对 GDM 孕妇的血浆外泌体microRNA进行了表征,并报告了miRNA-144、miRNA-16和miRNA-103 水平上调。在人体研究和体外细胞系模型中,这些miRNA与实体瘤恶性肿瘤和转移进展有关。这一发现表明,GDM中的系统性外泌体通讯可能会加剧肥胖相关癌症的风险。通过设计外泌体分析方法,可以评估来自患者的血浆中的外泌体miRNA,并评估它们对癌症进展的重要性。癌症患者代谢异常和慢性炎症的无创血浆外泌体生物标志物可以被制成试剂盒,并与经过验证的诊断方式(如影像学和肿瘤组织学)相结合,以改善风险评估和临床决策。这种方法对于合并症的患者可能特别重要,不愿意进行重复活检的患者可能更愿意提供血液(或其他侵入性更小的体液,例如尿液和唾液)用于外泌体分析。总之,外泌体是由所有细胞类型分泌的循环纳米直径囊泡。个体代谢状态决定了循环外泌体的独特miRNA谱。与代谢正常的成年人的组织不同,从患有胰岛素抵抗或T2DM的成年人组织释放到血浆中的外泌体miRNA与肿瘤进展、血管生成、转移和免疫衰竭相关。外泌体含量受营养摄取、细胞应激和代谢状态的调节。外泌体miRNA 货物可以通过重新编程转录网络来影响远处的细胞。研究人员建议使用血浆外泌体作为非侵入性生物标志物可能有助于临床医生更好地管理癌症患者的治疗策略,并帮助内分泌学家更好地管理代谢性疾病患者的治疗。此外,药物递送是外泌体的一个有前景的应用。外泌体生物学领域发展迅速,然而外泌体在精准医学中的最佳用途尚未确定。1. Jafari N, et al. Exosomes as novelbiomarkers in metabolic disease and obesity-related cancers. Nat RevEndocrinol. 2022 Mar 31.2. Jafari, N. et al. Novel plasma exosomebiomarkers for prostate cancer progression in co-morbid metabolic disease.Preprint at bioRxiv (2022).3. Jafari, N. et al. Adipocyte-derivedexosomes may promote breast cancer progression in type 2 diabetes. Sci. Signal (2021).外泌体资讯网 43分评论文章阐述外泌体在代谢性疾病相关癌症诊疗中的价值