肝细胞癌(HCC)是世界范围内最致命的恶性肿瘤之一,严重威胁人类健康,但目前尚无有效的非手术治疗方法。尽管基于免疫检查点的免疫疗法具有很大潜力,但对于肝癌的免疫疗效十分有限,响应率仅有5%-10%。主要由于HCC患者的肿瘤异质性和复杂度极高,微环境中严重缺乏足够的肿瘤特异性免疫细胞,且对病人个体肿瘤特异性抗原,特别是对肿瘤新生抗原缺乏有效识别,是现有肝癌免疫疗法面临的最大挑战。因此,亟需研发可有效识别肿瘤特异性抗原并具有普适性的个体化免疫疗法。
近日,天津医科大学基础医学院尹海芳教授团队在国际权威期刊Journal ofHematology&Oncology在线发表了题为“Universalimmunotherapeutic strategy for hepatocellular carcinoma with exosome vaccinesthat engage adaptive and innate immune responses”的研究成果(2022 Apr 29;15(1):46)。该研究首次报道了基于DEX(树突状细胞外泌体)通用型抗肿瘤疫苗策略,通过实现靶向肝细胞癌的内源性树突状细胞招募、激活和交叉提呈肿瘤抗原,特别是肿瘤新生抗原,从而激活机体适应性及固有免疫应答,在中晚期原位肝细胞癌小鼠中介导有效抗肿瘤免疫应答,实现66%肿瘤彻底根除,为个性化肿瘤疫苗研发提供了理论依据和新策略。

更为欣喜的是,研究人员发现,当利用AFP全蛋白抗原取代AFP212抗原短肽后,获得功能化纳米疫苗-DEXP&A&N,同时将临床应用的促进树突状细胞(DCs)分化的细胞生长因子FMS样酪氨酸激酶3配体(Flt3L)纳入DEXP&A&N疫苗治疗中。结果发现,组合治疗进一步增强了抗肿瘤免疫原性,66.7%的原位肝细胞癌小鼠出现肿瘤的完全清除,并在二次荷瘤后,仍实现了百分之百的存活,诱导了长效的肿瘤特异性T细胞免疫记忆。同时,研究人员还发现,DEXP&A&N疫苗亦可激活了机体内肿瘤抗原特异性抗体反应和增强NK细胞的有效杀伤效应。表明该疫苗通过多重途径激活适应性和固有免疫应答实现增强抗肿瘤免疫应答。
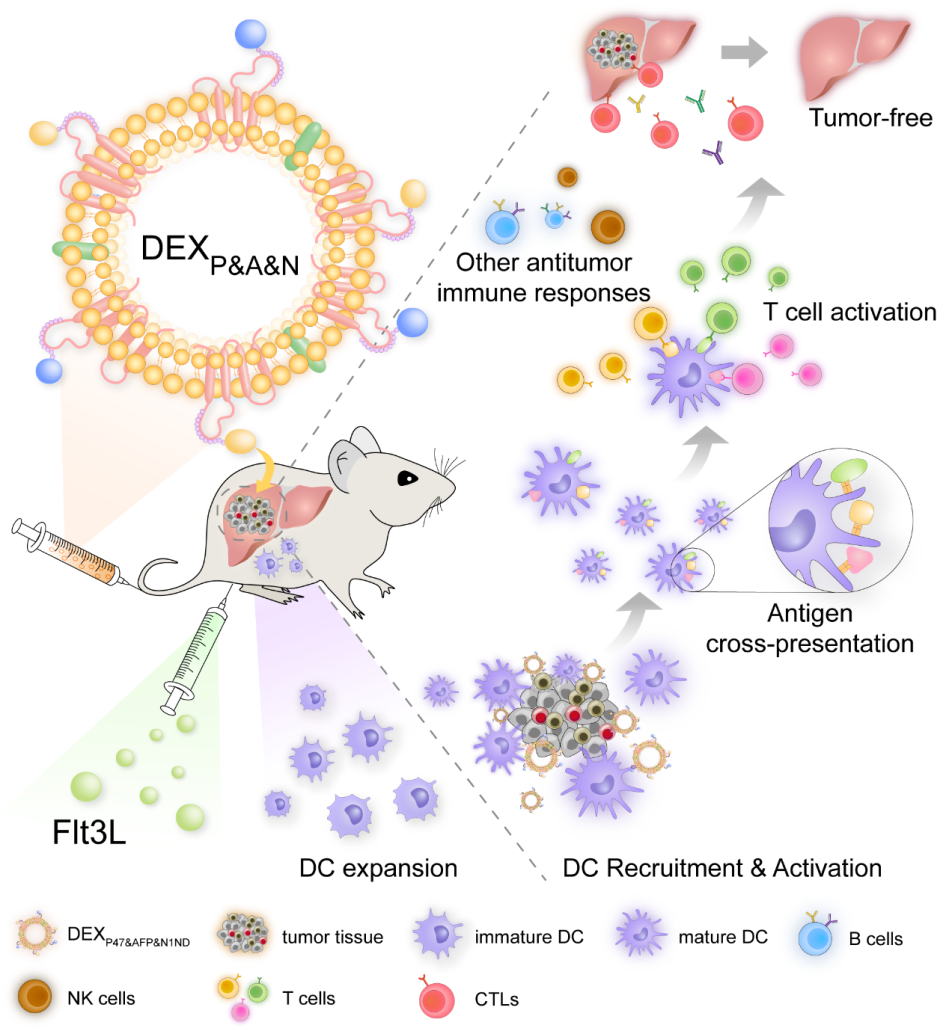
图. 通用型DEX纳米疫苗抗肿瘤机制图
该研究首次提出了一种新型具有普适性的抗肿瘤生物纳米疫苗策略,既可内源性DC的招募、活化和交叉提呈肿瘤新生抗原,亦可激活体内固有免疫应答,显著增强了抗肿瘤免疫应答效应。该新型疫苗策略疫苗的成功研发避免了繁杂的新生抗原鉴定工作,从而达到个体化免疫治疗的目的。为肝细胞癌和其他肿瘤的个性化肿瘤疫苗研发提供了理论依据和创新方法。该研究得到了国家自然科学基金重点项目等基金支持。
外泌体资讯网 J Hematol Oncol | 天津医科大学尹海芳团队:研发一种基于树突状细胞来源外泌体的通用型个体化肿瘤免疫治疗新策略