脑胶质瘤(Glioma)是中枢神经系统最常见的恶性肿瘤,其中胶质母细胞瘤(GBM)恶性程度最高,约占一半以上。传统治疗方式对其效果不佳,术后易复发,生存期短,预后极差。肿瘤的恶性程度不仅取决于肿瘤细胞本身,还取决于肿瘤及其微环境之间的相互作用。肿瘤免疫微环境由许多不同类型的免疫细胞构成,包括肿瘤相关巨噬细胞和小胶质细胞(TAMs)、树突状细胞(DCs)、髓系来源的免疫抑制细胞(MDSCs)、中性粒细胞和淋巴细胞等。近年来大量研究证明,外泌体在脑胶质瘤发生发展及其免疫微环境的形成中发挥了重要作用。
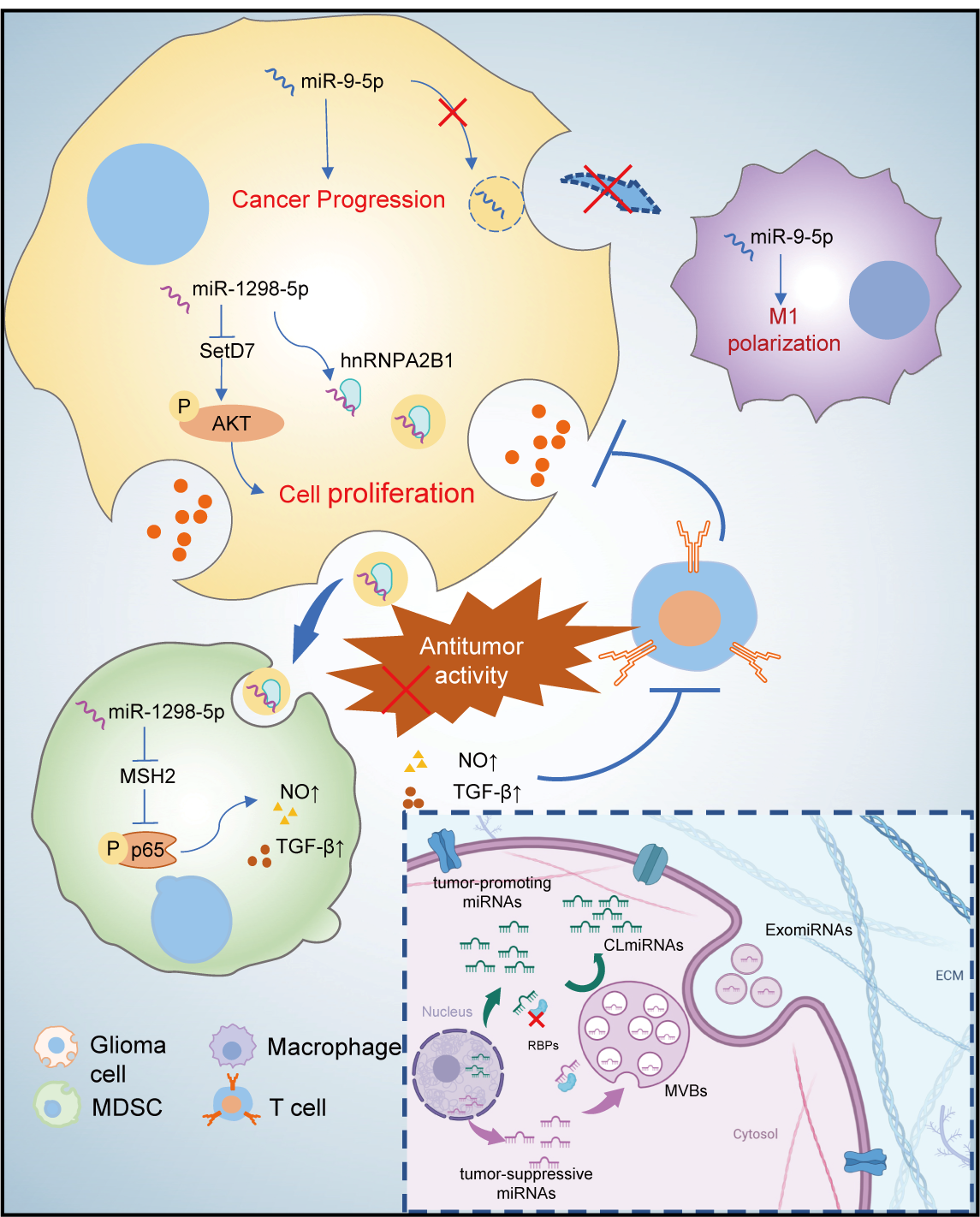
近日,山东大学齐鲁医院李刚教授团队与国家健康医疗大数据研究院薛付忠教授团队在国际权威杂志Cell Death & Disease发表了题为“The dual role of glioma exosomal microRNAs: glioma eliminates tumorsuppressor miR-1298-5p via exosomes to promote immunosuppressive effects ofMDSCs”的文章,首次证明了脑胶质瘤外泌体关键调控组分miRNA普遍存在的双重促肿瘤新机制,山东大学齐鲁医院神经外科李刚教授、薛皓副研究员和国家健康医疗大数据研究院薛付忠教授为共同通讯作者,齐鲁医院神经外科博士生亓彦华为论文第一作者。该研究通过对全级别全亚型脑胶质瘤患者肿瘤组织及其术前、术后和随访期的全病程脑脊液外泌体进行全转录组测序,在国家健康医疗大数据研究院和山大华链健康医疗大数据创新中心协助下,联合开发了国内外首个脑胶质瘤外泌体全病程全组学液体活检大数据库BrainLiquid&CEGA,并利用该数据库对脑胶质瘤患者肿瘤细胞和肿瘤外泌体中的各类分子标志物进行了全面系统研究,发现仅miRNA具有最稳定的表达特征和诊断能力;并将其按照分泌特征分为三大类5种亚型,即外泌体型(外泌体高选择型HSE和外泌体低选择型LSE)、细胞内型(细胞内高选择型HSC和细胞内低选择型LSC)和混合型(MIX)。经跨组学联合分析,发现外泌体高选择型HSE 的miRNAs多为抑癌miRNAs,而细胞内高选择型HSC中存在大量促癌miRNAs,并揭示了肿瘤通过外泌体外排途径进行miRNA双向分选和促肿瘤细胞内、外微环境精细整体细化调控的新机制。并据此提出了,脑胶质瘤外泌体miRNA促肿瘤的双重新机制假说,即一方面通过外排抑癌miRNA达到清除细胞内抑癌分子,促进肿瘤细胞进展的作用;另一方面通过将这些抑癌miRNA利用外泌体靶向运载至肿瘤微环境中的抑制性髓系免疫细胞(肿瘤相关巨噬细胞TAMs或髓系抑制细胞MDSCs),进而发挥促进肿瘤免疫微环境恶化,从而发挥双重促肿瘤的作用。这是首个提出这一假设的研究,为完善脑胶质瘤外泌体对miRNAs的分选机制提供了新的依据。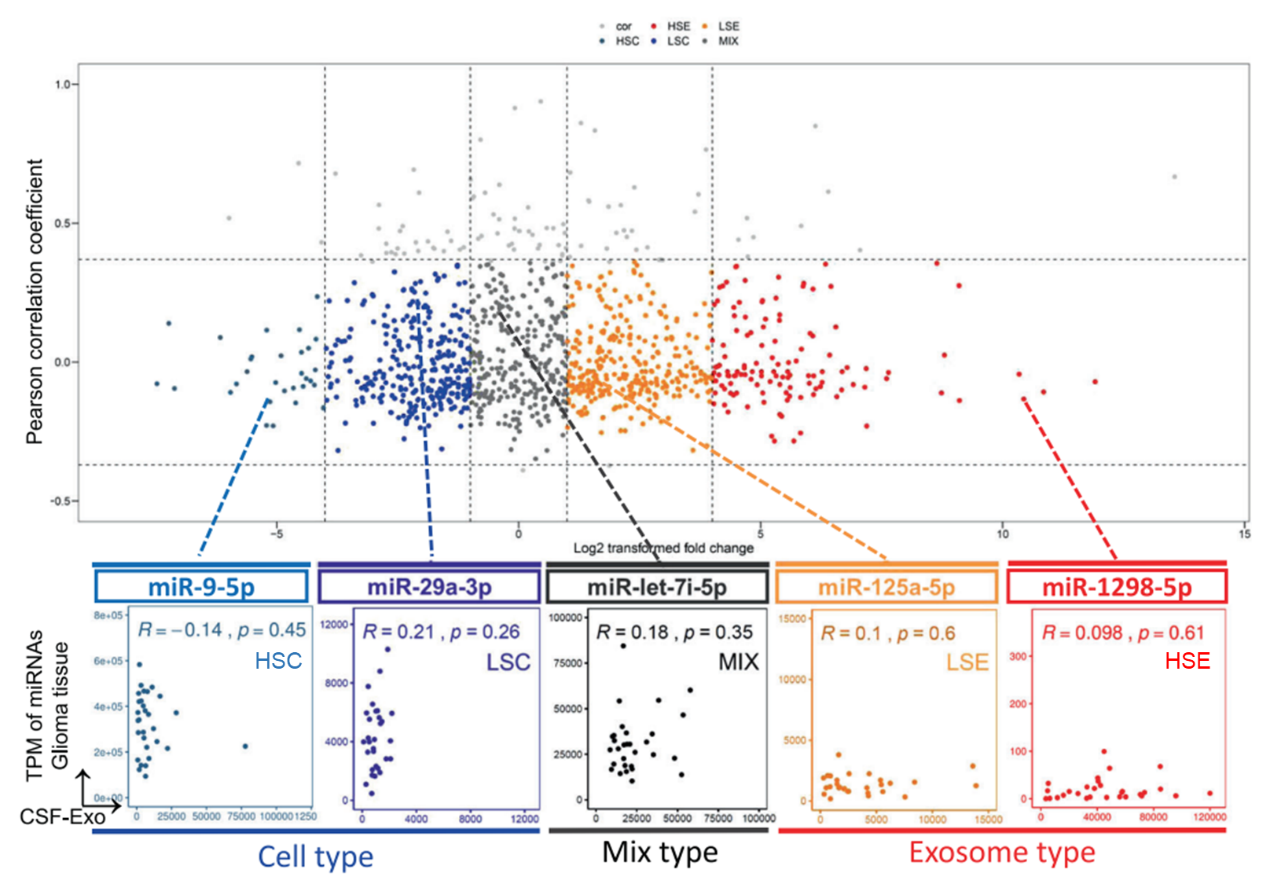 研究者在本文中对代表性外泌体型miRNAsmiR-1298-5p进行了深入研究,发现miR-1298-5p可以通过靶向SetD7影响AKT信号通路来抑制胶质瘤的增殖能力。胶质瘤细胞通过外排蛋白hnRNPA2B1将miR-1298-5p分泌到外泌体中从而将其排出肿瘤细胞,促进肿瘤的恶性进展。为了进一步研究抑癌的miR-1298-5p对免疫微环境的作用,研究者在髓系来源的免疫抑制细胞(MDSCs)中过表达miR-1298-5p。有趣的是,他们发现miR-1298-5p可以促进MDSCs的免疫抑制能力,从而进一步促进肿瘤的恶性进展。上述结果表明,脑胶质瘤可以将抑癌的miRNAs通过外泌体排到细胞外,并且促进肿瘤微环境中免疫细胞的免疫抑制表型的转化,从而达到促进肿瘤恶性进展的双重作用。该研究创新性地提出了胶质瘤外泌体分选miRNAs的新机制,为脑胶质瘤的治疗和诊断提供了新的思路和理论依据。The dual role of glioma exosomal microRNAs: gliomaeliminates tumor suppressor miR-1298-5p via exosomes to promoteimmunosuppressive effects of MDSCs, Cell Death Dis. 2022 May2;13(5):426. doi: 10.1038/s41419-022-04872-z.
研究者在本文中对代表性外泌体型miRNAsmiR-1298-5p进行了深入研究,发现miR-1298-5p可以通过靶向SetD7影响AKT信号通路来抑制胶质瘤的增殖能力。胶质瘤细胞通过外排蛋白hnRNPA2B1将miR-1298-5p分泌到外泌体中从而将其排出肿瘤细胞,促进肿瘤的恶性进展。为了进一步研究抑癌的miR-1298-5p对免疫微环境的作用,研究者在髓系来源的免疫抑制细胞(MDSCs)中过表达miR-1298-5p。有趣的是,他们发现miR-1298-5p可以促进MDSCs的免疫抑制能力,从而进一步促进肿瘤的恶性进展。上述结果表明,脑胶质瘤可以将抑癌的miRNAs通过外泌体排到细胞外,并且促进肿瘤微环境中免疫细胞的免疫抑制表型的转化,从而达到促进肿瘤恶性进展的双重作用。该研究创新性地提出了胶质瘤外泌体分选miRNAs的新机制,为脑胶质瘤的治疗和诊断提供了新的思路和理论依据。The dual role of glioma exosomal microRNAs: gliomaeliminates tumor suppressor miR-1298-5p via exosomes to promoteimmunosuppressive effects of MDSCs, Cell Death Dis. 2022 May2;13(5):426. doi: 10.1038/s41419-022-04872-z.外泌体资讯网 Cell Death Dis | 跨组学大数据驱动肿瘤机制研究:李刚团队与薛付忠团队共同揭示脑胶质瘤外泌体促肿瘤双重作用新机制