干细胞位于一个独特的微环境中,称为干细胞巢,乏氧微环境是影响干细胞巢的关键环境因素之一。不同的氧气浓度可作为信号分子或代谢产物来调控胚胎及成体干细胞的增殖、分化、凋亡等生物学行为。目前,传统MSCs的体外细胞培养条件下氧气浓度为21%,明显高于体内生理条件下的氧气浓度。研究表明在体内动脉血中的氧气张力约为12%;在其它部位的组织中根据部位不同,氧气张力约为在3%~7.4%。牙髓是高血管密度的组织,小鼠牙髓组织的氧气张力为3%左右。细胞所处的微环境不同,其携带的内容有所差异,因此可通过乏氧微环境来调控外泌体的内容物从而调控血管的生成过程。研究者猜测在乳牙牙根生理性吸收这一过程中,处于乏氧微环境中的脱落乳牙牙髓干细胞外泌体可促进血管生成,以代偿机体因血管减少造成的血供减少。因此研究者通过体外乏氧微环境模拟体内生理性微环境来验证SHED细胞经乏氧预处理后外泌体能否促进血管生成,为组织再生及缺血性疾病的治疗提供理论依据。2022年4月26日,山东大学口腔医学院和杭州医学院附属宁波口腔医院郭泾教授、吴训伟教授团队在Frontiersin cell and developmental biology上发表了题为“Exosomes Derived FromHypoxia-Conditioned Stem Cells of Human Deciduous Exfoliated Teeth EnhanceAngiogenesis via the Transfer of let-7f-5p and miR-210-3p”的文章 (2022 Apr 26;10:879877),阐述了乏氧预处理后人脱落乳牙牙髓干细胞(SHED)来源外泌体通过let-7f-5p及miR-210-3p 促进血管生成的作用机制及方式。该文章的第一作者为山东大学口腔医学院的刘盼盼博士生。
该研究在透射电镜下观察并比较发现常氧及乏氧外泌体形态基本一致,均呈类圆形的双膜结构,但乏氧外泌体平均粒径值显著大于常氧外泌体的平均粒径值。此外发现乏氧预处理能显著增加细胞上清中外泌体的浓度。PHK67所标记的这两种外泌体均能被内皮细胞吞噬至细胞内(图1)。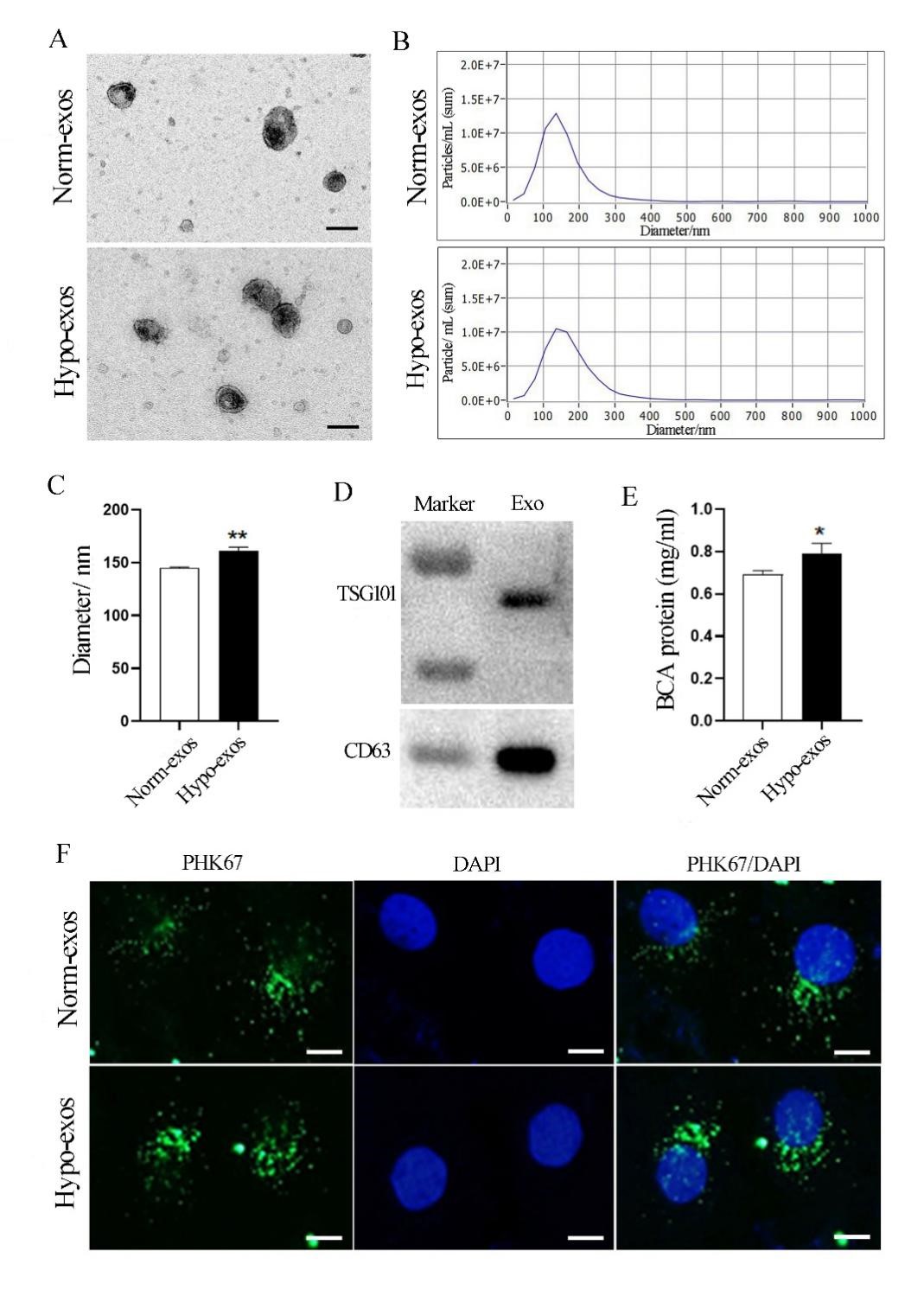
通过CCK-8实验及Ki67免疫荧光染色实验表明,与常氧外泌体相比,乏氧外泌体能显著促进内皮细胞的增殖潜能。细胞划痕实验及Transwell小室实验表明乏氧外泌体能显著促进内皮细胞的迁移能力(图2)。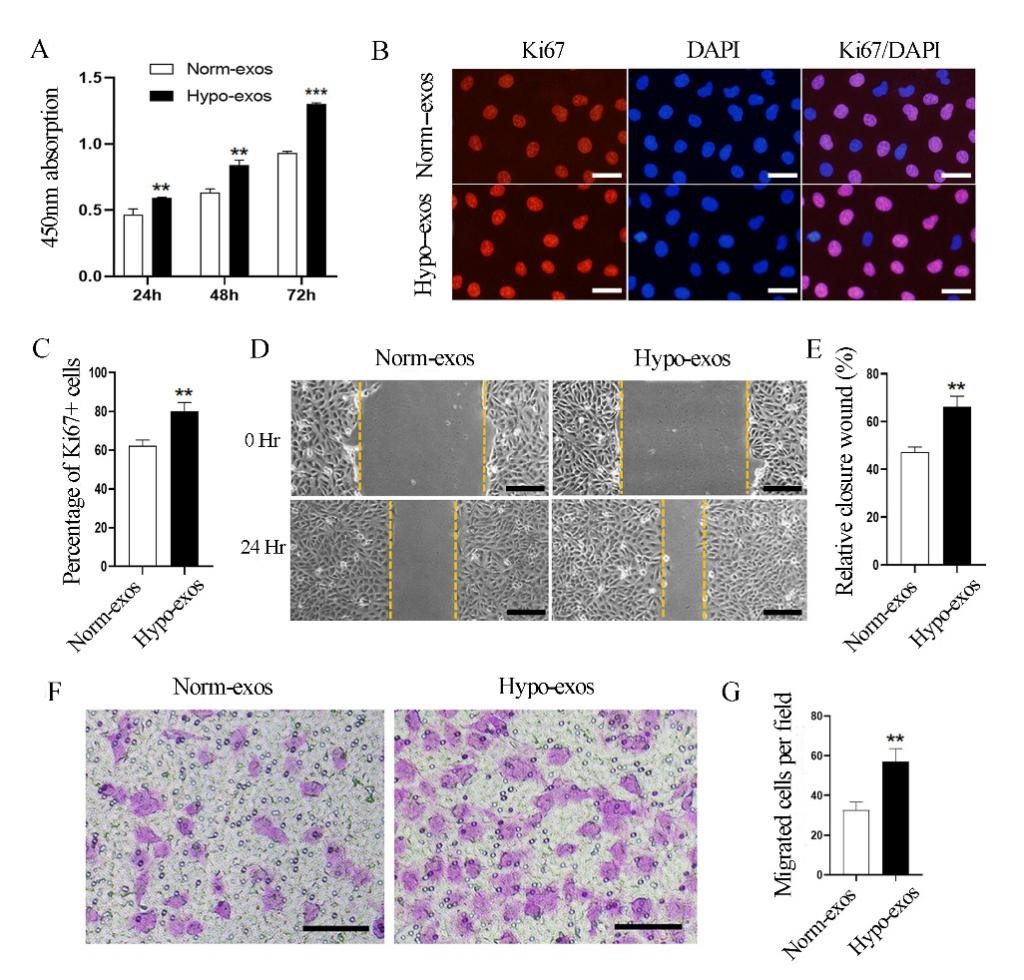
与常氧外泌体相比,乏氧外泌体显著促进内皮细胞的体外成管并正向调控内皮细胞中VEGF、MMP-9及ANGPT1表达(图3)。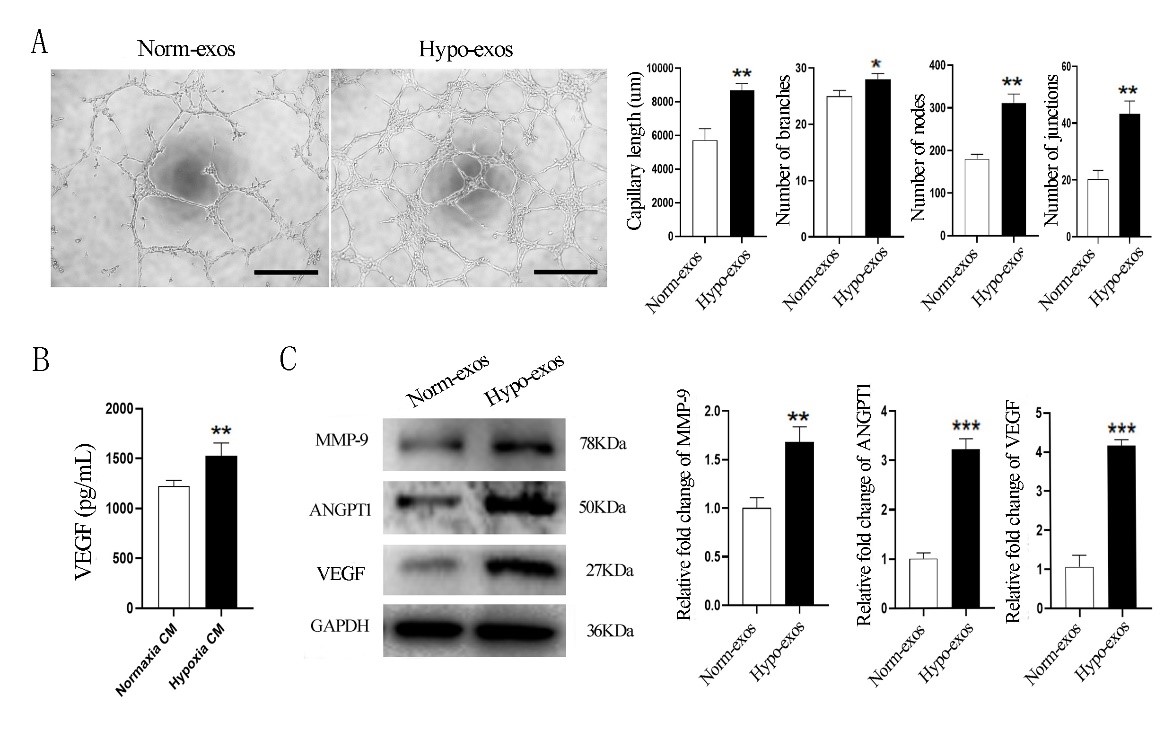
图3
裸鼠皮下基质胶成管实验表明乏氧外泌体组的基质胶栓较常氧外泌体组呈现出更红的外观且乏氧外泌体组的VEGF表达量及CD31阳性细胞所标记微血管的数量显著增加(图4)。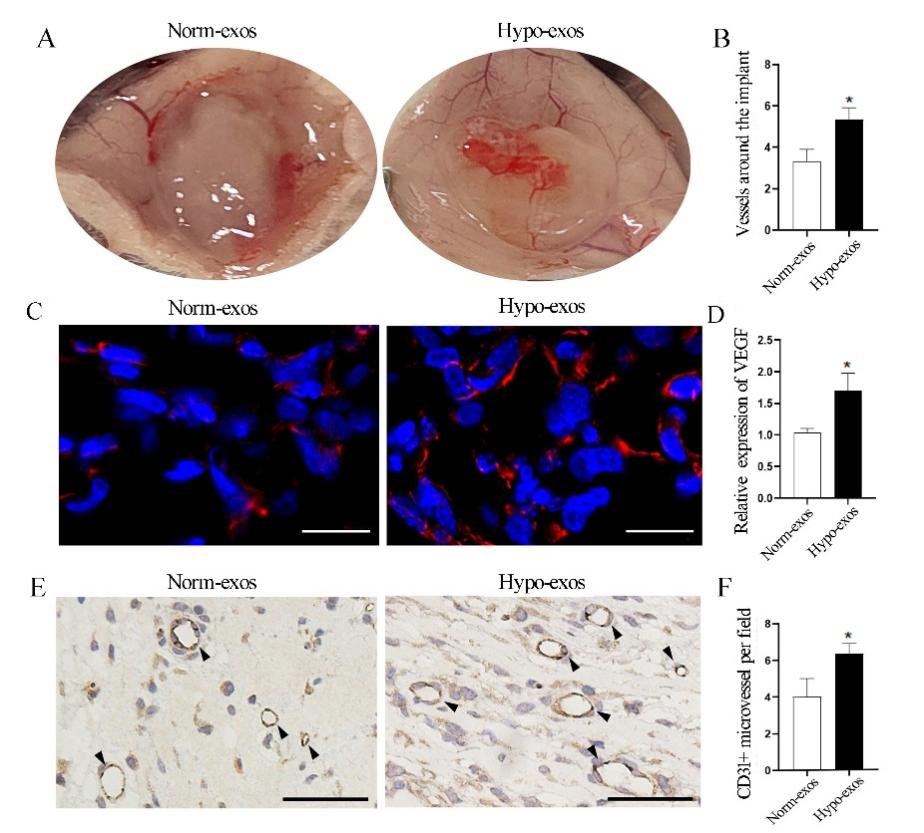
借助外泌体miRNA测序技术,筛选出常氧及乏氧外泌体中的差异miRNAs并通过qRT-PCR实验验证,结果表明乏氧外泌体中富集了更多的let-7f-5p 与miR-210-3p(图5)。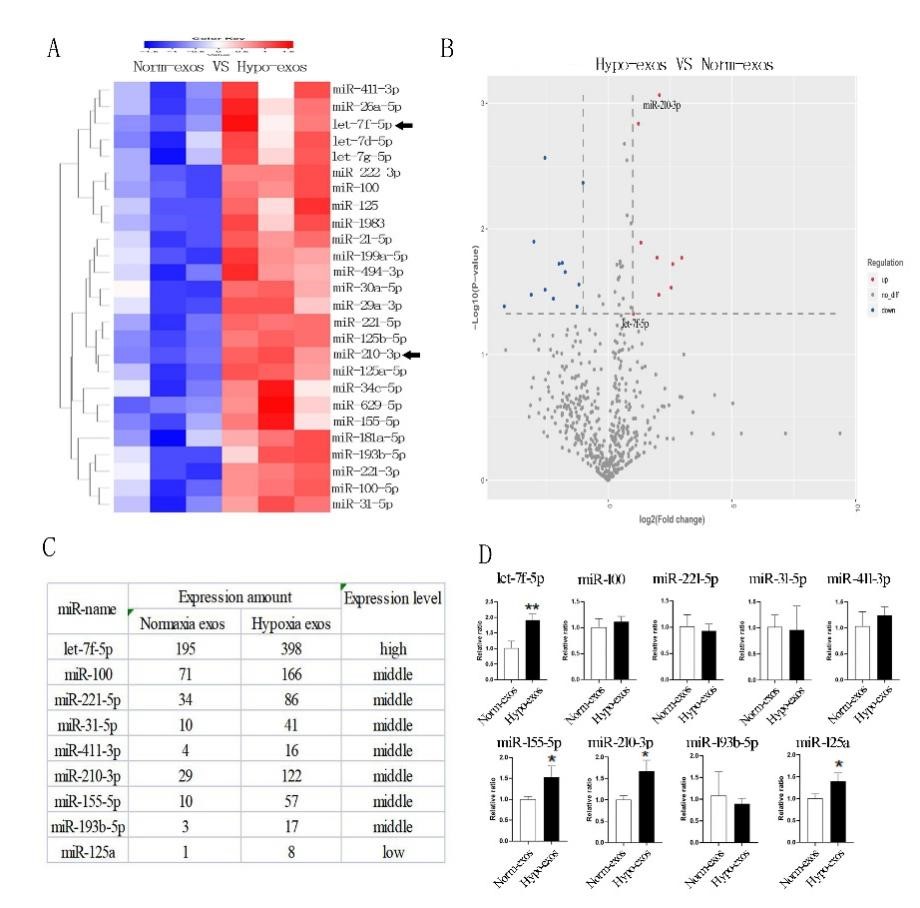
最后通过基质胶体外成管实验、qRT-PCR实验及Western blot实验进行相关分子通路的验证发现氧外泌体通过富集let-7f-5p及miR-210-3p促进血管生成,这与let-7f-5p/AGO1/VEGF及miR-210-3p/EphrinA3信号通路相关(图6)。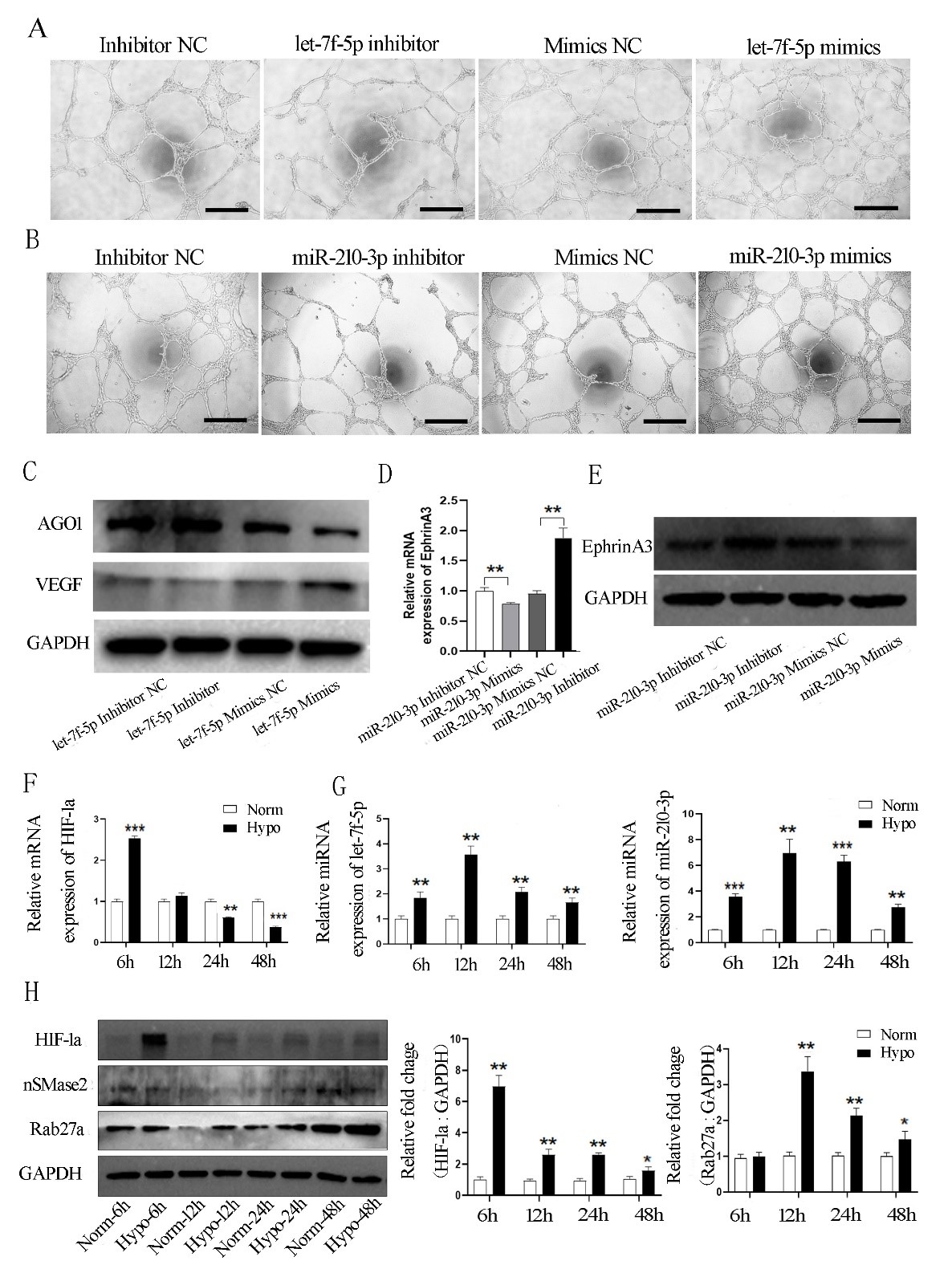
Exosomes derived fromhypoxia-conditioned stem cells of human deciduous exfoliated teeth enhanceangiogenesis via the transfer of let-7f-5p and miR-210-3p. Frontiers in cell and developmetal biology. 2022 Apr 26;10:879877. doi:10.3389/fcell.2022.879877.外泌体资讯网 FRONT CELL DEV BIOL | 山东大学和杭州医学院:缺氧条件下人脱落乳牙牙髓干细胞来源外泌体促进血管生成