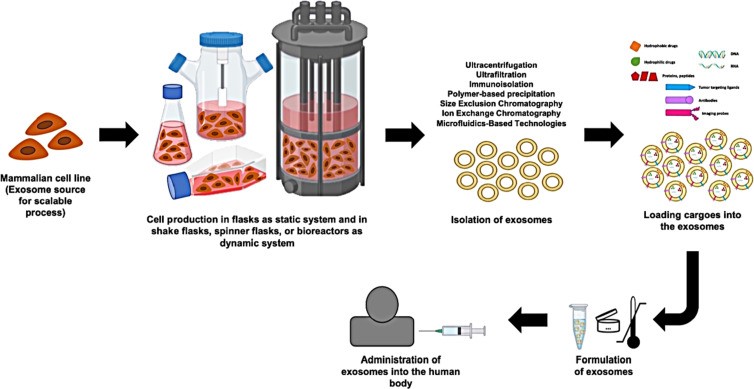
外泌体与脂质体和聚合物纳米颗粒等其他递送系统相比,具有显著优势,但需要开发大规模生产、分离和载药的外泌体方法,提高其效率和治疗潜力。来自土耳其埃格大学的研究人员在J Control Release杂志上发表综述,详细介绍了外泌体在药物递送系统中的应用潜力,对大规模生产外泌体、外泌体分离、外泌体货物装载和受体细胞摄取外泌体的方法进行了综述,并提出当前的挑战和潜在方向。
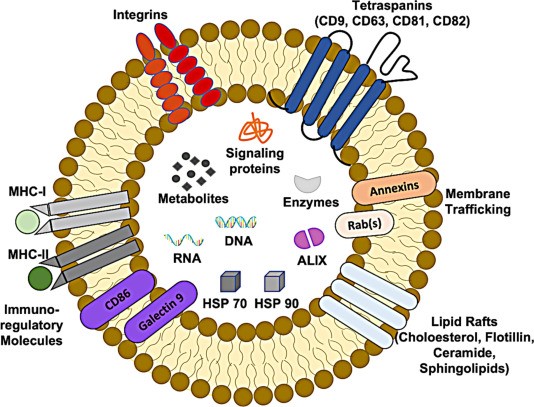
外泌体是纳米囊泡,大小为 20-100 nm,可以从各种细胞中释放出来,例如成纤维细胞、免疫细胞(T 细胞、B 细胞、树突细胞)、脂肪细胞和肿瘤细胞,并存在于各种体液里,如血液、尿液、母乳、羊水和支气管肺泡灌洗液。外泌体与ectosomes、微囊泡、膜囊泡和凋亡小体都属于细胞外囊泡 (EV)。外泌体的内容物也因细胞来源而异,被认为是含有蛋白质、脂质和核酸的囊泡。在其结构中,细胞骨架蛋白(肌动蛋白、微管蛋白、cofilin、moesin)、粘附分子(四次跨膜蛋白CD9、CD37、CD53、CD63、CD81、CD82和整合素)、ESCRT蛋白、转运/结合蛋白(膜联蛋白、Rab家族、GTP酶),还有Alix、TSG101 蛋白和热休克蛋白(HSP70、HSP90),它们充当标记物并参与外泌体生物发生。此外,还发现了诸如鞘磷脂、磷脂酰丝氨酸、胆固醇、flotillin和神经酰胺等脂质。外泌体中的核酸包括mRNA、miRNA和其他非编码RNA。ExoCarta数据库 (http://www.exocarta.org) 于2009 年首次创建,对哺乳动物外泌体中所含的蛋白质、RNA 和脂质以及分离和表征程序进行分类。Vesiclepedia (http://microvesicles.org) 和EVpedia (http://evpedia.info) 是分别与哺乳动物和非哺乳动物中所有类型的EV相关的数据库。
外泌体一词是在1970年代由RoseJohnstone博士发现的,他试图了解从网织红细胞转变为成熟红细胞的生物学过程。随着对这些囊泡具有细胞间通讯、维持身体平衡、信号传递和提供免疫稳态等功能的认识,外泌体在疾病诊断和治疗中的应用研究迅速增加。近年来,已经发表了大量关于外泌体作为药物载体的潜力的研究。Pubmed发表的包含“药物递送中的外泌体”这一短语的论文数量逐年上升。
为了系统地研究 EV 的安全性和有效性并确定其鉴定和纯度,国际细胞外囊泡协会 (ISEV) 于2014年推出了EV分离和表征方法的标准化指南。指南于2018年再次更新。由 ISEV 专家支持的欧洲科学技术合作 (COST) 行动中描述了关于基于EV新疗法的药物分类建议以及根据药物质量要求构建的程序研究。正在进行临床研究,以研究外泌体作为各种疾病早期诊断和治疗手段的安全性和有效性。然而,临床上充分使用的生产、分离和各种装载策略相关的问题尚未完全解决。
图:外泌体载药的一般流程
在这项综述里,研究者认为,外泌体代表了一种令人兴奋的药物转运研究新方法,具有合成脂质体的许多优点,例如在其脂质双层膜中运输疏水性药物和在其水核中运输亲水性药物的能力。因此,外泌体的载药潜力吸引了科学界的兴趣,作为包括癌症和神经系统疾病在内的多种疾病的一种可能的治疗选择。尽管外泌体被认为安全、生物相容性和非免疫原性,但由于它们的内源性来源的、未知的生物活性分子混合物的转移会带来一些风险。需要更多的研究来了解更多关于外泌体成分含量和潜在毒性的信息。
研究者认为,在药物递送中外泌体的效率取决于药物的化学成分、给药途径、靶组织和潜在机制。这些特性将对目前装载效率、细胞吸收、递送途径和可能的不利影响等方面产生重大改变。因此,必须根据限制以及竞争系统(如每个系统的脂质体)的优缺点仔细评估使用载药外泌体的好处。为了使这一突破更接近临床应用,需要进行更全面的体内研究以了解外泌体的效力和毒性。
简而言之,尽管在将外泌体投入实际应用方面存在挑战,但这种内源性囊泡具有巨大的药用价值,可用于开发新的药物输送和治疗方法。