阿尔茨海默病(Alzheimer’s disease, AD)是进行性发展的神经系统退行性疾病,严重影响了老年人的健康与生活质量,至今尚无有效逆转其病理进程的治疗药物。临床数据表明,AD病人血清和脑脊液中aFGF的水平高于无认知障碍受试者,然而,aFGF升高背后的效应鲜有研究。细胞外囊泡(Extracellular vesicles, EVs)是细胞通讯的重要调节者,在多种疾病的诊断和治疗上具有巨大的临床价值。
近日,来自暨南大学生物医药研究院的黄亚东教授和张齐好教授团队在Theranostics杂志上发表题为“Extracellular vesicles derived from astrocyte-treated with haFGF14-154 attenuate Alzheimer phenotype in AD mice”的研究论文(2022 May 9;12(8):3862-3881)。该研究发现酸性成纤维细胞生长因子(Acidic fibroblast growth factor, aFGF)可通过抑制星形胶质细胞EVs中关键调节分子miR-206-3p的表达,进而上调脑源性神经营养因子(BDNF)和突触相关蛋白的表达,减少AD小鼠脑内Aβ的沉积、促进神经元修复以及改善学习记忆能力,有效延缓AD的病理进程。
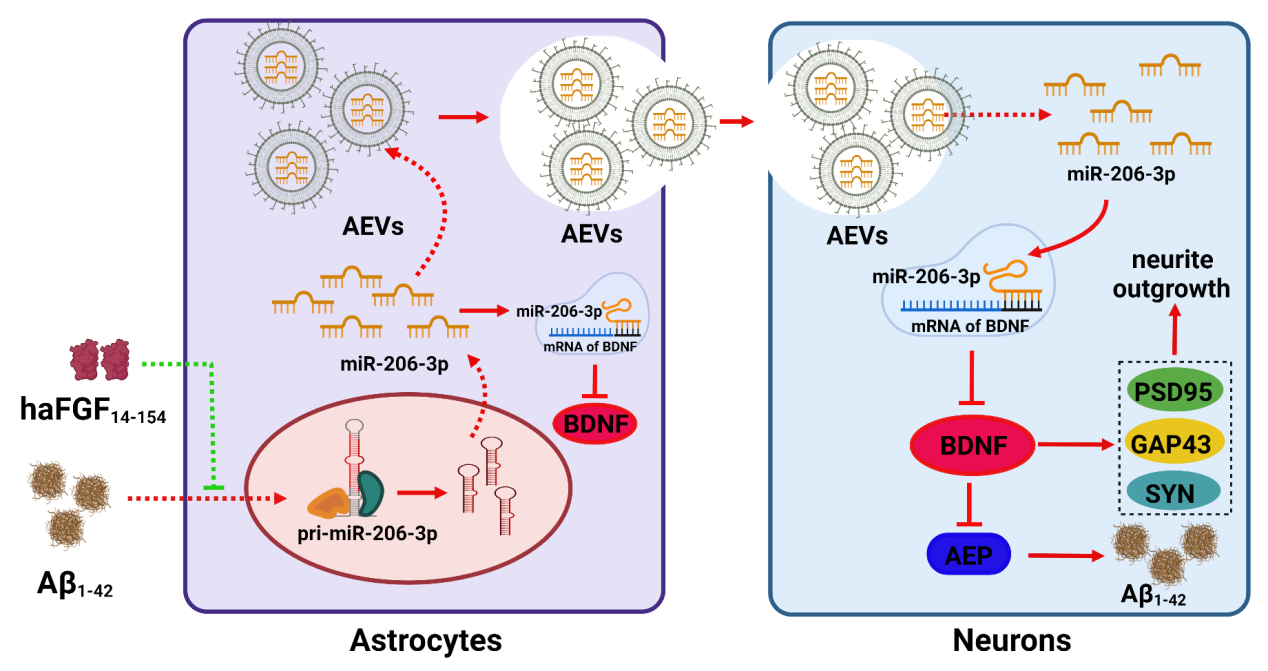
aFGF调控星形胶质细胞分泌EVs治疗AD的示意图
该团队进一步通过对临床AD患者血浆中miR-206-3p的表达进行检测,发现AD患者血浆中miR-206-3p的水平显著高于年龄匹配的正常受试者;且相比于帕金森病和精神分裂症患者,AD患者血浆中miR-206-3p的表达更具有特异性,有望成为AD早期诊断的候选生物标记物。
在之前的研究中,该团队利用脂质体包裹及穿膜肽TAT介导等技术联合鼻腔滴注的方式,建立了无创性脑内局部给药的治疗策略。这项研究再次证实以EV为载体同样可以使药物经鼻腔滴注的方式进入大脑发挥治疗作用,为神经退行性疾病乃至脑部疾病的防治提供新思路。目前,研究团队正在开展基于外泌体的药物载体应用基础研究和aFGF治疗神经退行性疾病新增适应症的临床前研究。
暨南大学为第一通讯单位,暨南大学的博士研究生彭冬为文章第一作者,暨南大学的黄亚东教授和张齐好教授为文章共同通讯作者。该工作受到国家自然科学基金(81871150, 82071634,81973072)、广东省科技计划项目(202103030003)和横向课题(暨南大学&暨源生物产学研平台合作项目2021-2023)的支持。
参考文献:
Extracellular vesicles derived from astrocyte-treated with haFGF14-154 attenuate Alzheimer phenotype in AD mice. Theranostics. 2022; 12 (8): 3862-3881. DOI: 10.7150/thno.70951.
外泌体资讯网 Theranostics|暨南大学黄亚东教授和张齐好教授团队:aFGF调节星形胶质细胞外泌体治疗阿尔茨海默病的新机制