骨关节炎(Osteoarthritis,OA)是一种临床高发的退行性关节疾病;目前尚无有效治疗的药物。基因编辑技术作为非传统治疗手段为OA提供新型的治疗方案。其中CRISPR/Cas9的革命突破为简便而有效的基因编辑开辟了一条全新途径。如何实现CRISPR/Cas9的高效安全递送受到研究者的高度关注。
近年来,外泌体在实现药物靶向递送上具有得天独厚的优势,香港中文大学化学系夏江教授团队和深圳市第二人民医院骨科基础研究团队在深港创新圈项目资助下构建基因工程化外泌体—脂质体,优化基因编辑工靶向递送体系治疗OA取得了新进展,相关研究成果以“Chondrocyte-specific genomic editing enabled by hybrid exosomes for osteoarthritis treatment”为题发表在生物医学一区TOP期刊Theranostics上 (2022 Jun 21;12(11):4866-4878),为利用工程化外泌体—脂质体杂交系统靶向递送基因编辑工具治疗OA提供新的策略。深圳市第二人民医院段莉研究员和香港中文大学夏江教授为本文的共同通讯作者,课题组成员梁宇杰博士为该文第一作者。深圳市第二人民医院课题组成员徐晓和徐丽梅为文章的共同第一作者。该项研究工作得到了国家自然科学基金、深港创新圈项目和香港特别行政区创新科技署粤港科技合作资助计划(TCFS)等相关基金的资助。

CRISPR/Cas9-sgRNA MMP-13可抑制软骨基质分解代谢,然而其缺乏对软骨细胞的靶向识别能力。该研究采用基因工程技术,通过对外泌体膜蛋白LAMP-2B进行改造,使软骨细胞亲和多肽CAP融合LAMP-2B后展示在外泌体膜上,外泌体与脂质体融合形成杂交外泌体并赋予其靶向软骨细胞的能力。改造后的杂交外泌体可靶向递送sgRNA MMP-13进入关节软骨细胞,抑制关节软骨基质分解代谢,实现有效治疗OA。
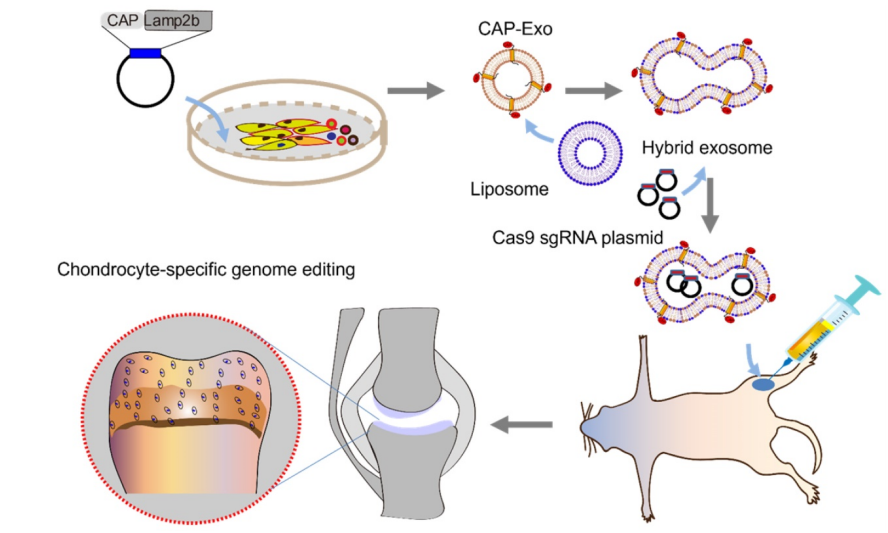
图:杂交外泌体—脂质体靶向递送基因编辑工具治疗骨关节炎示意图基于外泌体—脂质体膜融合的工程化改造实现高效且安全的CRISPR基因编辑治疗,将为基因治疗的临床转化提供新的举措。参考文献:Chondrocyte-specific genomic editing enabled by hybrid exosomes for osteoarthritis treatment. Theranostics, 2022; 12(11):4866-4878.
外泌体资讯网 Theranostics|香港中文大学夏江和深圳市第二人民医院骨科: 构建基因工程外泌体用于靶向递送基因编辑工具治疗骨性关节炎




