人间充质干细胞 (hMSC) 衍生的细胞外囊泡 (EVs) 被认为具有治疗潜力,然而这些EV中相应的治疗成分还仍然是未知的,同时hMSC EV的大规模生产是也是转化应用的主要挑战之一。来自美国佛罗里达州立大学的研究人员发现,hMSC在波动条件下会生长为3D聚集体,源自3D聚集体hMSC的EV分泌量大幅增加,与传统的平面培养相比表现出增强的治疗潜力。相关成果以“Engineering extracellular vesicles by three-dimensional dynamic culture of human mesenchymal stem cells”为题于今年6月18日在细胞外囊泡期刊J Extracell Vesicles杂志上发表。
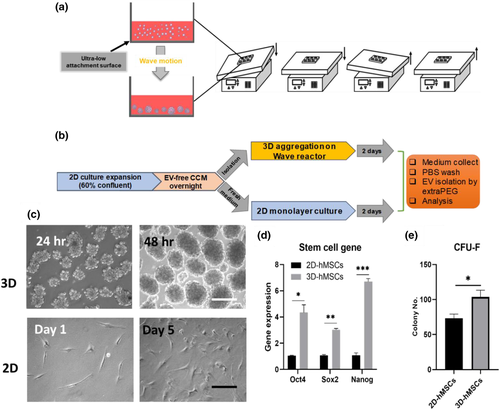
人间充质干质细胞 (hMSC) 近年来成为了干细胞治疗的宠儿,有望用于阿尔茨海默病、心肌病、移植后排异反应、传染病等疾病的治疗。MSC通过其分泌组和旁分泌因子发挥治疗作用,具有多向分化潜能。在MSC分泌物里,细胞外囊泡 (EV) 是近年来被研究最多的治疗物之一。EV 是从细胞释放的小的膜包裹颗粒,直径20-500 nm,能够转移细胞溶质蛋白、脂质、代谢物和遗传物质的膜成分和货物,在细胞间通讯中发挥重要作用。hMSC EV 的内部物质和膜成分可能对治疗神经退行性疾病有治疗益处。据报道,hMSC EVs 还可促进缺血性疾病中的组织再生,并通过减少细胞氧化应激发挥抗衰老作用。临床前研究表明,在自身免疫性脑脊髓炎 (EAE) 模型中,源自hMSCs的EV可减少氧化应激、改善炎症并促进少突胶质细胞形成和髓鞘再生。在临床前缺血性中风研究里中,hMSC EVs 促进了病变部位的抗炎和抗细胞凋亡反应以及血管生成,梗死体积显著减少、运动功能显著改善。在阿尔茨海默病模型中,hMSC EV处理的小鼠具有更好的认知行为和更低的海马Aβ斑块。虽然这些结果证明了hMSC EV在治疗各种神经系统疾病方面的潜力,但在体外培养条件下,亲代细胞转录组与hMSC EV中的蛋白质、microRNA或代谢物的货物谱以及神经再生能力之间的相关性仍然需要研究。不同培养条件下的MSC所具备的治疗应用以及功能会有差别。MSC EV的一些特性与微环境和体外条件相关,比如,在生物反应器中的缺氧或流体动力培养下有所区别。与2D培养相比,3D聚集培养作为一种预处理策略,有望促进具有有益货物特征的hMSC EV生产。与传统2D培养下生成的 EV 相比,HSP90和EpCAM在3D癌症类器官分泌的EV中高表达,并且3D培养下的EV更好地反映了体内外泌体的特征。来自人诱导多能干细胞 (hiPSC) 的3D微球体的EV货物谱,反映了干细胞分化的谱系特异性发育阶段。此外,最近的研究提供了强有力的证据,表明3D聚集培养诱导hMSC的稳态发生剧烈变化,其特征是糖酵解增强、自噬激活、抗衰老特性、具有体外hMSC 原始表型。特别是,与2D培养相比,3D hMSC聚集细胞群体的分泌物中表现出与免疫抑制和抗细胞凋亡相关的细胞因子的表达增强。虽然hMSCs的3D聚集方法研究火热,但3D hMSC 聚集体分泌的 EV 的特性尚未得到很好的研究。由于EV具有亲代细胞的大部分细胞特征,因此3D hMSC 聚集体的 EV 可能表现出更好的治疗益处。在这项研究中,研究人员比较了源自3D聚集体 (3D-hMSC-EVs) 和 2D平面培养 (2D-hMSC-EVs) 下的两种hMSC EVs的特性。对于3D培养,研究人员将骨髓来源的 hMSC 放置于小型动态波动生物反应器中进行自发聚集。随后,hMSC-EV被分离,并表征其产量、大小分布、EV标记物、蛋白质货物和miRNA货物,检测了对具有复制性衰老的成体干细胞的抗衰老作用、对巨噬细胞极化的免疫调节作用、体外伤口愈合模型实验等。为了揭示可能的相关分子途径,研究人员进行了mRNA测序、EV蛋白货物的蛋白质组学分析、以及2D和3D hMSCs 的转录组。研究结果表明,3D hMSC 聚集体促进了转运依赖性和非依赖性途径所需的内体分选复合物的激活。mRNA测序揭示了3D hMSC 聚集体的全局转录组改变。与 2D-hMSC-EVs 相比,3D-hMSC-EVs的数量显著增加,且尺寸更小,miR-21和miR-22表达更高,细胞因子和抗炎因子等蛋白质货物上调。在功能上,3D-hMSC-EVs 使衰老干细胞恢复活力并表现出增强的免疫调节潜力。本研究为从具有增强治疗潜力的hMSCs大规模生产高质量 EV 提供了新希望。参考文献:Engineering extracellular vesicles by three-dimensional dynamic culture of human mesenchymal stem cells. J Extracell Vesicles. 2022;11(6):e12235.




