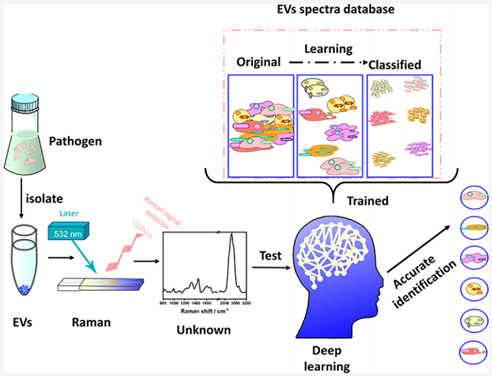
病原微生物感染,特别是具有抗生素抗性的病原菌感染,被世界卫生组织列为全球健康的重大威胁。病原微生物来源的细胞外囊泡(EVs)被视为引发感染事件的 “远程武器”。EVs是由细胞分泌的尺寸为40-200 nm的膜囊泡。从致病菌释放的EVs携带来自致病菌的内含物,如蛋白质、核酸、碳水化合物、脂质和毒力因子等致病因子。特别是EVs尺寸小,可以穿过病原菌难以穿越的血脑和胎盘屏障,将致病因子送至宿主细胞,激活宿主免疫系统,并可能加速细菌感染过程。因此,快速准确识别不同微生物尤其是病原菌来源的EVs,对于感染的早期诊断、及时干预和治疗非常重要。近日,中国科学院城市环境研究所崔丽研究员与厦门大学化学化工学院任斌教授团队合作,开发了基于拉曼光谱结合深度学习的方法,实现了对不同病原菌来源细胞外囊泡的快速精准识别和生成机制研究。相关研究成果以“Deep Learning-Enabled Raman Spectroscopic Identification of Pathogen-Derived Extracellular Vesicles and the Biogenesis Process”为题发表在国际期刊 Analytical Chemistry上 (doi: 10.1021/acs.analchem.2c02226)。崔丽研究员团队长期致力于环境微生物单细胞前沿分析技术的开发研究,近年来针对环境耐药菌和有益功能菌,在发展单细胞拉曼光谱联用稳定同位素标记、单细胞分选和基因测序等方面,取得系列成果,引起国际同行关注,并将相关技术拓展应用至病原菌来源的细胞外囊泡领域。任斌教授团队长期致力于发展高灵敏度和高时空分辨的光谱仪器方法,近年利用机器学习实现信号去噪,成像超分辨重构和光谱分类等方面取得系列进展。该团队针对6种典型临床病原菌及其分泌的EVs,采集三个不同批次样品的拉曼光谱,建立了包含4335条光谱数据的拉曼数据库,并开发了基于注意力机制的神经网络(aNN)深度学习算法鉴别不同EVs的拉曼光谱。该算法在革兰氏阴性/阳性水平、菌种水平、抗生素耐药和敏感菌株水平,以及相同菌株不同生理状态水平下,均能实现对EVs的准确鉴别,准确度分别达到96%以上(革兰氏阴/阳和菌种),93%以上(菌株)和87%以上(生理状态),显著高于其它机器学习和深度学习算法。进一步发展了积分梯度法算法(IG),挖掘拉曼光谱所包含的丰富生物化学信息,实现了不同来源EVs拉曼标志峰的可视化。通过比较EVs及其病原菌的拉曼光谱指纹特征,对EVs形成过程中携带内含物的化学性质(如外膜脂质的变化)等方面有了新的理解。未来可发展对纳米单颗粒进行分析的拉曼平台和算法,实现血液、尿液和痰等临床样本中混合EVs的直接检测和识别,这对早期诊断细菌感染源、及时指导治疗和解析EV引发的感染机制等具有重要意义。该研究得到国家自然科学基金优秀青年基金(21922608),面上项目(22176186),中科院从0到1原始创新项目(ZDBS-LY-DQC027)等项目的资助。Deep Learning-Enabled Raman Spectroscopic Identification of Pathogen-Derived Extracellular Vesicles and the Biogenesis Process, Anal Chem. 2022 Aug 27. doi: 10.1021/acs.analchem.2c02226.外泌体资讯网 Anal Chem |中科院城市环境研究所崔丽与厦门大学化学化工学院任斌:拉曼光谱结合深度学习快速准确识别病原菌来源的细胞外囊泡