虾青素是一种主要存在于海洋藻类虾类及酵母中的叶黄素类胡萝卜素的生物活性物质,具有广泛的生物活性如抗炎、抗氧化、抗肥胖及免疫调节活性。其已经广泛的应用于食品功能物质中,为食品提供良好的生物活性功能。但由于其自身结构中存在大量的不饱和键,因此其对光,热,酸碱性的改变极其敏感,且虾青素主要以酯的形式存在,导致水溶性差,极大降低虾青素的生物利用度。为了提高口服食品功能物质的健康功效,研究人员设计了多种载体,如脂质体、树枝状聚合物、胶束、聚合物偶联物、聚合物纳米颗粒等来对营养物质进行递送。通常,这些候选载体是通过复杂设计、合成和构建过程来实现其复杂功能,并通过优化其理化性质,从而使其可用于功能物质递送和治疗诊断。然而这些载体面临许多重要问题,比如复杂的合成过程带来的技术挑战、高成本和低效率。此外,这些人工合成的物质在临床应用时还要面临低生物降解性、不良稳定性、潜在毒性等严重限制。因此,开发一种简便、通用,且生物相容性好的递送策略非常有必要。近日,大连工业大学食品交叉学院谭明乾教授和食品学院苏文涛副教授课题组在农林科学SCI一区Top 杂志Journal of agriculture and food chemistry上发表题为“Engineering Milk-Derived Exosome for Enhancing Cellular Astaxanthin Delivery”的文章(doi: 10.1021/acs.jafc.2c03683),该研究将牛乳源外泌体作为虾青素的活性物质载体,构建了炎症部位靶向的活性物质递送系统,表现出优异的巨噬细胞靶向能力和抗炎功效。大连工业大学食品学院苏文涛副教授为本文的通讯作者,硕士研究生崔维娜为本文的第一作者。
含有磷脂双分子层、蛋白质和核酸混合物的外泌体,在细胞间通讯和分子物质在细胞和组织间的转运中起着关键的生理作用。哺乳动物来源的外泌体具有作为各种药物(特别是核酸)载体的潜力,因为相比目前使用的各种合成聚合物,它们的天然成分可能提供优异的耐受性。大多数来源的哺乳动物外泌体不适合或不具有用作口服药物载体的可行性,这是因为它们在通过胃和小肠恶劣生理条件下缺乏稳定性。然而,乳源外泌体已经过自然特殊进化,可以完成负责生物分子口服运输的任务。乳源外泌体是进化上保守的独特微泡类别,其在穿过胃和胃肠道途中保持其内含的核酸和蛋白质的完整性,它们可以在局部发挥作用或被运送到循环系统中。此外,乳源外泌体似乎比其他天然存在的外泌体更稳定,其在酸性条件下以及在其它类型外泌体通常不稳定的其他恶劣条件下表现出稳定性。基于该课题组前期细胞外囊泡的研究基础(Trends Anal. Chem., 2019;Biomicrofluidics, 2019; Diagnostics, 2021),依托于乳源外泌体独特属性,该文章在牛乳源外泌体表面修饰具有靶向炎症细胞表面CD44受体能力的透明质酸,提高虾青素在细胞中的富集,探究引入功能化的外泌体作为载体能否更有效地发挥虾青素的抗炎、抗氧化的生物活性。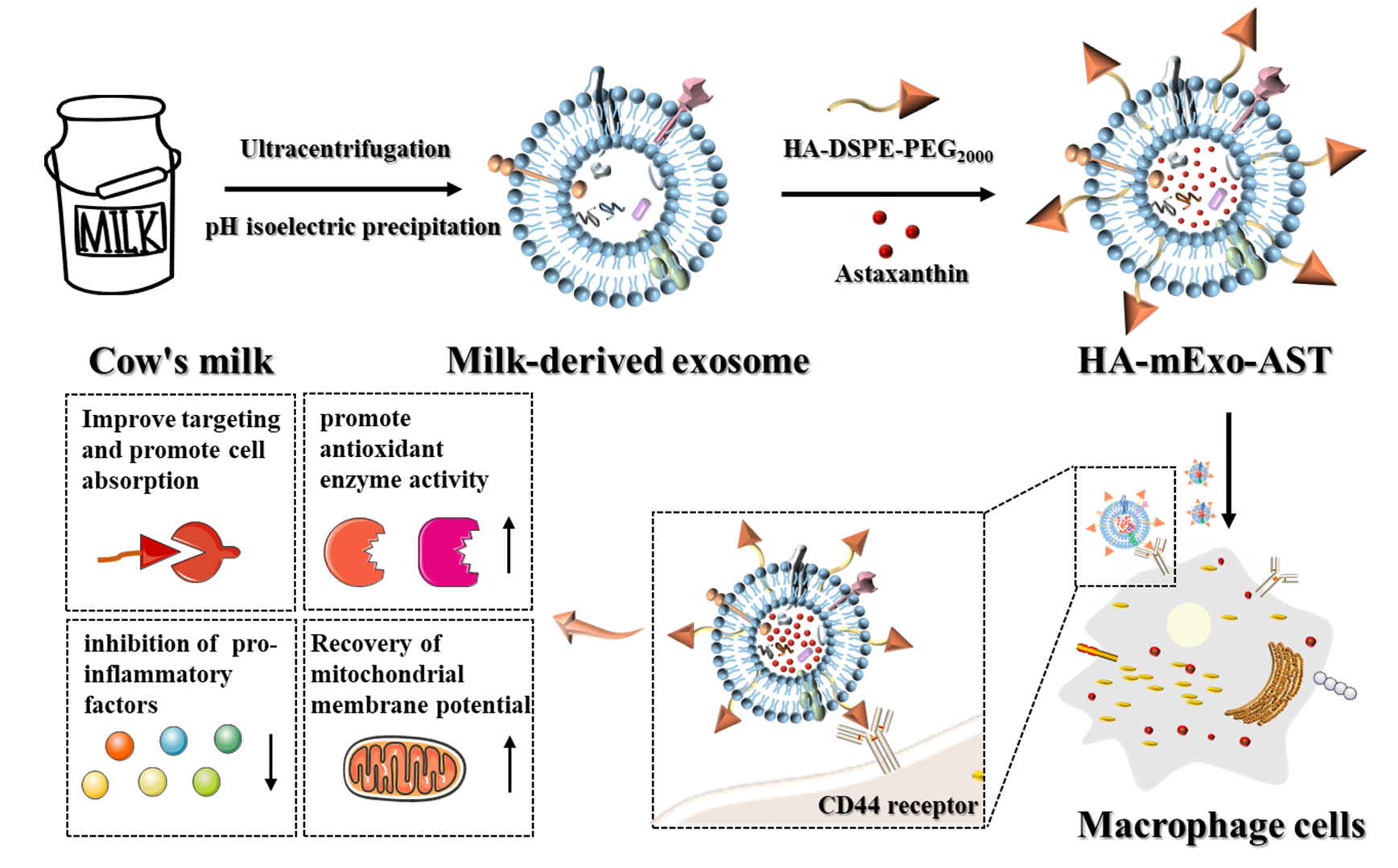
通过细胞摄取及竞争性抑制试验发现:透明质酸靶向的牛乳外泌体具有更好的靶向细胞能力,富集作用更为显著。进一步利用脂多糖诱导的炎症巨噬细胞作为研究模型,研究富集虾青素生物活性的发挥:靶向功能化的外泌体能够有效在细胞部位富集虾青素,对细胞内的氧化应激所引起的细胞线粒体膜电位的降低和细胞内氧化应激所产生的酶变化及活性氧产生具有明显的缓解作用。该研究中建立的靶向递送体系为生物活性物质的递送提供了新策略。Engineering Milk-Derived Exosome for Enhancing Cellular Astaxanthin Delivery. J. Agric. Food Chem. doi: 10.1021/acs.jafc.2c03683.外泌体资讯网 J AGR FOOD CHEM|大连工业大学食品交叉学院谭明乾和食品学院苏文涛团队:工程化牛乳外泌体口服制剂增强虾青素的抗炎能力






