恶性肿瘤是全球范围内首屈一指的公共卫生问题,给人类健康构成了持续性挑战。随着肿瘤诊疗技术的发展,患者生存期明显延长,一些肿瘤已逐渐变成了一种“慢性病”。然而,随之而来的心血管疾病风险却明显增加,主要来自于肿瘤药物的副作用。研究表明合并心血管疾病的肿瘤患者全因死亡风险较不合并者高3.78倍,而且8.8%的长期存活肿瘤患者死于心血管疾病。因此,如何降低癌症患者药物治疗过程中的心脏毒性,已成为提高癌症患者的生存期和生存质量的关键问题,同时也是新兴的肿瘤心脏病学科的重点研究领域。
近日,南方医科大学附属东莞医院李振华研究员课题组在缓解肿瘤化疗诱导的心肌毒性的研究取得新进展:DNA工程化的外泌体抑制化疗药物阿霉素进入细胞核,从而缓解阿霉素诱导的心肌损伤。相关研究成果以“Decoy Exosomes Offer Protection Against Chemotherapy-Induced Toxicity”为题,发表在国际权威学术期刊Advanced Science上(10.1002/advs.202203505)。该工作延续了李振华研究员去年发表的利用肺球状细胞来源的纳米诱饵作为病毒的中和药物的工作(Nature Nanotechnology, 2021, 16, 942-951)。
在这项工作中,该团队利用间充质干细胞外泌体同时作为组织修复和递送载体,结合富含“G-C”的DNA纳米结构,构成了诱饵外泌体。在此基础上,通过在DNA纳米结构修饰心肌靶向肽,增加诱饵外泌体在心脏组织的富集。诱饵外泌体上富含“G-C”的DNA纳米结构能够高效结合阿霉素并抑制其进入细胞核,有效缓解阿霉素诱导的心肌细胞凋亡,为心脏解毒。此外,间充质干细胞的外泌体也显示出诱导巨噬细胞向M2表型极化的作用,进而发挥抗炎作用,促进受损心脏组织修复。
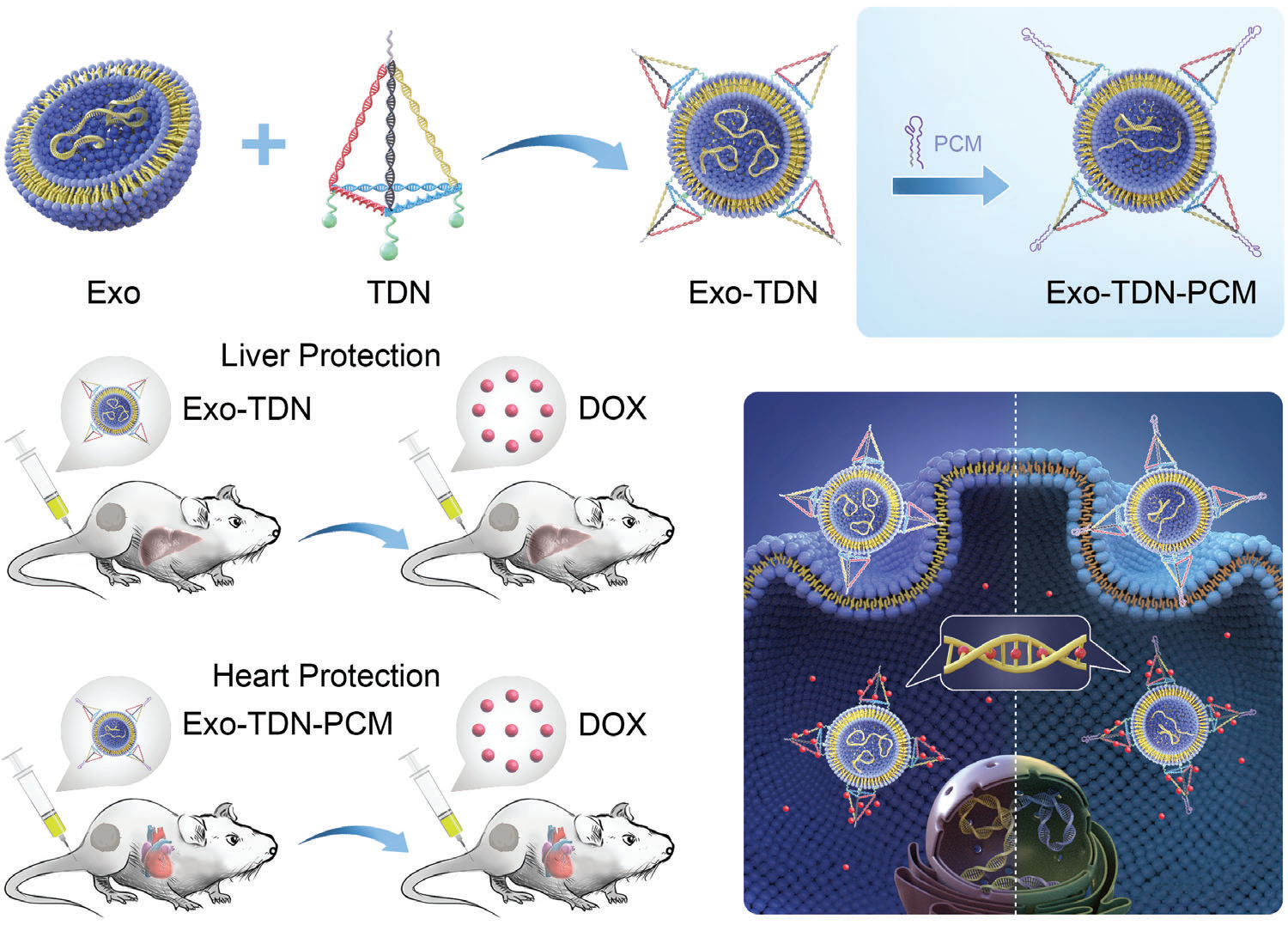
研究结果表明,当心肌细胞摄取诱饵外泌体后,四面体DNA能够捕获阿霉素并抑制阿霉素进入细胞核,从而显著增加了心肌细胞的存活率。此外,对诱饵外泌体处理后的巨噬细胞表型进行了鉴定,结果显示,诱饵外泌体能够有效促进巨噬细胞向M2表型极化。在此基础上,建立“阿霉素治疗乳腺癌”模型,证明诱饵外泌体提供针对化疗诱导的心脏毒性的保护作用。结果显示,诱饵外泌体能够有效的缓解化疗过程中阿霉素诱导的小鼠心肌损伤。重要的是,由于诱饵外泌体主要分布在小鼠的肝脏和心脏组织,因此诱饵外泌体并不影响阿霉素的抗肿瘤效果。
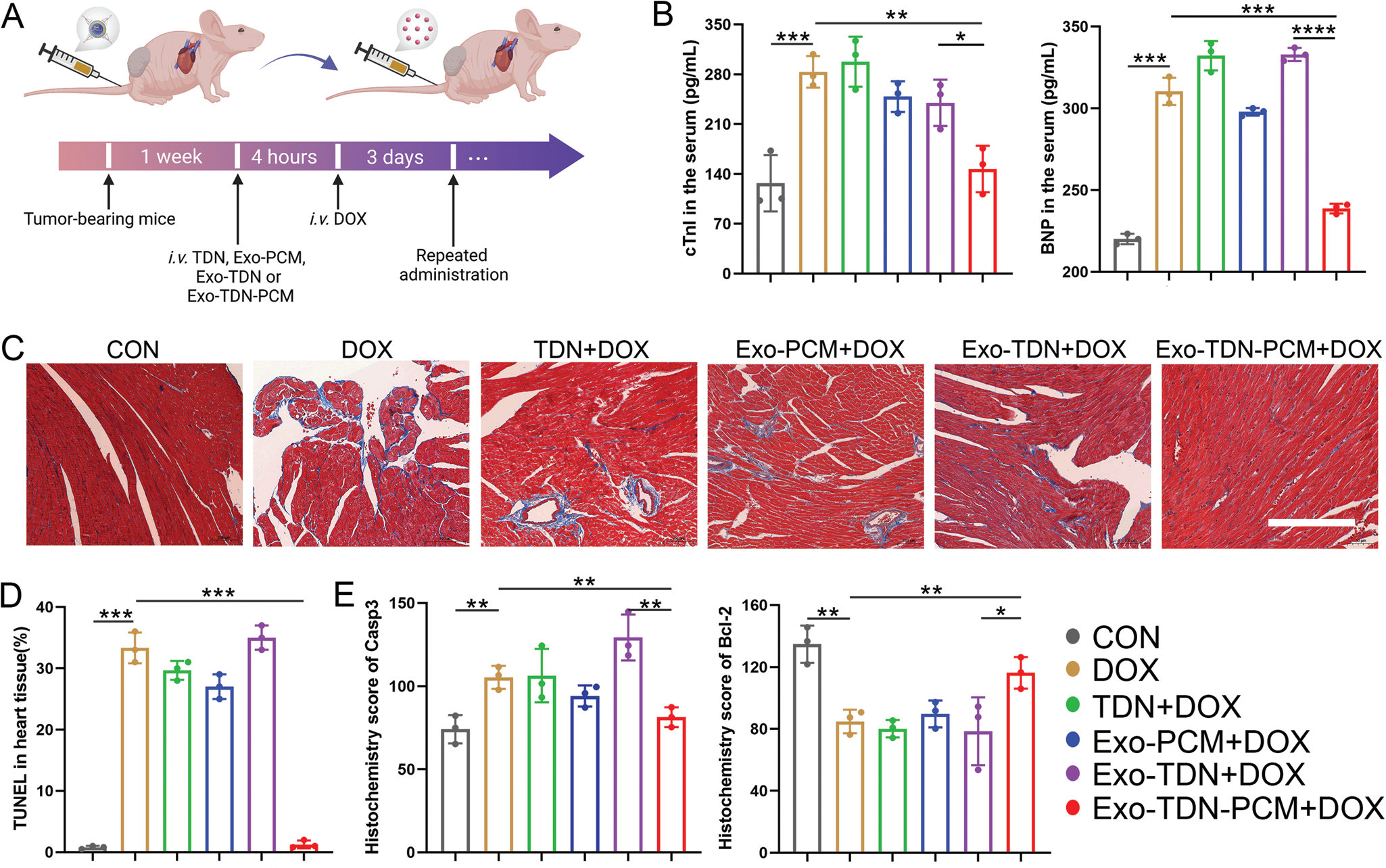
该项研究立足解决肿瘤治疗引起的严重心脏毒副作用问题,具有重要的研究意义。同时,拓展了工程化外泌体的应用,促进肿瘤心脏病学这一新兴学科的发展。附属东莞医院李振华研究员、河北大学张金超教授,以及北卡州立大学程柯教授为本文的共同通讯作者。河北大学博士研究生樊淼、硕士研究生李航,以及郑州大学第一附属医院沈德良教授为本文共同第一作者。该研究得到了国家自然科学基金等基金的资助。参考文献:1. Cell-mimicking nanodecoys neutralize SARS-CoV-2 and mitigate lung injury in a non-human primate model of COVID-19. Nat Nanotechnol. 2021, 16, 942-951. doi: 10.1038/s41565-021-00923-2.2. Decoy Exosomes Offer Protection Against Chemotherapy-Induced Toxicity. Adv Sci (Weinh). 2022, 2203505. doi: 10.1002/advs.202203505.
外泌体资讯网 Advanced Science | 南方医科大学附属东莞医院李振华团队:外泌体诱饵解决肿瘤化疗引起的心肌毒性





