在癌症免疫治疗中,理想的疫苗应具有肿瘤特异性抗原,以有效激活抗原呈递细胞。迄今为止,包括重组蛋白、合成肽、全肿瘤裂解物和核酸在内的各种抗原已被开发并用于肿瘤疫苗的设计。然而,这些抗原大多免疫原性较低,难以达到预期的效果。肿瘤特异性抗原具有肿瘤特有的突变基因、抗原表位及特异性蛋白,因此具有更强的免疫原性。以疫苗为基础的癌症治疗的另一个关键步骤是有效的抗原呈递。由于肿瘤相关巨噬细胞、髓源性抑制细胞等免疫抑制细胞的存在,肿瘤微环境具有高度的免疫抑制状态。免疫抑制微环境严重制约了抗原呈递作用,导致肿瘤疫苗效果不佳。因此,具有改善免疫抑制的特异性肿瘤疫苗有望提高癌症免疫治疗效果。
近日,河北大学刘会芳和张金超教授与南方医科大学附属东莞医院李振华研究员合作,构建了负载免疫佐剂CpG的凋亡小体疫苗。相关成果以“Exosome Transportation-mediated Immunosuppression Relief through Cascade Amplification for Enhanced Apoptotic Body Vaccination”为题发表在Acta Biomaterialia上(10.1016/j.actbio.2022.09.014)。
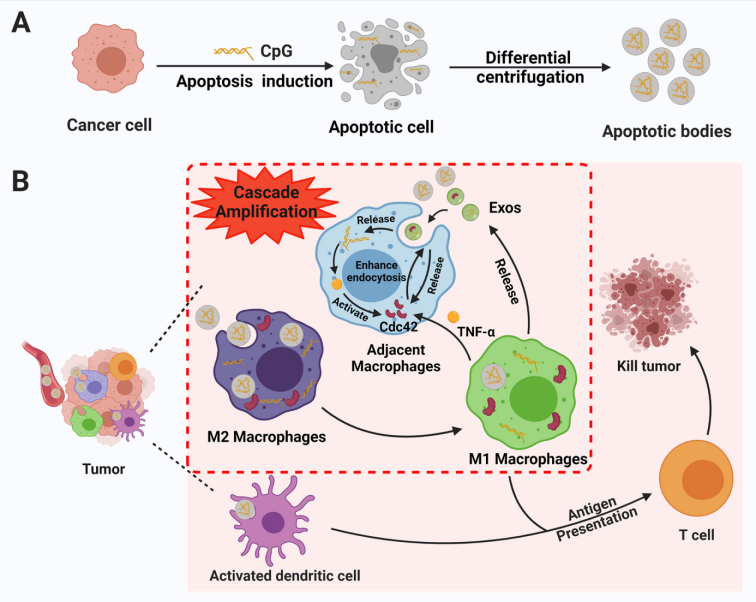
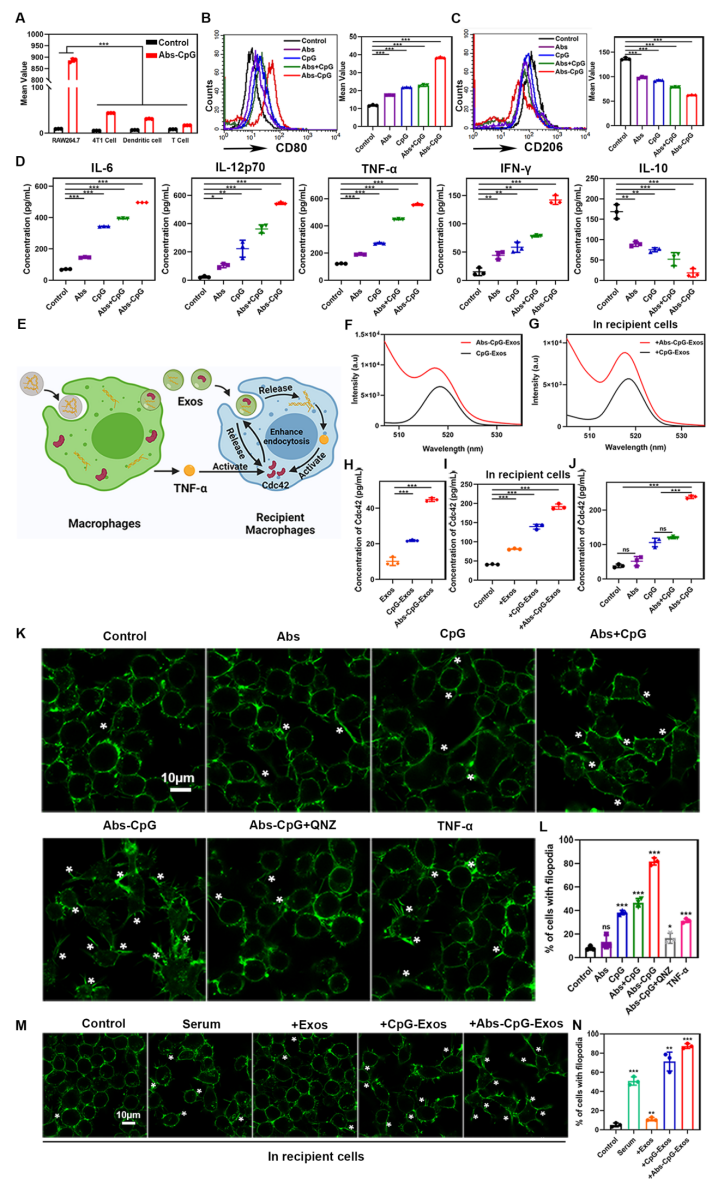
在此项工作中,来源于癌细胞的凋亡小体可以作为肿瘤特异性抗原。凋亡小体上的磷脂酰丝氨酸作为“吃我”信号,使其被巨噬细胞有效内化。免疫佐剂CpG可使免疫抑制的M2型巨噬细胞极化为抗肿瘤的M1型,并显著增加TNF-α等抗肿瘤细胞因子的水平。此外,更加有趣的是,CpG刺激的巨噬细胞外泌体可将Cdc42和CpG转移到邻近的巨噬细胞,通过TNF-α激活Cdc42,从而产生级联放大的正反馈作用,提高邻近巨噬细胞的吞噬能力。
研究结果表明,凋亡小体疫苗能够高度选择性的被巨噬细胞摄取,并通过释放外泌体产生级联放大免疫调节作用,将肿瘤微环境的巨噬细胞从M2型极化为M1型,改善免疫抑制微环境,从而增强巨噬细胞的吞噬能力和抗原呈递能力并释放大量抗肿瘤细胞因子。此外,凋亡小体疫苗能够有效的激活树突细胞、T细胞和NK细胞,引起强烈的免疫反应,显著抑制荷瘤小鼠肿瘤的生长、复发和转移。
该凋亡小体疫苗是合作团队继前期发展的树突状细胞外囊泡疫苗(Biomaterials, 2022, 282, 121424)和巨噬细胞外囊泡疫苗(iScience, 2022, 25, 103639)的又一新型工程化细胞外囊泡疫苗。河北大学硕士研究生赵高倩为本文第一作者,南方医科大学附属东莞医院李振华研究员以及河北大学张金超教授/刘会芳教授为本文的共同通讯作者。该研究得到了国家自然科学基金等基金的资助。
参考文献:
1. Exosome Transportation-mediated Immunosuppression Relief through Cascade Amplification for Enhanced Apoptotic Body Vaccination. Acta Biomaterialia, 2022. DOI: 10.1016/j.actbio.2022.09.014.2. A CAR T-inspiring platform based on antibody-engineered exosomes from antigen-feeding dendritic cells for precise solid tumor therapy,Biomaterials, 2022, 282, 121424.3. Therapeutic exosomal vaccine for enhanced cancer immunotherapy by mediating tumor microenvironment. iScience2022, 25, 103639.
外泌体资讯网 Acta Biomaterialia |南方医科大学李振华/河北大学张金超、刘会芳:外泌体缓解免疫抑制并增强凋亡小体疫苗作用