外泌体在临近和远隔的细胞间通讯中发挥重要作用,参与机体内环境稳态的维持等生理过程和几乎所有的病理过程。
近日,香港中文大学(深圳)医学院杜鹃教授团队在Oxid Med Cell Longev 发表综述“Crosstalk between Oxidative stress and Exosomes”文章(022 Aug 30;2022:3553617),阐述了细胞内活性氧自由基(ROS)调节外泌体形成与释放的多种机制,以及不同类型细胞外泌体对氧化应激的影响。
研究表明低浓度的ROS可以通过抑制mTOR以及溶酶体钙离子通道TRPML1等抑制细胞内多泡体(MVBs)与溶酶体的融合,增加外泌体生成与分泌。但高浓度的ROS则激活自噬,促使MVBs与自噬体融合并降解,减少外泌体的分泌(图1)。
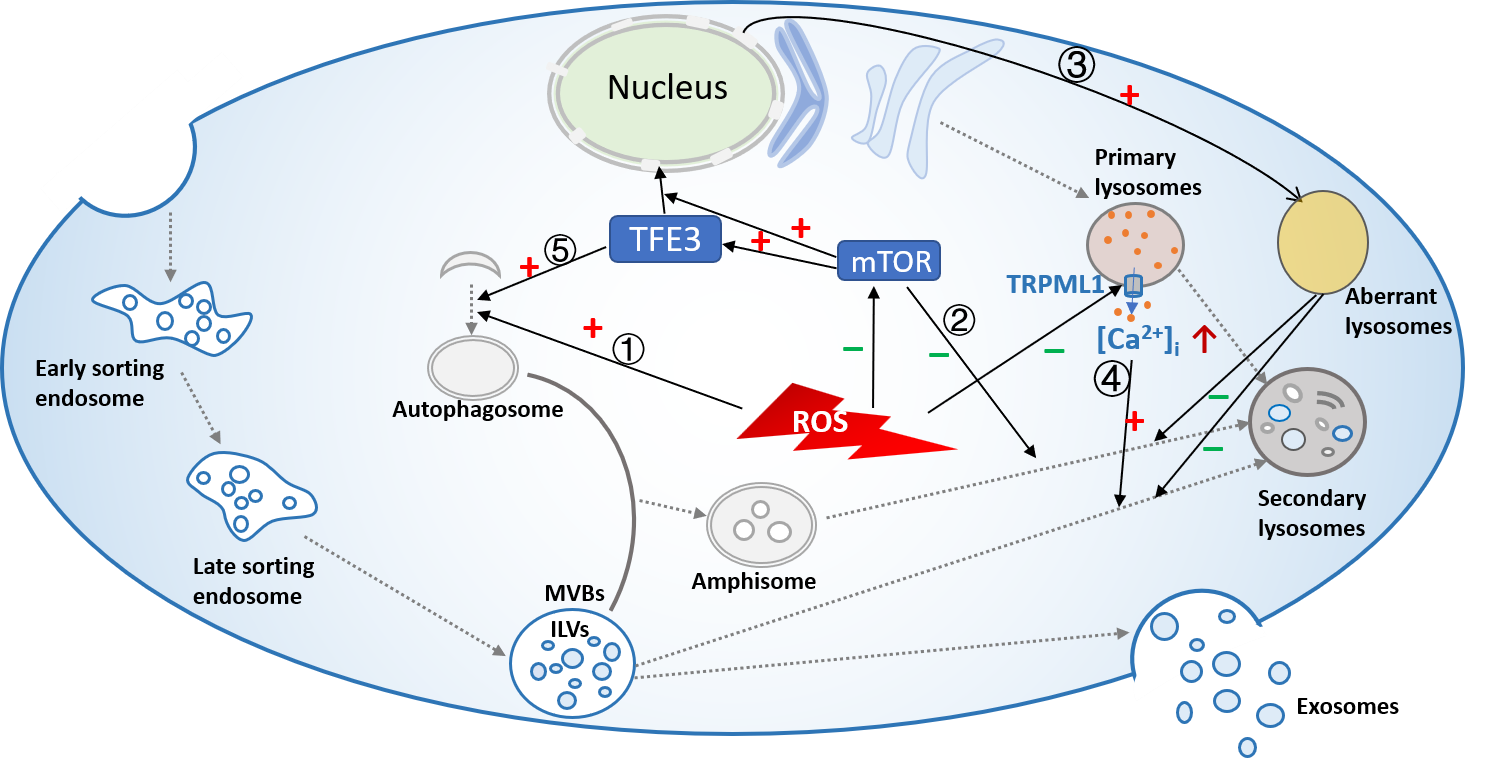
图1. 不同水平ROS通过不同通路影响外泌体分泌量间充质干细胞、脂肪干细胞等具有抗氧化应激能力,却因容易引起患者严重的免疫反应而应用受限,但这些细胞分泌的外泌体具有和来源细胞同样的抗氧化应激能力,且不易引起患者严重的免疫反应,具有重要的临床应用价值。这些细胞外泌体将其携带的各类抗氧化酶mRNA、miRNA、circRNA递送到受体细胞,这些信号分子通过不同的信号通路降低受体细胞内氧化应激水平(图2)。
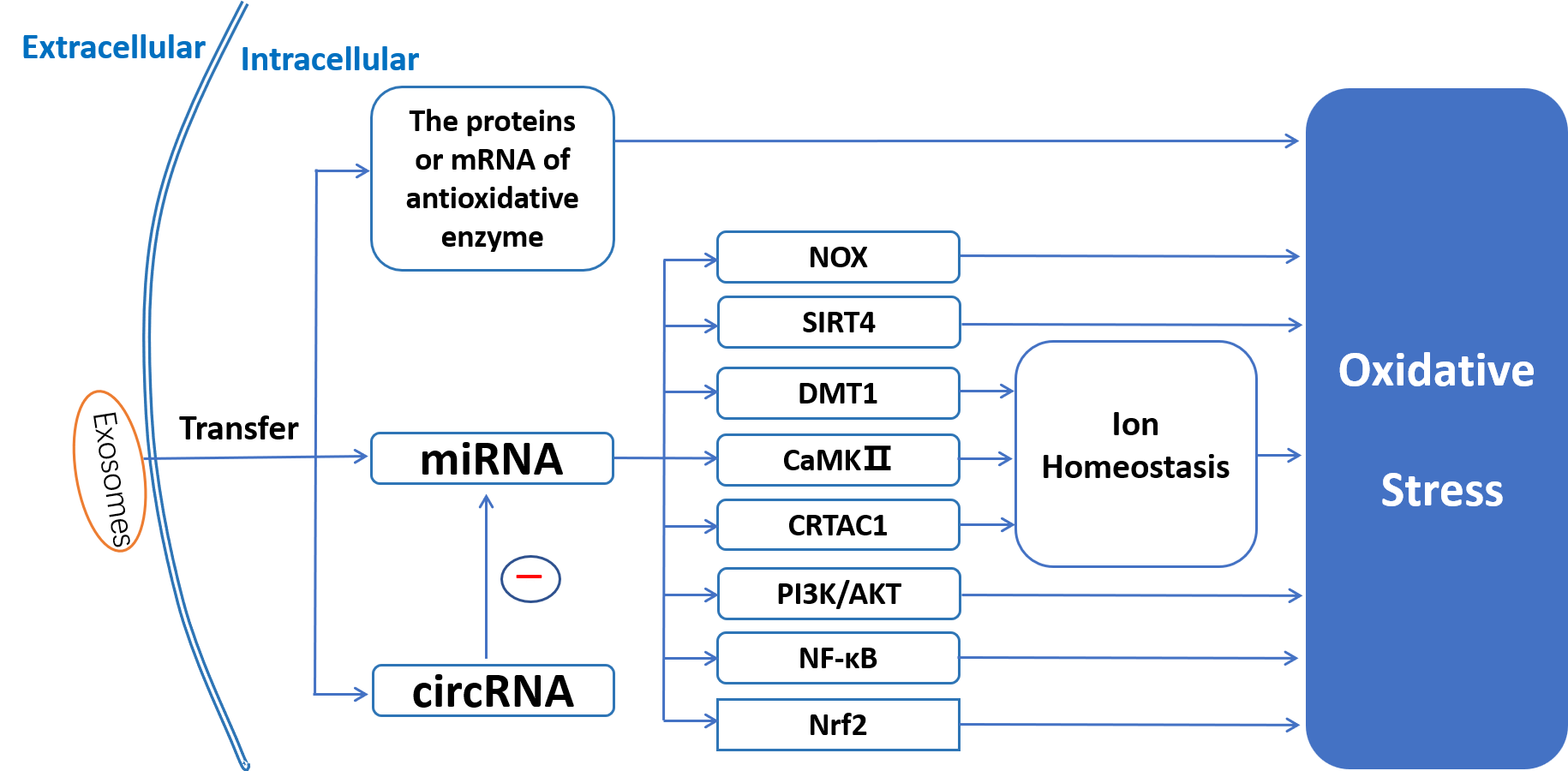
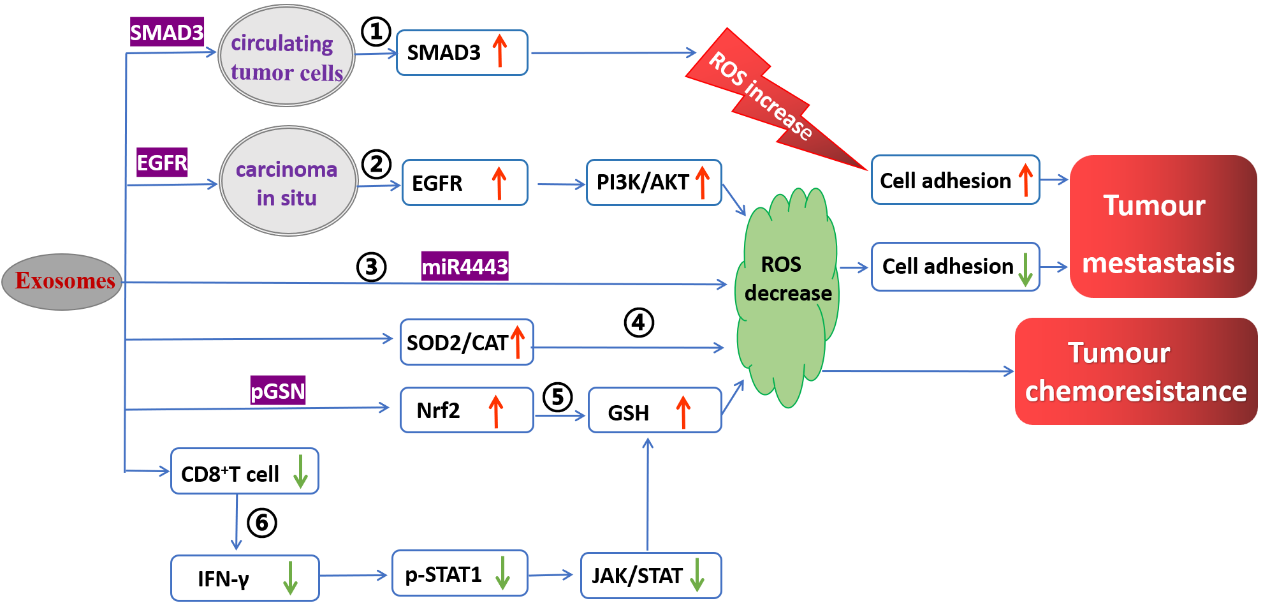
图2. 外泌体缓解受体细胞氧化应激研究表明肿瘤细胞的外泌体能够促进肿瘤转移以及耐药。其中的机制就包括肿瘤细胞外泌体通过传递信号分子到受体细胞,或者通过影响肿瘤微环境浸润的免疫细胞降低受体细胞ROS水平,导致原位肿瘤细胞的粘附性下降以及耐药性增强。也有研究发现肿瘤细胞外泌体通过传递SMAD3促进循环肿瘤细胞ROS的升高,促进细胞粘附性增加,利于循环肿瘤细胞穿过血管并定植在新的转移位置,促进肿瘤转移。可见,肿瘤外泌体对原位肿瘤细胞以及循环肿瘤细胞ROS水平的不同影响,参与肿瘤微环境调节(图3)。
图3. 肿瘤细胞外泌体促进肿瘤转移和耐药的机制参考文献:Crosstalk between Oxidative Stress and Exosomes. Oxid Med Cell Longev2022, 2022:3553617.
外泌体资讯网 Oxid Med Cell Longev | 香港中文大学(深圳)医学院杜鹃教授团队:氧化应激与外泌体的相互作用