细胞外囊泡(Extracellular vesicles, EVs)由于其携带疾病相关的蛋白质或核酸分子,已证明可以作为疾病诊断的重要生物标志物。具有表面等离子体共振效应(LSPR)的纳米结构可以作为探针被用来标记EV表面分子并产生相应信号,广泛用于 EV 传感,但需要在依赖于材料尺寸的信号强度和结合效率之间进行权衡。铜纳米颗粒由于其优异的LSPR效应,可以作为探针产生强的散射信号,提高检测的灵敏度。现有的增强等离子体信号方法通常需要复杂的材料合成步骤。该问题的一种解决方案是在已成功结合目标生物标志物的纳米颗粒上诱导成核并进行原位纳米颗粒生长以进行信号放大,但材料生长方法普遍需要苛刻的条件或缺乏成核特异性,容易对生物样本性质造成破环,或破坏抗体-蛋白抗原之间的免疫结合, 不适用于在生物样本表面实现。近日,来自杜兰大学的Tony Hu课题组在Small上以“Monocrystalline Labeling Enables Stable Plasmonic Enhancement for Isolation-Free Extracellular Vesicle Analysis”为题发表了研究论文(2022 Nov 10;e2204298)。这项工作报道了一种原位铜壳生长介导的等离子体增强的细胞外囊泡免疫检测平台(Cu-NEI),利用单晶金纳米棒免疫标记并原位生长单晶铜壳的方法增强表面等离子体散射信号并通过暗场显微镜检测表达特性蛋白的细胞外囊泡。该方法不会破坏探针-靶标相互作用或脂质双层的结构,从而在不降低信号的情况下在金纳米棒探针上诱导单晶铜壳生长,实现 EV生物标志物检测。此方法提高了外泌体的检测限并在结核病临床样品中得到验证。
由于单晶金纳米棒的特性,原位生长的铜纳米颗粒同样具有单晶结构,表面等离子效应在理论上具有最优的增强效果,暗场显微镜下的散射光信号也证实了单晶铜壳具有稳定的增强信号。在 10 分钟的铜纳米壳生长反应后,这种方法将检测到的纳米粒子信号增加了大约两个数量级,从而提高了对低丰度EV的检测效果(图1)。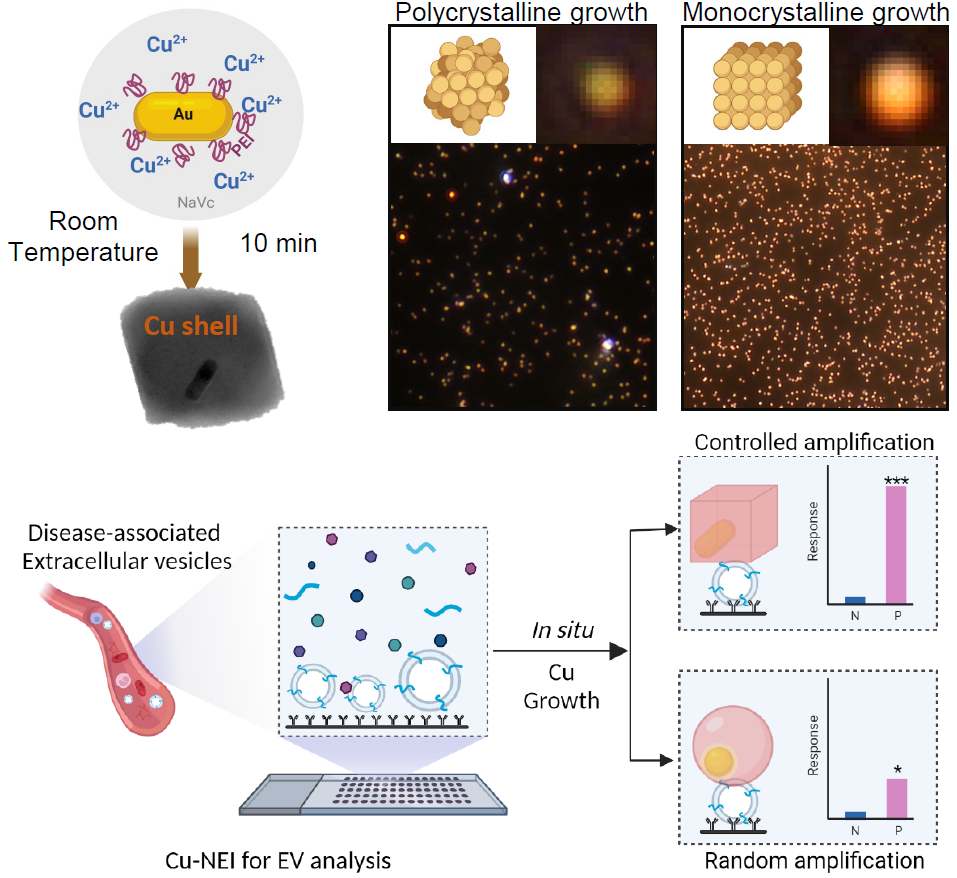
图1:利用单晶纳米材料介导的原位单晶铜壳生长方法用于表面等离子体增强-免疫测定(Cu-NEI)对外泌体进行免预分离分析。接下来研究人员将Cu-NEI应用于一组免疫缺陷-结核(HIV-TB)共感染的儿童临床样品的诊断。由于结核杆菌(Mtb)的特性, 传统儿童结核的诊断方法需要在痰液样本中培养结核杆菌, 由于采集HIV病人产生的痰液非常困难,因此传统方法灵敏度差(约15%)且费时费力。基于课题组已发表的工作(Nat. Biomed. Eng 6, 979–991 (2022)),发现血清中携带Mtb lipoarabinomannan(LAM)糖脂的EV可以作为诊断儿童结核的重要标志物。研究人员利用Cu-NEI平台对31个儿童结核病(TB)临床血清样本的检测,可以更好的区分来自携带LAM的EV的信号与背景信号。曲线下面积(Area Under Curve, AUC)达到0.92,并且可以成功诊断出传统方法漏诊的阳性病人。利用原位单晶铜纳米颗粒生长的方法标记并检测LAM-EV可以将儿童结核诊断的灵敏度提高至76.2%,这对儿童TB的诊断具有重要意义。Monocrystalline Labeling Enables Stable Plasmonic Enhancement for Isolation-Free Extracellular Vesicle Analysis, Small. 2022 Nov 10;e2204298. doi: 10.1002/smll.202204298.外泌体资讯网 Small:单晶纳米材料免疫标记介导的等离子体信号增强用于免预分离细胞外囊泡分析






