Brexogen公司首个进入临床试验阶段的外泌体疗法是外泌体治疗特应性皮炎。美国FDA已接受Brexogen公司BRE-AD01的Ⅰ期临床试验启动,这是一种基于外泌体的特应性皮炎(AD)疗法。韩国公司Brexogen正在使用自己的外泌体平台技术开发BRE-AD01。该试验是全球首个外泌体治疗特应性皮炎的Ⅰ期试验。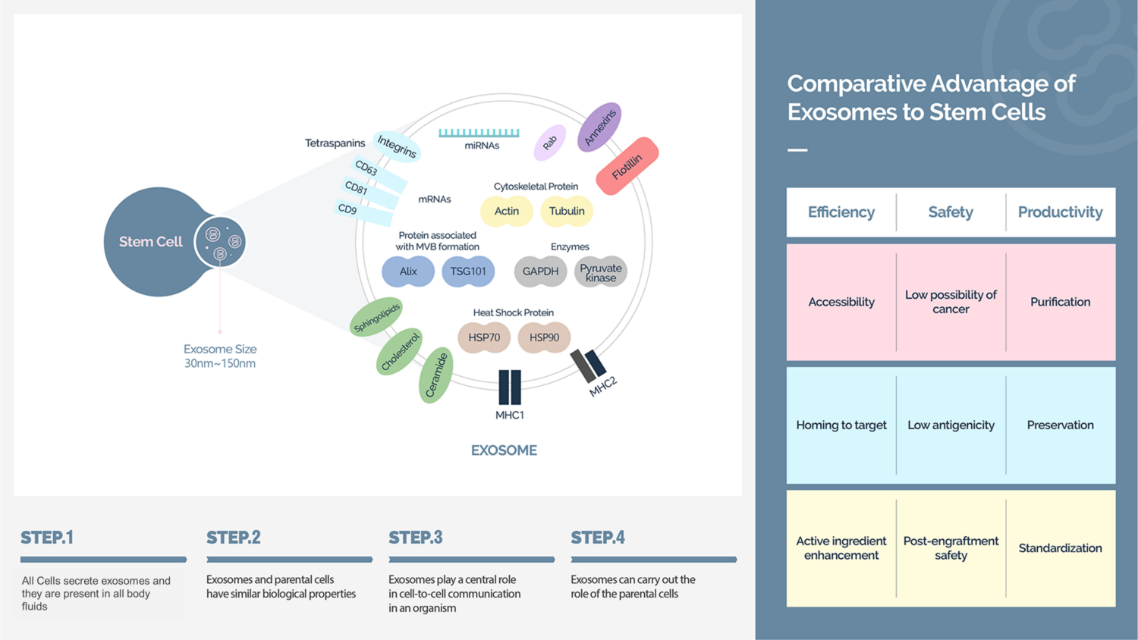
BRE-AD01是由干细胞用一种特定的、定义明确的临床可用化合物刺激产生的,这是Brexogen技术和开发的重要组成部分。在之前的临床前模型中,与目前的竞争药物如Janus激酶(JAK)抑制剂相比,BRE-AD01显示出积极的治疗效果。在动物身上使用BRE-AD01的临床前模型中,未报告任何不良事件。Breoxgen希望BRE-AD01能够成功抑制2型免疫反应,调节IL-31R,促进皮肤屏障恢复。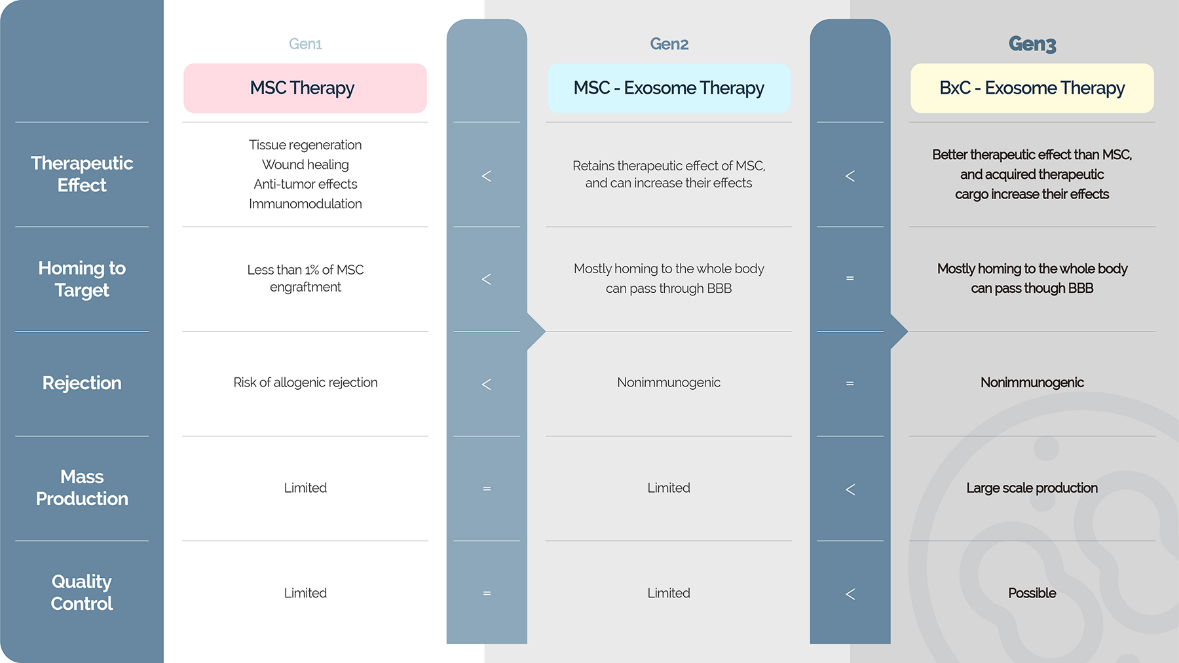
BxC-外泌体疗法在功效、效率、安全性、生产力和质量控制方面优于传统细胞疗法FDA生物制品评价与研究中心于2022年10月27日完成了对Brexogen公司BRE-AD01的Ⅰ期临床试验的审查,并确认Ⅰ期临床试验开始。在试验中,患有严重AD的患者将接受BRE-AD01。还将通过研究者整体评分法(IGA)、湿疹面积和严重程度指数以及特应性皮炎评分(SCORAD) 评估安全性和治疗效果。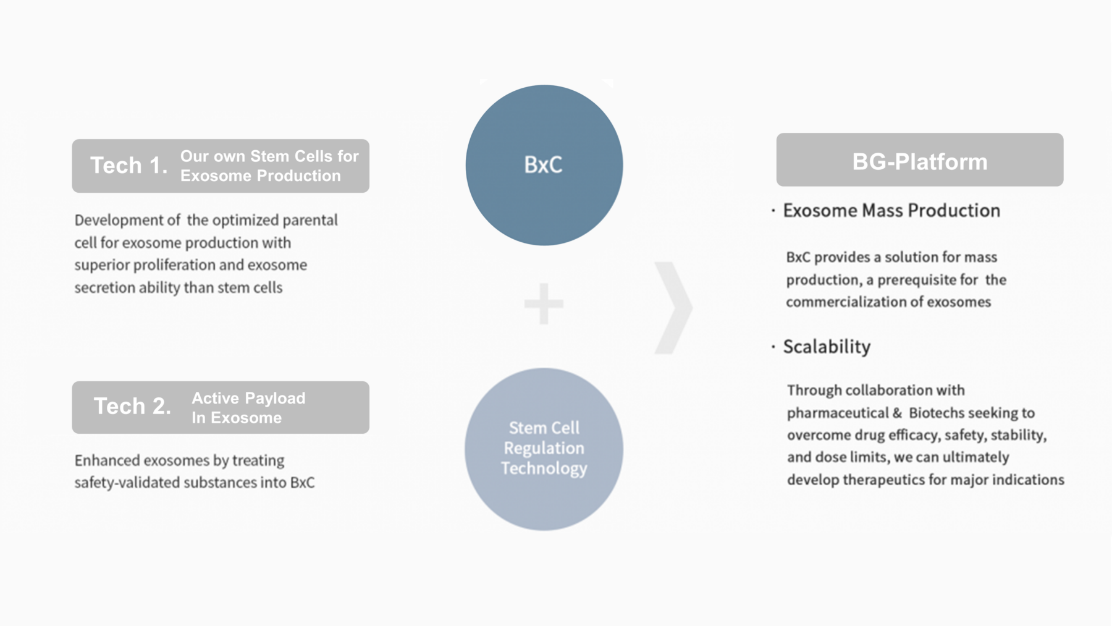
BG-Platform是通过优化干细胞及其产生的外泌体的蛋白质谱来建立的,从而可以获得所需的治疗结果Brexogen的创始人和首席执行官,医学博士SooKim,希望外泌体技术可以提高到可以商业化作为AD治疗的可靠选择的水平。Brexogen的干细胞启动策略将用于利用BRE-AD01临床试验的结果加速即将推出的管线药物的开发。后续试验将在1期试验成功完成后进行。Kim表示,外泌体疗法在开发过程中仍面临质量控制和制造过程等困难。Brexogen的技术通过优化治疗性货物装载的外泌体针对多种疾病,例如特应性皮炎(BRE-AD01)、心肌梗塞(BRE-MI01)和非酒精性脂肪性肝炎(BRE-NA01)。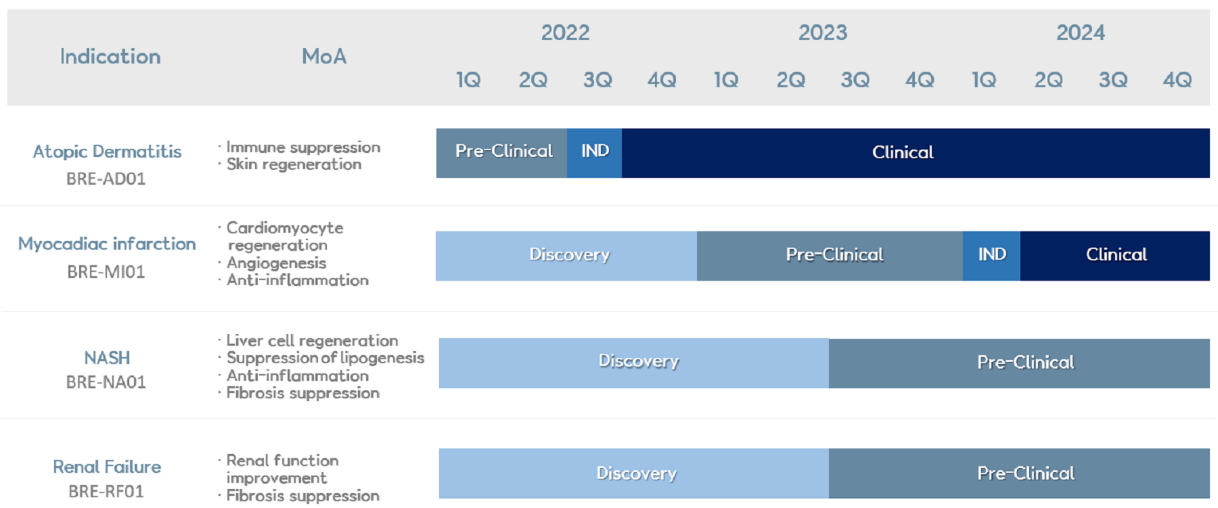
Brexogen公司于2019年3月成立,2019年10月获得220万美元的pre-A轮融资,2020年9月获得660万美元的A轮融资。公司总部位于韩国首尔,主要从事干细胞外泌体的疾病治疗应用开发。参考资料:Brexogen’s exosome therapy for atopic dermatitis, “BRE-AD01” accepted for phase 1 clinical trials by US FDA. PR Newswire. Published November 6, 2022. Accessed November 7, 2022.外泌体资讯网 Brexogen公司外泌体治疗特应性皮炎Ⅰ期临床试验获FDA批准








