近日,中山大学医学院张旭东副教授课题组在国际细胞外囊泡学会(ISEV)官方期刊Journal of Extracellular Vesicles (Q1,IF:17.34)上发表了题为“Biosynthetic neoantigen displayed on bacteria derived vesicles elicit systemic antitumour immunity”的研究论文 (2022 Dec;11(12):e12289)。研究团队利用基因工程细菌合成肿瘤新抗原(Neoantigen)并展示在细菌外膜上,利用携带新抗原的细菌外膜制备膜囊泡,开发了新型个性化肿瘤疫苗用于肿瘤治疗研究。
治疗性肿瘤疫苗,是将肿瘤抗原以各种佐剂形式递送至患者体内,抗原递呈细胞获取抗原后,激活患者自身的免疫系统,诱导机体产生抗原特异性的体液和细胞免疫应答,从而达到清除肿瘤细胞的目的。早期的肿瘤疫苗主要集中于利用肿瘤细胞中异常表达或过表达的自身抗原,即肿瘤相关抗原(tumor associated antigens, TAAs),制备多肽疫苗。但TAAs在临床上未能产生有效的抗肿瘤免疫反应。这些疫苗存在免疫原性低、肿瘤异质性等问题,导致大多数早期肿瘤疫苗在临床试验阶段终止。与TAAs相比,肿瘤特异性抗原又称新抗原(Neoantigen),是肿瘤细胞通过“非同义突变”产生的一种异常蛋白质。肿瘤特异性T细胞可以直接对突变的新表位驱动癌症免疫,引发强大的肿瘤特异性免疫反应。通过外显子组测序,突变抗原已可从患者肿瘤组织中被鉴定出来。因此,用新抗原开发的疫苗为增强肿瘤特异性免疫反应提供了机会。在目前的研究中,基于新抗原的疫苗已被证明可特异性诱导肿瘤抗原特异性CD4+和CD8+ T细胞应答,结合免疫检查点抑制(ICI)治疗可提高患者生存期。新抗原已成为个性化、肿瘤特异性癌症疫苗的最佳抗原。然而,新抗原开发的疫苗,其实际应用仍存在免疫识别效率低等问题。因此,开发高效的抗原特异性识别和传递系统是增强免疫治疗的潜在途径。目前,脂质体、外泌体、肿瘤细胞膜囊泡和细菌外膜囊泡 (OMV) 等一类脂质纳米颗粒 (NP) 已被广泛应用于肿瘤药物递送系统。其中,由革兰氏阴性细菌天然分泌的OMVs,由于其独特的外膜出芽形式,使其成分与亲本细菌相似,含有脂多糖(LPS)、外膜蛋白、脂质和核苷酸等。同时,OMVs还具有与病原体相当的大小,并包含多种病原体相关分子模式(pathogen-associated molecular patterns, PAMPs)和病原体相关抗原,可以有效激活机体的固有免疫。虽然OMV装载了各种免疫原,但作为疫苗载体,相比细菌本身表现出更可靠的安全性,是一种良好的肿瘤抗原潜在载体。
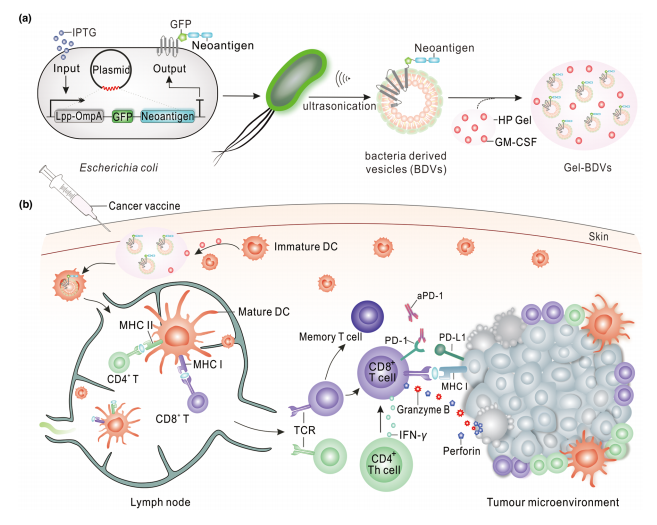
图1. Gel-BDVs的制备和联合PD-1抗体治疗肿瘤的机制示意图
- Gel-BDVs的制备过程;(b) Gel-BDVs激活效应T细胞对抗黑色素瘤;TCR:T细胞受体,MHC-I:主要组织相容性复合体I,MHC-II:主要组织相容性复合体II
基于以上研究背景,张旭东副教授团队基于合成生物学,通过基因工程手段将特定的新抗原合成并定位到细菌外膜上,进而实现肿瘤新抗原在细菌外膜的呈递。研究人员首先利用基因工程手段,将个体化肿瘤新抗原稳定表达在大肠杆菌外膜上,再通过超声等方法制备了表达新抗原的细菌外囊泡(Bacterial-derived vesicles,BDVs)。进而将表达新抗原的仿生细菌外囊泡(BDV-Neo)与粒细胞巨噬细胞刺激因子(GM-CSF)包裹进温敏型HP水凝胶,联合制备肿瘤疫苗(Gel-BDVs)。该疫苗通过皮下接种,可持续释放GM-CSF,进而募集DC细胞摄取BDVs获取新抗原,进而促使初始T细胞活化及分化成效应T细胞。该疫苗与检查点阻断药物PD-1抗体联用,可以有效增强CD8+ 细胞毒性T细胞 (CTL) 的活性和增殖能力,高效的识别并清除肿瘤细胞。此外,肿瘤特异性T细胞可转化为记忆T细胞,增强抗肿瘤效应,有效减缓术后残留肿瘤的复发和转移,延长了术后生存期。综上所述,展示新抗原的细菌囊泡疫苗可有效激发特异性肿瘤免疫反应,该研究为个性化癌症疫苗的开发提供了新的思路,具有良好的应用转化前景。
该研究论文第一完成单位为中山大学医学院。中山大学医学院张旭东副教授和广东医科大学基础医学院梁欣博士为论文的共同通讯作者。中山大学医学院特聘副研究员孟繁蔷、研究生张芷让和李丽艳为共同第一作者。这项工作得到了国家自然科学基金,广东省自然科学基金,深圳市优秀科技创新人才培养项目(优青项目),深圳市基础研究重点项目等的支持。
参考文献:
Biosynthetic neoantigen displayed on bacteria derived vesicles elicit systemic antitumour immunity, Journal of Extracellular Vesicles (2022), 11, e12289. https://doi.org/10.1002/jev2.12289
外泌体资讯网 Journal of Extracellular Vesicles | 中山大学张旭东团队:工程化细菌膜囊泡展示新抗原用于肿瘤免疫治疗