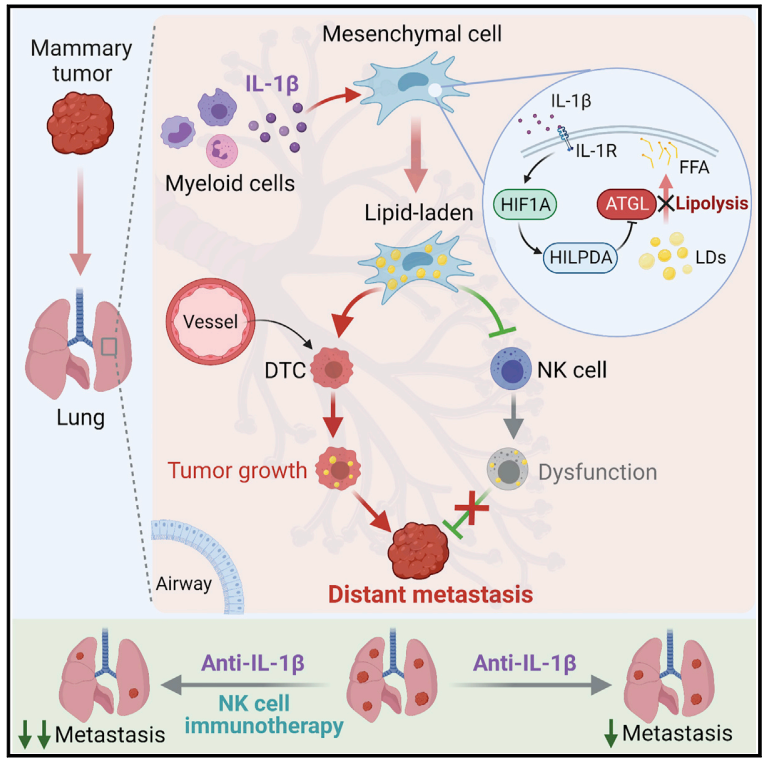
众所周知,肿瘤转移的发生离不开远端器官的微环境支持,但其在这一过程中,代谢如何调节肿瘤转移微环境,其机制目前仍未确定。来自美国杰克森实验室任光文课题组的研究人员发现肺间充质细胞中富含大量脂质,其可以通过外泌体样囊泡的分泌途径将脂质传递给肿瘤细胞和NK细胞,重塑肿瘤前微环境并促进乳腺癌肺转移。相关研究以“Lipid-laden lung mesenchymal cells foster breast cancer metastasis via metabolic reprogramming of tumor cells and natural killer cells”为题发表在Cell Metabolism杂志上。
90%的实体肿瘤引起的相关死亡,是由于远端重要器官的肿瘤转移和治疗后的复发。在肿瘤转移的多个步骤中,播散肿瘤细胞(disseminated tumor cells,DTCs)的远端器官定植是一个效率低下且速度受限的步骤,只有非常低比例的DTC能够逃避了强大的免疫监测,从原发肿瘤位置扩散出来,并在新的具有挑战性的其他器官环境中生存,最终定植在远端的器官。肿瘤转移研究的一系列重大进展揭示了DTC和器官转移前生态位之间复杂的相互作用,这对转移病灶的发展至关重要。然而,这种DTC-器官相互作用主要在细胞、转录层和蛋白质水平上进行研究。目前尚不清楚器官微环境是否可以在代谢上调节DTC。
目前,有限的证据显示,临床前肿瘤模型中器官生态位定植中存在着代谢调节的概念。在乳腺癌肺转移模型中,在肺间质液中富集的丙酮酸被DTC吸收,启动代谢级联,重编程了细胞外基质,帮助肺转移生态位的形成。在卵巢癌模型中,大网膜脂肪细胞通过脂肪酸氧化(FAO)为DTC提供能量,或激活DTC中的生存和增殖相关信号通路,促进卵巢癌向大网膜转移。这些结果强调了器官微环境在代谢上支持DTC定植方面的新作用。
在实体瘤容易发生的重要器官中,肺是最常见的部位之一。在肺的微环境中,先前的研究表明,浸润的先天性免疫细胞中中性脂质的积累赋予了它们促进肿瘤转移的能力,有助于形成转移前和转移后的生态位。
在这项研究中,研究人员发现肺间充质细胞(mesenchymal cells,MCs)在未发病和荷瘤状态下都表现出高水平的细胞内甘油三酯(TG)含量。研究人员将TG在其中一种肺MCs——脂肪成纤维细胞中进行了研究,发现TG可以保护肺泡免受氧化损伤,并在肺泡发育过程中为肺表面活性剂合成提供底物。然而,肺MC来源的中性脂质在病理过程中的作用仍然是未知的。因此,研究人员利用乳腺癌小鼠模型,研究了肺MCs通过中性脂代谢调节乳腺癌肺转移的机制。
在该乳腺癌模型中,研究人员发现肺间充质细胞MCs在转移前阶段积累了大量中性脂质。而这是由白细胞介素-1β (IL-1β)介导的缺氧诱导脂滴相关蛋白(HILPDA)介导的,HILPDA随后抑制肺MCs中的脂肪甘油三酯脂肪酶(ATGL)活性。小鼠中MC特异性ATGL或HILPDA基因的敲除分别增强和减少了乳腺癌的肺转移,这表明含脂MCs具有促进转移的作用。在机制上,含脂质的MCs通过外泌体样囊泡将脂质运输到肿瘤细胞和自然杀伤细胞(NK),最终导致肿瘤细胞生存和增殖,以及NK细胞功能障碍的增强。阻断IL-1β单独可以显示显著的肿瘤抑制,也发现可以提高NK细胞的免疫治疗效果并减轻肺转移。总的来说,肺MCs通过脂质代谢调节肿瘤细胞进展和抗肿瘤免疫,促进乳腺癌肺转移。
尽管研究人员发现中性脂质,从含富含脂质的MCs中转运出来后,在肿瘤细胞(利用脂质)和NK细胞(储存脂质)中经历了不同的命运。然而,潜在的分子机制仍有待确定。此外,原位鉴定脂质来源、MCs释放脂质的刺激因子以及不同肺环境细胞间的脂质转运还有待进一步探索。虽然从含脂的MCs释放的外泌体样囊泡介导肿瘤细胞和NK细胞的功能重编程,但来自细胞外囊泡的确切代谢物仍有待鉴定。含脂MCs仅在肺转移模型的背景下进行了研究,未来研究人员将继续了解这种代谢表型在其他情况下,如稳态、炎症、肺癌和其他肺部疾病中的作用。
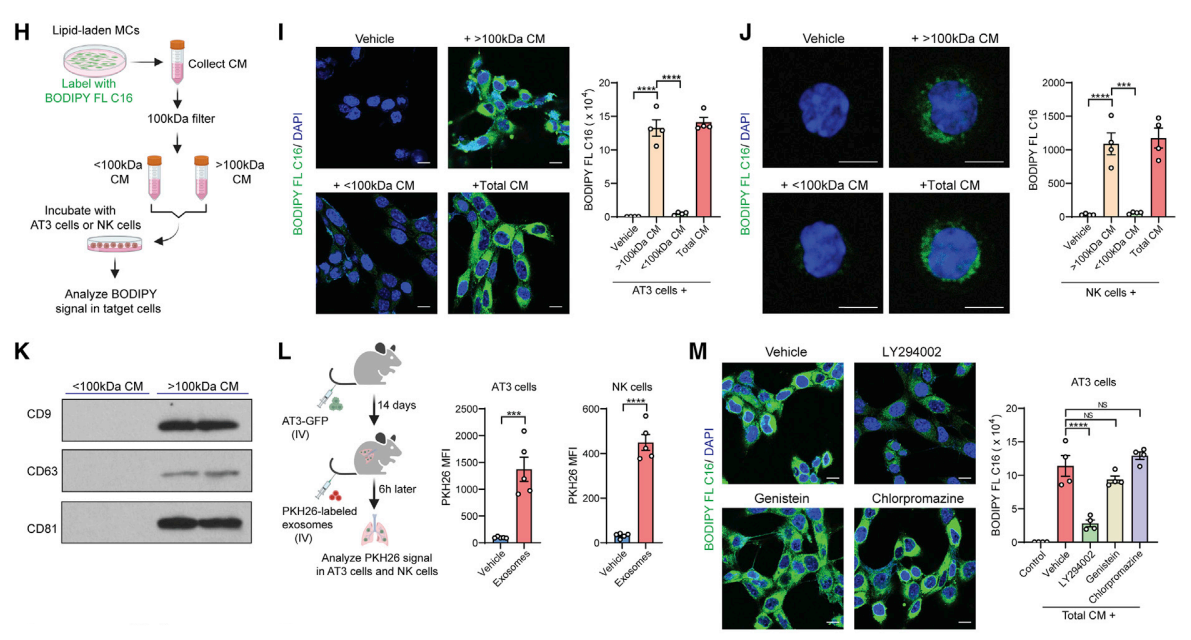
图:含脂MCs通过外泌体样囊泡将脂质运输到肿瘤细胞和NK细胞。通过溶酶体途径抑制剂抑制承载脂质的MCs的脂质转运,可以消除肿瘤细胞和NK细胞的代谢重编程,从而减少肿瘤转移性定植。
参考文献:Lipid-laden lung mesenchymal cells foster breast cancer metastasis via metabolic reprogramming of tumor cells and natural killer cells. Cell Metab. 2022 Dec 6;34(12):1960-1976.e9.