尽管肌腱损伤的治疗已经取得显著进步,当下仍有大量患者缺乏有效的治疗措施。近期,间充质干细胞来源的细胞外囊泡治疗被报道称,可以通过调控巨噬细胞的免疫表型来发挥治疗作用。作为一种生物材料,生物活性玻璃预处理间充质干细胞,可强化干细胞旁分泌作用并促进组织修复中的成血管进程,亦在近期被首次提出。然而,生物活性玻璃赋能细胞外囊泡的是否可以作为一种高效的无细胞治疗手段,其调控巨噬细胞极化表型和促进血管再生的机制仍不清晰。
近日,来自香港中文大学的研究人员报道了经生物活性玻璃预处理人源脂肪干细胞,通过提纯脂肪干细胞条件培养基,获得的工程化细胞外囊泡治疗肌腱损伤的研究成果,并以“Bioactive glass-elicited stem cell-derived extracellular vesicles regulate M2 macrophage polarization and angiogenesis to improve tendon regeneration and functional recovery”为题发表在Biomaterials上(2023 Jan 10;294:121998). 香港中文大学矫形外科与创伤学系许宏涛博士(现南京医科大学附属第一医院主治医师),香港中文大学组织工程与再生医学研究所朱彦伦博士和香港中文大学矫形外科与创伤学系Allen Wei-Ting HSIAO博士为该文章共同第一作者,河内医科大学第三医院张英泽院士、香港中文大学Vivas Hon Fai CHAN教授和台中中国医药大学Chien-Wei LEE教授为本文共同通讯作者。
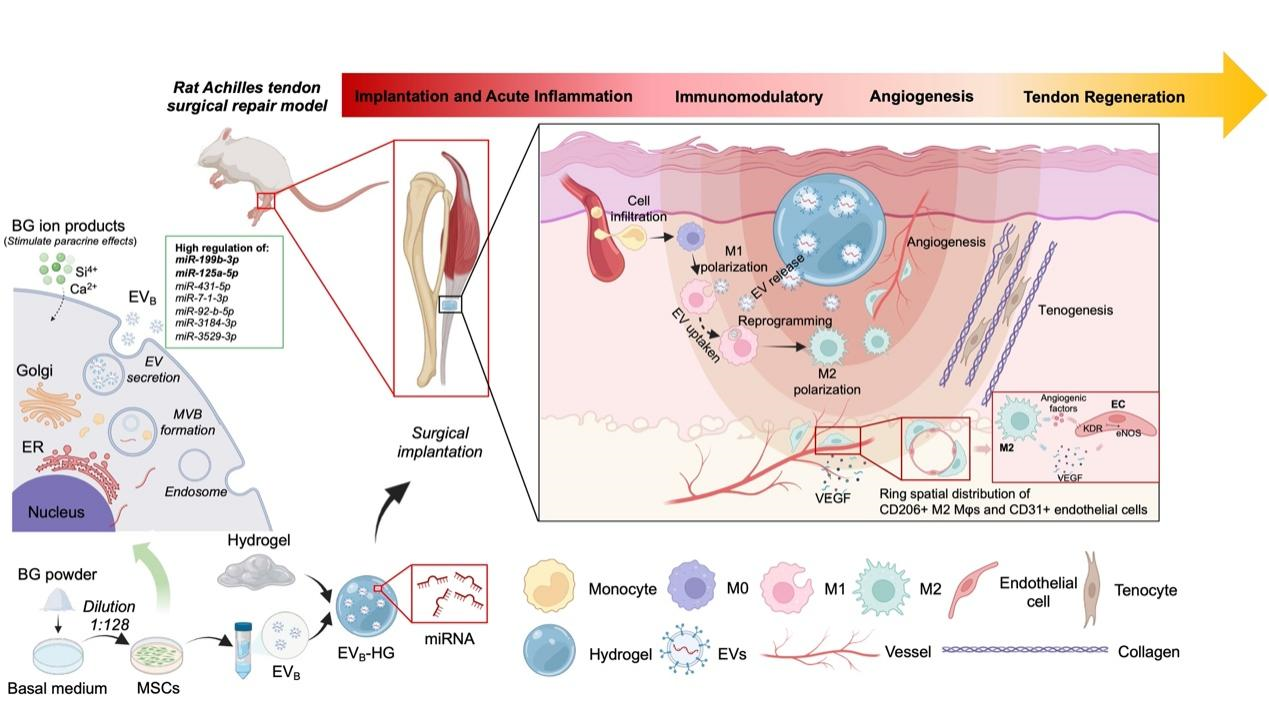
为使细胞外囊泡在肌腱损伤部位贮留和缓释,研究者采用紫外光合交联甲基丙烯酰水凝胶装载赋能细胞外囊泡,获得水凝胶-细胞外囊泡支架复合体,并在跟腱缝合术中同期植入损伤部位。赋能细胞外囊泡的局部释放,原位激活新生肉芽组织内巨噬细胞浸润,激活抗炎极化表型(M2型)转化进程,进而募集血管内皮细胞迁移浸润,诱导M2型巨噬细胞与再生血管产生空间关联性。通过microRNA测序分析赋能细胞外囊泡装载的小RNA等内容物改变。
体内试验结果表明,赋能细胞外囊泡可有效诱导M2型巨噬细胞极化转变并促进血管再生进程,并在肌腱再生区域新生肉芽组织内部形成C206+ M2型巨噬细胞围绕CD31+血管内皮细胞的环状紧密结构(Ring Spatial Distribution);显著性提高肌腱成熟相关标记物的表达;同时可抵抗修复术后跟腱体部有害性延长和跟腱横截面扩大;有效恢复跟腱生物力学性能,包括极限负载,刚度,拉伸弹性模量,和腓肠肌-跟腱-跟骨复合体再断裂模式。体外试验表明,生物活性玻璃赋能细胞外囊泡能够有效促进M2型巨噬细胞极化;同时赋能细胞外囊泡处理的巨噬细胞条件培养基能够显著性促进血管内皮细胞的迁移和成血管基因VEGF,eNOS和KDR的高表达,并且,显著性加快血管内皮细胞成管实验中的管腔形成进程。microRNA测序分析解释了生物活性玻璃预处理赋能的细胞外囊泡是通过上调内部miR-199b-3p和miR-125a-5p等小RNA的装载,进而实现调控巨噬细胞介导的血管再生。
综上所述,生物活性玻璃赋能的细胞外囊泡通过影响损伤部位微环境,进而能够有效促进巨噬细胞介导的再血管化进程,并有效促进局部肌腱损伤后组织再生,其效果优于未赋能的细胞外囊泡。该研究为生物活性玻璃赋能细胞外囊泡结合生物水凝胶治疗肌腱损伤提供了重要研究基础和转化应用依据。
示意图:生物活性玻璃赋能外泌体装载的水凝胶复合体能够通过调控巨噬细胞介导再血管化以促进肌腱再生
参考文献:
Bioactive glass-elicited stem cell-derived extracellular vesicles regulate M2 macrophage polarization and angiogenesis to improve tendon regeneration and functional recovery, Biomaterials. 2023 Jan 10;294:121998. doi: 10.1016/j.biomaterials.2023.121998.
外泌体资讯网 Biomaterials |香港中文大学:生物活性玻璃赋能间充质干细胞来源的细胞外囊泡调控M2型巨噬细胞和再血管化以促进肌腱再生