新年好!1月份国内新出的细胞外囊泡/外泌体领域论文不完全统计有321篇。IF>10的有68篇、F>20的有15篇。本期主要内容包括:肿瘤外泌体miR-141控制卵巢癌的转移前生态位形成、细胞微粒递送化学药物重置巨噬细胞的抗肿瘤活性、细胞外囊泡介导SARS-CoV-2的抗体抗性传播、大小EVs的生物分布和致瘤潜力、肝细胞癌、老化皮肤的修复、肌肉再生、细胞外囊泡对铁代谢的体液调节驱动抗菌反应等方面内容。内容十分丰富,不容错过。全部文献列表及部分文章原文可在外泌体之家论坛同名贴下下载。
1.香港中文大学陈卫教授等:肿瘤分泌的外泌体miR-141激活肿瘤-基质相互作用并控制卵巢癌转移中的转移前生态位形成Mo, Y., et al. (2023). "Tumor-secreted exosomal miR-141 activates tumor-stroma interactions and controls premetastatic niche formation in ovarian cancer metastasis."
Mol Cancer 22(1): 4. IF= 41.444转移定植是肿瘤转移的关键步骤之一。转移定植需要转移前生态位,并由肿瘤-基质相互作用决定,但其机制基础仍未完全了解。基于PCR的miRNome分析、qPCR、免疫荧光分析评估了外泌体miR-141的表达和细胞间通讯。LC-MS/MS蛋白质组学分析和双荧光素酶分析将YAP1鉴定为miR-141的直接靶标。细胞因子分析、ChIP、荧光素酶报告基因检测和亚细胞分级分析证实YAP1可调节GROα的产生。一系列体外致瘤试验、离体模型和Yap1基质条件敲除(cKO)小鼠模型证明了miR-141/YAP1/GROα/CXCR1/2信号级联的作用。RNAi、CRISPR/Cas9和CRISPRi系统用于基因沉默。包括血清、OvCa肿瘤组织样本和组织阵列用于临床相关性评估。结果:Hsa-miR-141-3p(miR-141)是一种外泌体miRNA,由卵巢癌细胞高度分泌,并将基质成纤维细胞重编程为促炎性癌症相关成纤维细胞(CAF),从而促进转移定植。一项机制研究表明,miR-141靶向YAP1(Hippo通路的关键效应子),降低核YAP1/TAZ比率并增强基质成纤维细胞产生GROα。小鼠模型中Yap1的基质特异性敲除(cKO)塑造了富含GROα的微环境,促进了体内肿瘤定植,但这种效应在OvCa细胞中的Cxcr1/2耗尽后被逆转。YAP1/GROα相关性在临床样本中得到证实,突出了这项研究的临床相关性,并为阻碍卵巢癌转移前生态位形成和转移进展提供了潜在的治疗干预。结论:本研究揭示了miR-141作为OvCa衍生的外泌体microRNA,通过激活YAP1/GROα/CXCRs信号级联来介导肿瘤-间质相互作用和肿瘤促进间质生态位的形成,为卵巢癌腹膜转移患者的治疗提供了新的见解。
2.【综述】中南大学:液体活检在胃癌中的临床应用及检测技术Ma, S., et al. (2023). "Clinical application and detection techniques of liquid biopsy in gastric cancer."
Mol Cancer 22(1): 7. IF=41.444这篇综述介绍了循环肿瘤细胞、循环游离DNA、循环肿瘤DNA、非编码RNA、外泌体和蛋白质的临床应用,这些都是胃癌液体活检技术的主要标志物。
3.中国医学科学院基础医学研究所黄波课题组与华中科技大学马婧薇团队合作:细胞微粒中的化学药物通过激活溶酶体P450和核hnRNPA2B1来重置巨噬细胞的抗肿瘤活性Wei, K., et al. (2023). "Chemo-drugs in cell microparticles reset antitumor activity of macrophages by activating lysosomal P450 and nuclear hnRNPA2B1."
Signal Transduct Target Ther 8(1): 22. IF=38.104肿瘤中的巨噬细胞(肿瘤相关巨噬细胞,TAM)是大多数肿瘤中的主要细胞群,通过刺激血管生成、增强肿瘤细胞生长和抑制抗肿瘤免疫发挥关键的稳态功能。通过简单、有效和安全的方法重置TAMs是增强抗肿瘤免疫力和减轻肿瘤细胞恶性肿瘤的理想方法。以前的研究中使用肿瘤细胞衍生的微粒来包装化疗药物(药物-MPs),通过中性粒细胞募集在人类恶性胸腔积液中产生了显著的治疗效果,暗示药物-MPs可能会重置TAMs,考虑到M2的抑制作用巨噬细胞对中性粒细胞的募集和激活。该研究表明药物-MPs可以通过重置具有M1表型和IFN-β释放的TAM来发挥抗肿瘤免疫调节剂的作用。从机制上讲,肿瘤MPs中的药物分子激活巨噬细胞溶酶体P450单加氧酶,导致超氧阴离子形成,从而通过激活溶酶体NOX2进一步放大溶酶体ROS的产生和pH值。因此,溶酶体Ca(2+)信号被激活,从而使巨噬细胞极化至M1。同时,药物分子从溶酶体输送到细胞核,在那里它们激活DNA传感器hnRNPA2B1以产生IFN-β。这种溶酶体-核机制通过靶向溶酶体pH和核先天免疫充分激发巨噬细胞的抗肿瘤活性。这些发现强调药物-MPs可以通过恢复巨噬细胞的抗肿瘤活性作为一种新的免疫治疗方法。这种机制的阐明可以转化为通过药物-MPs结合PD-1阻断来治疗恶性腹水。4.中国科学院上海药物研究所高召兵研究员、李佳研究员、武汉病毒研究所张磊砢研究员、昆明动物研究所郑永唐研究员合作:细胞外囊泡介导SARS-CoV-2的抗体抗性传播Xia, B., et al. (2023). "Extracellular vesicles mediate antibody-resistant transmission of SARS-CoV-2."
Cell Discov 9(1): 2.IF=38.079严重急性呼吸系统综合症冠状病毒2(SARS-CoV-2)已引起全球大流行。抗体耐药性抑制了中和抗体疗法,并威胁到当前的全球冠状病毒(COVID-19)疫苗接种活动。除了出现耐药SARS-CoV-2变体之外,人们对SARS-CoV-2如何逃避抗体知之甚少。该研究报告了一种新的细胞外囊泡(EV)介导的SARS-CoV-2细胞间传播机制,该机制有助于SARS-CoV-2逃避中和抗体。这些EV最初是在SARS-CoV-2包膜蛋白表达细胞中观察到的,由各种SARS-CoV-2感染细胞分泌,包括VeroE6、Calu-3和HPAEpiC细胞,这些细胞正在经历感染诱导的细胞焦亡。各种SARS-CoV-2感染细胞产生类似的EV,其特征是超大尺寸(直径1.6-9.5μm,平均直径>4.2μm)比之前报道的病毒产生的囊泡大得多。透射电子显微镜分析和斑块测定表明,这些SARS-CoV-2诱导的EV含有大量活病毒颗粒。特别是,包裹着囊泡的SARS-CoV-2病毒对中和抗体具有抗性,并且能够独立于报告的受体和辅因子重新感染幼稚细胞。一致地,构建的3D图像显示完整的EV可以直接被受体细胞吸收,支持SARS-CoV-2的囊泡介导的细胞间传播。该研究结果揭示了一种通过细胞间传播的受体非依赖性SARS-CoV-2感染的新机制,为SARS-CoV-2的抗体抗性提供了新的见解,并为未来的抗病毒治疗提出了潜在的目标。前期报道:https://www.exosomemed.com/13272.html
5.【综述】武汉大学人民医院:脂肪组织巨噬细胞——对肥胖相关癌症的影响Li, B., et al. (2023). "Adipose tissue macrophages: implications for obesity-associated cancer."
Mil Med Res 10(1): 1. IF=34.915这篇综述描述了脂肪组织巨噬细胞 (ATM)的起源、表型和功能。随后总结了肥胖相关微环境中ATM重编程的潜在机制,包括功能失调代谢物的直接交换、过多的细胞因子和其他信号介质、细胞外囊泡货物的转移以及肠道微生物群及其代谢物的变化。更好地了解ATM在肥胖条件下的特性和功能将促进开发针对肥胖相关癌症的新治疗干预措施。
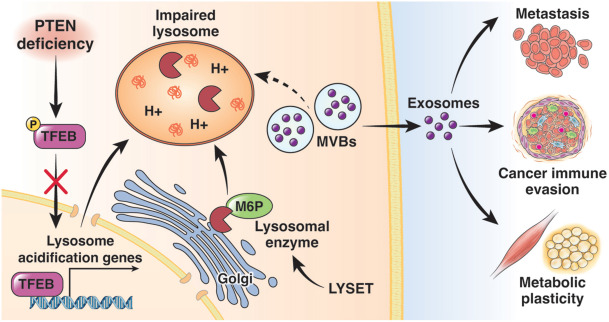
6.【评论】北京协和医学院刘芝华研究员与俄克拉何马大学健康科学中心合作:溶酶体通过PTEN缺陷肿瘤的外泌体促进癌症转移Zhou, Z., et al. (2023). "Lysosomes Promote Cancer Metastasis via Exosome in PTEN-Deficient Tumors."
Gastroenterology. IF=33.883
7.台湾研究院原子与分子科学研究所:膜蛋白修饰在体内调节乳腺癌中大小细胞外囊泡的生物分布和致瘤潜力Magoling, B. J. A., et al. (2023). "Membrane Protein Modification Modulates Big and Small Extracellular Vesicle Biodistribution and Tumorigenic Potential in Breast Cancers in vivo."
Adv Mater: e2208966.IF=32.086细胞释放细胞外囊泡(EV),以在病理和生理条件下介导细胞间通讯。虽然对小型EV(sEV;<100-200nm,外泌体)进行了深入研究,但对中型和大型EV(大型EV[bEV];>200nm,微泡)的特性和功能研究较少。该研究将bEV和sEV识别为不同的EV群体,并确定bEV在侵袭性人类三阴性乳腺癌(TNBC)亚型中以更高的bEV:sEV比率释放。PalmGRET是一种基于生物发光共振能量转移(BRET)的EV报告基因,与亲脂性荧光染料相比,揭示了在非致死和生理EV剂量下的剂量依赖性EV生物分布。值得注意的是,bEVs和sEVs表现出独特的生物分布特征,在同源免疫活性TNBC乳腺肿瘤小鼠模型中单独促进体内肿瘤生长。bEV和sEV共享质谱(MS)鉴定的肿瘤进展相关EV表面膜蛋白(tpEVSurfMEM),其中包括SLC29A1、CD9和CD44。tpEVSurfMEM耗尽减弱了EV肺器官向性,改变了生物分布,并降低了致癌潜力。这项研究确定了bEV和sEV在乳腺癌中的不同体内特性和功能,这表明bEV在疾病、诊断和治疗应用中的重要作用。
8.【综述】南方医科大学南方医院郑磊教授:植物来源的囊泡状纳米颗粒作为有前途的生物治疗工具Feng, J., et al. (2023). "Plant Derived Vesicle-Like Nanoparticles as Promising Biotherapeutic Tools: Present and Future."
Adv Mater: e2207826. IF=32.086细胞外囊泡(EV)是异质的、磷脂双层封闭的生物颗粒,可通过分子货物输送和表面信号传导调节细胞通讯。EV由几乎所有活细胞分泌,包括植物细胞。植物来源的囊泡状纳米颗粒(PDVLN)是一个通用术语,指的是从植物中分离出的囊泡状纳米结构颗粒。它们的低免疫原性和广泛可用性使PDVLN更安全、更经济地开发为治疗剂和药物载体。越来越多的证据表明PDVLN在调节人与植物之间的界间串扰中的关键作用。PDVLN能够进入人体系统并将效应分子递送至调节细胞信号通路的细胞。因此,由植物释放或从植物中获得的PDVLNs对人类健康和疾病有很大影响。这篇综述介绍了PDVLN的生物发生、详细制备方法、各种物理和生化特性、生物安全性和保存,以及这些特性如何与其生物安全性和保存性相关。然后,系统地讨论了PDVLN在不同植物和哺乳动物疾病中的潜在应用以及PDVLN研究标准化。
9.香港大学Irene Oi-Lin Ng教授:S100A10通过细胞外囊泡转移和调节其蛋白质货物促进HCC的发展和进展Wang, X., et al. (2023). "S100A10 promotes HCC development and progression via transfer in extracellular vesicles and regulating their protein cargos."
Gut.IF=31.793越来越多的证据表明肿瘤细胞表现出与其谱系祖细胞相似的特征。研究发现S100钙结合蛋白A10(S100A10)表现出类似于肝祖基因的表达模式。然而,S100A10在肝细胞癌(HCC)进展中的作用尚不清楚。此外,细胞外囊泡(EV)是肿瘤发生和转移的关键介质,但S100A10的细胞外功能,尤其是与EV(EV-S100A10)相关的细胞外功能尚不清楚。该研究在体外和体内研究了S100A10和EV-S100A10在HCC进展中的功能和机制。针对S100A10的中和抗体(NA)用于评估EV-S100A10的显着性。结果显示,在功能上,S100A10在体外和体内促进HCC的起始、自我更新、化学抗性和转移。重要的是,研究发现HCC细胞在体外和HCC患者的血浆中都将S100A10分泌到EV中。富含S100A10的EV可增强HCC细胞的干性和转移能力,上调表皮生长因子受体(EGFR)、AKT和ERK信号,并促进上皮-间质转化。EV-S100A10还在HCC细胞运动中充当趋化剂。重要的是,S100A10控制EV中的蛋白质货物,并通过与整合素αⅤ的物理结合介导MMP2、纤连蛋白和EGF与EV膜的结合。重要的是,用S100A10-NA阻断EV-S100A10会显著消除这些增强作用。结论:总而言之,结果表明,S100A10通过其在EV中的转移和调节EV的蛋白质货物显著促进HCC进展。EV-S100A10可能是HCC进展的潜在治疗靶点和生物标志物。
10.北京大学深圳研究生院的Andrew S Lee 教授团队:细胞外囊泡递送胶原蛋白mRNA用于老化皮肤的修复You, Y., et al. (2023). "Intradermally delivered mRNA-encapsulating extracellular vesicles for collagen-replacement therapy."
Nat Biomed Eng. IF=29.234前期报道:https://www.exosomemed.com/13210.html
11.空军军医大学金岩教授团队:MSCs衍生的凋亡细胞外囊泡通过诱导成肌细胞释放Pannexin 1通道依赖性肌酸来促进肌肉再生Ye, Q., et al. (2023). "MSCs-derived apoptotic extracellular vesicles promote muscle regeneration by inducing Pannexin 1 channel-dependent creatine release by myoblasts."
Int J Oral Sci 15(1): 7.IF=24.897
12.【综述】四川大学华西医院应斌武:人源唾液生物标志物检测在临床诊断中的应用前景Song, M., et al. (2023). "Promising applications of human-derived saliva biomarker testing in clinical diagnostics."
Int J Oral Sci 15(1): 2.IF=24.897
13.【综述】国家纳米中心梁兴杰研究员、北京理工大学黄渊余教授:克服核酸药物研发的制药瓶颈Lu, M., et al. (2023). "Overcoming Pharmaceutical Bottlenecks for Nucleic Acid Drug Development."
Acc Chem Res. IF=24.466
14.上海交通大学仁济医院陈东芹教授等:外泌体LOC85009通过调节ATG5诱导的自噬抑制肺腺癌多西紫杉醇耐药Yu, Z., et al. (2022). "Exosomal LOC85009 inhibits docetaxel resistance in lung adenocarcinoma through regulating ATG5-induced autophagy."
Drug Resist Updat 67: 100915. IF=22.841
15.四军医大学刘世宇、金岩团队:细胞外囊泡对铁代谢的体液调节驱动抗菌反应Kuang, H., et al. (2023). "Humoral regulation of iron metabolism by extracellular vesicles drives antibacterial response."
Nat Metab 5(1): 111-128.IF=19.865宿主启动的立即限制铁是防止细菌感染的关键过程,并且已经在肝脏和脾脏中进行了描述,但目前尚不清楚这种反应是否还需要一种体液机制,该机制可以在感染时实现铁的全身隔离。该研究表明在细菌入侵后,宿主巨噬细胞会立即释放捕获循环含铁蛋白质的细胞外囊泡(EV)。从机制上讲,在雌性小鼠的败血症模型中,肠沙门氏菌亚种,鼠伤寒肠杆菌可诱导巨噬细胞内质网应激并激活需要肌醇的酶1α信号,引发溶酶体功能障碍,从而促进EV的释放,EV具有铁摄取所需的多种受体。通过与循环中的含铁蛋白质结合,这些EV可以防止细菌获取铁,从而抑制它们的生长并最终防止感染和相关组织损伤。该研究结果揭示了一种体液机制,可以在细菌感染期间迅速调节全身铁代谢。
16.深圳市康宁医院荣晗教授等:重度抑郁症患者星形胶质细胞的过度炎症——来自血清星形胶质细胞来源的细胞外囊泡的证据Xie, X. H., et al. (2022). "Hyper-inflammation of astrocytes in patients of major depressive disorder: Evidence from serum astrocyte-derived extracellular vesicles."
Brain Behav Immun 109: 51-62. IF=19.227
17.【综述】中山大学赵春顺等:利用工程免疫细胞和细菌作为癌症免疫治疗的药物载体Jiang, J., et al. (2023). "Harnessing Engineered Immune Cells and Bacteria as Drug Carriers for Cancer Immunotherapy."
ACS Nano.IF=18.027
18.南京中医药大学王若宁教授等:装载自组装纳米胶束的免疫外泌体穿过血脑屏障用于针对胶质母细胞瘤的化学免疫疗法Cui, J., et al. (2023). "Immune Exosomes Loading Self-Assembled Nanomicelles Traverse the Blood-Brain Barrier for Chemo-immunotherapy against Glioblastoma."
ACS Nano. IF=18.027有效的药物输送和预防术后复发是当前胶质母细胞瘤(GBM)治疗的重大挑战。药物输送不良主要是由于血脑屏障(BBB)的存在,而术后复发主要是由于GBM细胞对化疗药物的耐药性和免疫抑制微环境的存在。该研究制备了一种基于内源性外泌体的仿生纳米药物递送平台,无需靶向修饰即可有效靶向大脑,并共同递送纯药物纳米胶束和免疫佐剂,用于安全有效地针对GBM进行化学免疫治疗。受小分子自组装技术的启发,丹参酮IIA(TanIIA)和甘草酸(GL)是中药(TCM)信号转导抑制剂和转录激活剂3,自组装形成TanIIA-GL纳米胶束(TGM)。选择内源性血清外泌体包被纯药物纳米胶束,将Toll样受体9激动剂CpG寡核苷酸锚定在外泌体膜上,获得载有中药自组装纳米胶束的免疫外泌体(CpG-EXO/TGM)。结果表明,CpG-EXO/TGM可以结合血液中的游离转铁蛋白,延长血液循环,并在穿过BBB和靶向GBM细胞时保持完整的结构。在GBM微环境中,CpG-EXO/TGM的强抗GBM作用主要归因于两个因素:(i)GBM细胞的高效摄取和足够的细胞内药物释放以诱导细胞凋亡和(ii)树突细胞的刺激通过CpG寡核苷酸成熟和诱导肿瘤相关巨噬细胞极化以产生抗GBM免疫反应。进一步研究发现,CpG-EXO/TGM与替莫唑胺联用不仅能产生更好的疗效,还能预防术后复发。
19.复旦大学附属肿瘤医院陆嘉德教授、孔琳教授:肿瘤固有的YTHDF1通过促进MHC-I降解来驱动免疫逃避和对免疫检查点抑制剂的抵抗Lin, W., et al. (2023). "Tumor-intrinsic YTHDF1 drives immune evasion and resistance to immune checkpoint inhibitors via promoting MHC-I degradation."
Nat Commun 14(1): 265. IF=17.694鉴于其对免疫治疗反应的潜在影响,最近描述的RNA甲基化在调节免疫细胞浸润到肿瘤中的作用引起了人们的兴趣。YTHDF1是一种多功能且功能强大的m6A阅读器,但对其对免疫逃避的影响的了解有限。该研究发现肿瘤固有的YTHDF1驱动免疫逃避和免疫检查点抑制剂(ICI)抵抗。此外,YTHDF1缺乏会将冷肿瘤转化为反应性热肿瘤,从而提高ICI疗效。从机制上讲,YTHDF1缺陷会抑制溶酶体基因的翻译并限制主要组织相容性复合物I类(MHC-I)和抗原的溶酶体蛋白水解,最终恢复肿瘤免疫监视。此外,研究设计了一个系统,用于在体内将外泌体介导的CRISPR/Cas9递送至靶向YTHDF1,从而导致YTHDF1耗尽和抗肿瘤活性。研究结果阐明了肿瘤固有的YTHDF1在驱动免疫逃逸中的作用及其潜在机制。
20.南方医科大学白晓春教授、崔忠凯教授:外泌体释放通过处理过时的生物分子延缓衰老Zou, W., et al. (2023). "Exosome Release Delays Senescence by Disposing of Obsolete Biomolecules."
Adv Sci (Weinh): e2204826.IF=17.521
21.武汉大学陈刚教授等:小细胞外囊泡运输和miRNA释放动力学的实时剖析Xia, H. F., et al. (2023). "Real-Time Dissection of the Transportation and miRNA-Release Dynamics of Small Extracellular Vesicles."
Adv Sci (Weinh): e2205566. IF=17.521
22.华中科技大学:通过重编程肿瘤微环境和抑制MAPK通路治疗小鼠脑转移的工程微粒Lu, L., et al. (2023). "Engineered Microparticles for Treatment of Murine Brain Metastasis by Reprograming Tumor Microenvironment and Inhibiting MAPK Pathway."
Adv Sci (Weinh): e2206212. IF=17.521
23.复旦大学生物医学研究院商珞然教授等:液滴限制磁性自组装的旋转结构彩色纺锤体Chen, H., et al. (2023). "Rotary Structural Color Spindles from Droplet Confined Magnetic Self-Assembly."
Adv Sci (Weinh): e2207270. IF=17.521
24.南开大学刘定斌、许晨团队:粪便中的细胞外囊泡:一种新型结直肠癌标志物Zhang, Z., et al. (2023). "Identification of faecalextracellular vesicles as novel biomarkers for the non-invasive diagnosis and prognosis of colorectal cancer."
J Extracell Vesicles 12(1): e12300. IF= 17.337前期报道:https://www.exosomemed.com/13173.html
25.上海大学转化医学研究院/长海医院:基于骨靶向外泌体治疗炎症性肠病骨丢失Guo, J., et al. (2023). "Exosome-based bone-targeting drug delivery alleviates impaired osteoblastic bone formation and bone loss in inflammatory bowel diseases."
Cell Rep Med 4(1): 100881. IF= 16.988前期报道:https://www.exosomemed.com/13155.html
26.南方科技大学生物医学工程系蒋兴宇教授:用内部和外部工程化的外泌体对肿瘤相关巨噬细胞进行原位重编程Zhang, L., et al. (2023). "In Situ Reprogramming of Tumor-Associated Macrophages with Internally and Externally Engineered Exosomes."
Angew Chem Int Ed Engl. IF= 16.823
27.复旦大学:富含netrin-1 modRNA的工程外泌体通过减轻炎症和细胞焦亡促进脊髓损伤中的轴突生长Lu, X., et al. (2023). "Engineered exosomes enriched in netrin-1 modRNA promote axonal growth in spinal cord injury by attenuating inflammation and pyroptosis."
Biomater Res 27(1): 3. IF= 15.863
28.香港中文大学:生物活性玻璃赋能间充质干细胞来源的细胞外囊泡调控M2型巨噬细胞和再血管化以促进肌腱再生Xu, H., et al. (2023). "Bioactive glass-elicited stem cell-derived extracellular vesicles regulate M2 macrophage polarization and angiogenesis to improve tendon regeneration and functional recovery."
Biomaterials 294: 121998.IF= 15.304前期报道:https://www.exosomemed.com/13223.html
29.第四军医大学:通过工程化细胞外囊泡有效递送GSDMD-N mRNA诱导细胞焦亡以增强免疫疗法Xing, Y., et al. (2023). "Efficient Delivery of GSDMD-N mRNA by Engineered Extracellular Vesicles Induces Pyroptosis for Enhanced Immunotherapy."
Small: e2204031. IF= 15.153
30.山东大学刘宏教授等:纳米材料在基于干细胞的心脏修复和再生治疗中的应用Qiu, J., et al. (2023). "Application of Nanomaterials in Stem Cell-Based Therapeutics for Cardiac Repair and Regeneration."
Small: e2206487.IF= 15.153篇幅有限,仅介绍其中少数文献。如需全部文献列表及部分文章原文,请至外泌体之家论坛同名贴下载。(搜索:外泌体之家;或网址:www.exosome.com.cn)以上,1月份国内细胞外囊泡/外泌体领域研究进展的月总结整理。
感谢大家关注!愿有所收获。下个月见!
外泌体资讯网 国内外泌体领域进展总结(2023年1月)