Human Reproduction 上海交通大学医学院附属仁济医院团队:细胞外囊泡在睾丸的新作用
睾丸是哺乳动物重要的生殖及内分泌器官,其功能异常通常导致男性不育症、性功能障碍等。两者发病率高,但目前相当一部分患者病因不明。细胞外囊泡(Extracellular vesicle, EV)在多种疾病中发挥细胞间通讯、功能调控等作用,然而其在睾丸中的角色几乎未被发掘。对睾丸内EV的研究可能有助于尚未揭开面纱的多种男科疾病的病因、诊断、治疗及预后。
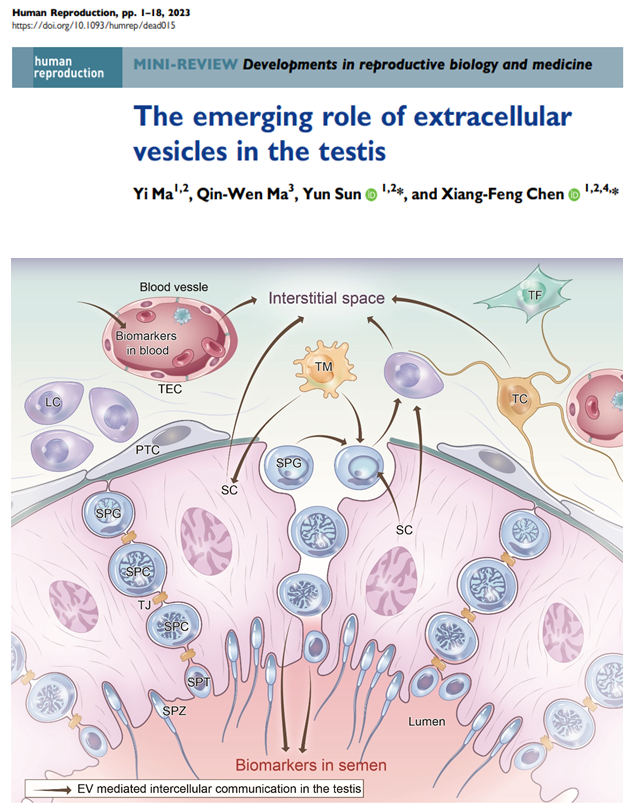
2月4日,上海交通大学医学院附属仁济医院生殖中心陈向锋团队在总结既往本团队的相关成果(Endocrinology、Andrology、Molecular Human Reproduction)及细胞外囊泡在睾丸的新进展后,以Review article的形式在Human Reproduction在线发表了题为“The emerging role of extracellular vesicles in the testis”的论文,图形摘要如下。论文第一作者为上海交通大学医学院附属仁济医院主治医师马逸,通讯作者为主任医师孙赟、陈向锋教授。该论文受到国家自然科学基金面上项目(81871199,马逸),上海交通大学医学院高水平创新研究团队(SHSMU-ZLCX20210200,马逸)的资助。
图1. 图形摘要。EV介导睾丸中的细胞间通讯。LC:间质细胞;PTC:管周肌样细胞;SC:支持细胞;SPC:精母细胞;SPG:精原细胞;SPT:精子细胞;SPZ:精子;TC:telocyte;TEC:睾丸内皮细胞;TF:睾丸成纤维细胞;TJ:紧密连接;TM:巨噬细胞。
该团队首先总结了睾丸的细胞结构和互作(详见全文及下图):
图2. 睾丸组织。睾丸横截面,显示曲细精管和间质的位置
在曲细精管中,处于不同成熟阶段的生殖细胞嵌入支持细胞(SC)中。管腔中显示精子。曲细精管被管周肌样细胞(PTCs)包围。在间质,存在血管、间质细胞(LC)、telocyte(TC)、成纤维细胞(TF)、巨噬细胞(TM)和一些其他免疫细胞。SPC:精母细胞;SPG:精原细胞;SPT:精子细胞;SPZ:精子;TEC:睾丸内皮细胞;TF:睾丸成纤维细胞;TJ:紧密连接。
随后,简要介绍了EV的作用模式(下图):
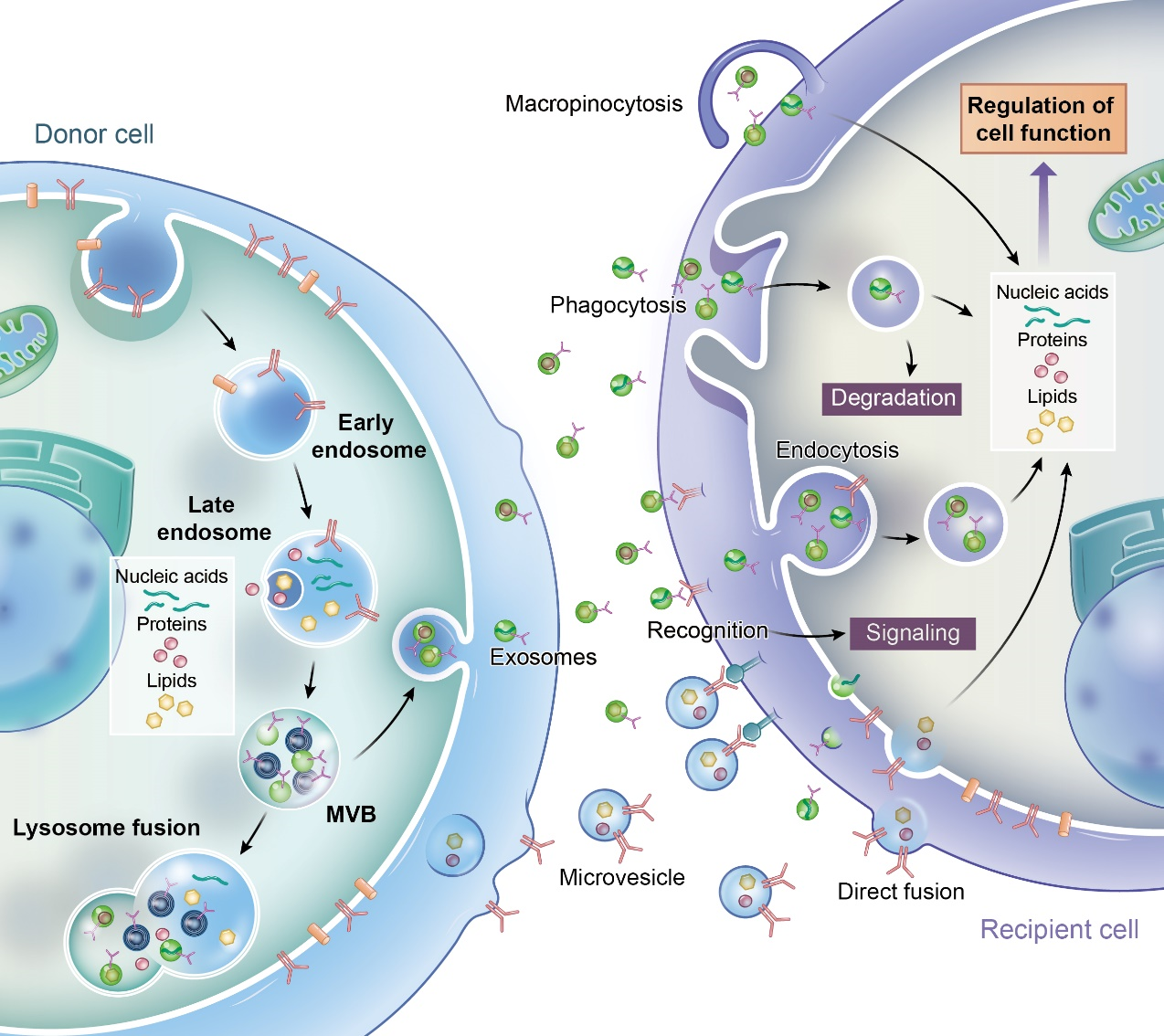
图3. EV的生物发生、释放和内化
左图:外泌体和微囊泡的生物发生和释放的简化描述。右图:EVs可以通过多种途径被靶细胞内化,包括大吞噬、吞噬、内吞和直接融合,囊泡内容物可以被释放或降解。EVs也可以与受体细胞表面结合并启动信号通路。MVB:多泡体。
随后,详细介绍了睾丸内细胞的EV互作(见下图及图注)。此外,睾丸细胞释放的EVs可以在精浆中检测到,这使其成为反映睾丸功能和疾病状态的潜在生物标志物。精浆中的睾丸EVs也可能通过调节精子RNA来调控女性生殖道以促进受孕,甚至影响早期胚胎发育。
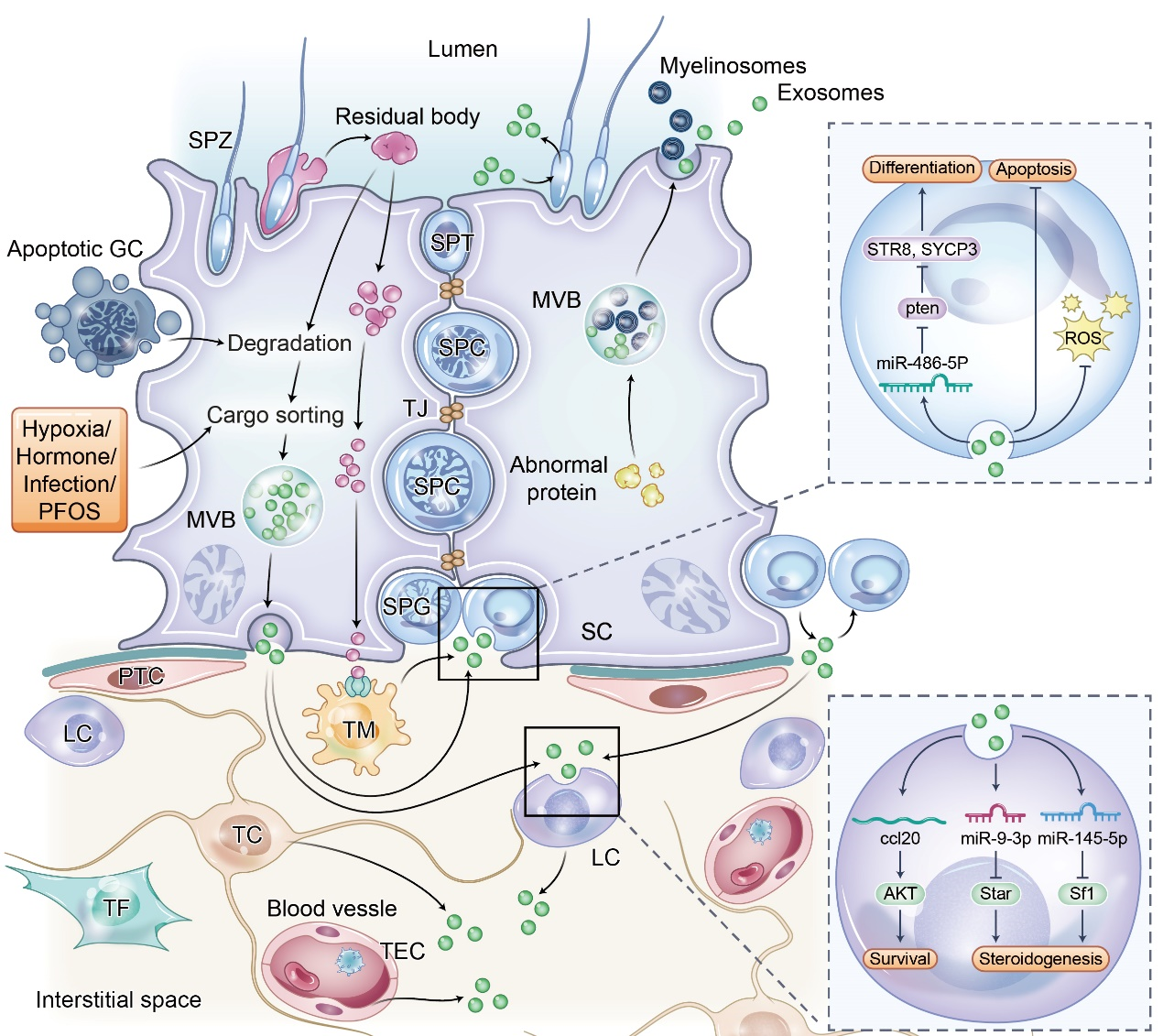
图4. EV介导睾丸中的细胞间通讯
在曲细精管中,支持细胞(SCs)中外泌体的内容物可由缺氧、激素、感染和PFOS调节。凋亡的生殖细胞和残余体可以被SC吞噬和降解,一些内容物可以通过EV释放到间质空间,EV可能参与将抗原输送到睾丸巨噬细胞(TM)以实现免疫耐受。异常蛋白可以被SC释放的EV去除。SC释放的外泌体可以通过miR-486-5p促进精原干细胞(SSC)的分化。SC来源的外泌体还可以到达间质中的间质细胞(LC),通过Ccl20刺激细胞存活,并通过miR-9-3p和miR-145-5p抑制类固醇生成。未分化的A精原细胞可以释放外泌体并抑制SSC的增殖。精子可以从管腔摄取/释放EVs。在睾丸间质中,EVs可由内皮细胞、TM、端细胞和LC分泌。从TMs中分离的外泌体可以保护精原细胞免受辐射损伤。MVB:多泡体;PFOS:全氟辛烷磺酸;PTC:管周肌样细胞;SPC:精母细胞;SPG:精原细胞;SPT:精子细胞;SPZ:精子;TC:telocyte;TEC:睾丸内皮细胞;TF:睾丸成纤维细胞;TJ:紧密连接。
EV代表了睾丸中的一种新型细胞间信使,详细了解睾丸EV的作用可能有助于发现男性不育的新机制,并有助于开发治疗不育男性的新诊断和治疗策略。
参考文献:
The emerging role of extracellular vesicles in the testis, Hum Reprod. 2023 Feb 2;dead015. doi: 10.1093/humrep/dead015.