细胞外囊泡(EV)在各种疾病中的诊断和治疗应用越来越受到关注,这些天然纳米颗粒受益于良好的安全性和独特的生物分布能力,比人工合成的其他治疗载体在药物传递上更具有优势。然而EV的广泛使用受到技术缺陷和生物学知识差距的限制,这些缺陷未能揭示它们的异质性,因此深入了解其生物成因对于释放EV全部治疗潜力至关重要。来自瑞典卡罗林斯卡学院的研究人员发表综述,总结了各类EV亚型的特征及货物分选机制,并提出了通过控制EV生物发生和货物分选途径实现工程化EV改造,最终用于疾病治疗。相关内容以“Exploiting the biogenesis of extracellular vesicles for bioengineering and therapeutic cargo loading”为题于2月20日在线发表在国际学术期刊Molecular Therapy杂志上。
细胞外囊泡(EVs)是由所有细胞分泌的天然膜包裹的纳米颗粒,是细胞间通信的重要介质,EV以蛋白质、脂质、核酸、甚至细胞器的形式向周围或远处的细胞传递信息。因此,EV不仅发挥生理功能,而且发挥病理功能,这使它们成为有吸引力的治疗靶点。相应的,EV及其内容物可以作为诊断生物标志物,主要用于癌症和神经退行性疾病。由于其独特的生物分布能力、多功能性和免疫耐受性,EV正越来越多地被用作药物输送工具。然而,EV的广泛应用在一定程度上受到EV异构性相关的技术挑战限制,这些问题包括从产生细胞的选择到EV分离和表征的方法。此外,另一个重要的技术限制是缺乏依赖于EV生物成因或组成的可靠的货物装载策略。
传统意义上,EV根据其来源分为三种类型的囊泡:(1)外泌体(50-200 nm),形成于内溶酶体系统或质膜;(2)微泡或外切体(0.1-1 μm),直接从质膜上出芽;(3)死亡细胞产生1 ~ 5 μm的凋亡小体。在体内,由于巨噬细胞可以识别和清除凋亡小体,因此主要是外泌体和微囊泡具有治疗意义,研究人员将这两种囊泡作为综述的重点。到目前为止,该领域一直在努力从物理上分离这两类EV,因为二者在尺寸和组成上重叠。这两种EV甚至在生物发生途径上也有共同之处,这使得寻找相互排斥的独立特性来进行两种囊泡表征变得更加复杂。然而,由于技术的进步,人们对控制其生物发生和决定其组成的机制了解得越来越多。此外,了解潜在的过程对于利用EV作为生物疗法至关重要。
在这篇综述里,研究人员探讨了如何利用EV进行生物工程化的知识,将治疗性蛋白质或核酸装载到EV上。研究人员总结了超过75篇文章,并讨论了他们在外泌体和微囊泡的形成和组成方面的发现,揭示了可能是货物依赖的多种途径所诱导。研究人员进一步确定了自然EV货物装载的关键调控因素,并讨论了如何将这些内容应用到开发工程化EV生物疗法中。
研究人员认为,在过去的几十年里,EV领域发生了巨大的变化,从被视为垃圾到现在被视为细胞间通信的重要介质。由于具有跨越细胞和生物屏障转移大分子的独特能力,EV被认为是药物递送领域的新星。值得注意的是,EV在更好的疗效、肝外给药和低毒性方面优于大多数合成给药载体。总的来说,这些发展导致了各种临床试验的开始,使用EV作为治疗干预的明星产品。有趣的是,一些临床试验报告了EV的治疗活性,最重要的是,总体上没有观察到显著毒性。这些正在进行的1期临床试验的报告是非常有希望的推动临床应用,希望很快会进入到2/3期的安慰剂对照设置研究中。
然而,尽管存在大规模和良好生产规范(GMP)级细胞培养技术,EV的临床制造仍然是一个未解决的领域。这主要是由于缺乏更新的技术,无法在不影响其完整性和生物物理特性的情况下大规模生产高纯度EV。从细胞外环境中纯化EV的一个特殊挑战是富集EV的同时还得到大量凋亡小体、蛋白聚集物和核糖核酸复合物,这些杂质表现出与EV相似的特征,如大小或密度,因此使用当前技术可能很难与EV分开。另一个在很大程度上尚未解决的障碍是,在保留EV治疗效果的同时,获得GMP/良好临床规范(GCP)级存储条件。获得关于EV稳定性的更深入的知识,以及开发用于富集特定EV种群的纯化技术,将是未来实现从实验室顺利转化到临床的关键。
该综述的内容提纲:
- EV的生物成因
- 外泌体和微囊泡的基本信息
- 货物(蛋白质、RNA、DNA)如何被分选进入EV
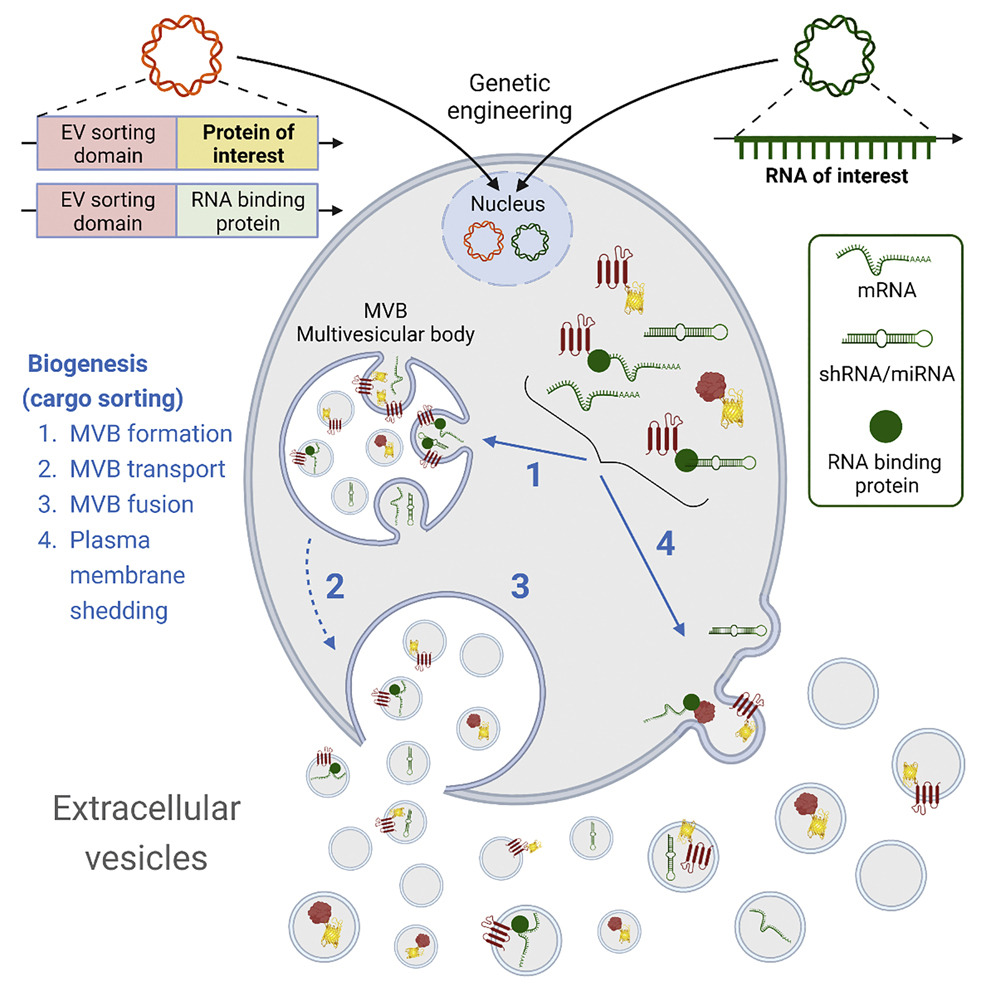
- 劫持EV生物发生途径用于生物治疗货物装载
- 非遗传源性细胞修饰用于内源性EV货物装载
参考文献:Exploiting the biogenesis of extracellular vesicles for bioengineering and therapeutic cargo loading. Mol Ther. 2023 Feb 20:S1525-0016(23)00076-X.