迄今为止,结直肠癌(CRC)衍生的细胞外囊泡(EVs)对肝脏转移前微环境(PMN)的影响仍不完全清楚。
2023年3月6日,四川大学王自强及韩俊宏教授共同通讯在Signal Transduction and Targeted Therapy(IF=38)在线发表题为“Colorectal cancer-derived extracellular vesicles induce liver premetastatic immunosuppressive niche formation to promote tumor early liver metastasis”的研究论文(2023 Mar 6;8(1):102),该研究表明结直肠癌来源的细胞外囊泡诱导肝脏转移前免疫抑制微环境的形成,促进肿瘤早期肝转移。
作者前期结果已证实了CRC衍生EVs有助于肿瘤早期肝转移,因此作者推测EVs诱导肝脏PMN转化为免疫抑制微环境。越来越多的证据证实,髓源性抑制细胞(MDSCs)是病理条件下免疫反应的主要调节因子,也是肿瘤进展的关键因素。这项研究分析了肠癌源性EVs预处理前后肝脏PMN中MDSCs的演变情况,结果发现EVs预处理后显著增加了肝脏PMN中的CD11b+Gr1+细胞。既往研究中,MDSCs通过抑制T细胞功能促进肿瘤免疫逃逸。然而,募集的MDSCs诱导肝脏PMN进入免疫抑制状态的机制仍有待阐明。作为先天免疫系统的重要细胞组成部分,自然杀伤细胞(NK)在肿瘤免疫逃逸的早期监控中起着至关重要的作用。作者首先运用动物模型实验表明,肿瘤细胞逃避了免疫系统的早期监视,这提示NK细胞在EVs预处理后细胞毒性降低。此外,流式细胞实验进一步证实,NK细胞的主要功能活化受体NKG2D的表达在EVs预处理后显著降低,尽管NK细胞的数量没有变化。进一步通过回复实验证实募集的MDSCs和原本肝脏PMN中驻留的NK细胞在肝PMN重塑中均发挥重要作用。总的来说,作者的研究结果表明,CRC衍生的EVs通过募集MDSCs在诱导肝脏免疫抑制PMN的形成中具有重要作用,并且MDSCs抑制了NK细胞的功能,导致免疫监测失败。
为了进一步探索EVs如何启动次序性事件诱导肝脏PMN形成,作者研究了EVs在体内的分布。结果发现EVs主要积聚在肝脏中,并被肝星状细胞(HSCs)摄取;进一步诱导肝星状细胞转化为CAFs,CAFs分泌纤维连接蛋白及趋化因子CXCL12重塑肝脏PMN。作者进一步通过RNA-seq证实HSCs摄取EVs后趋化因子信号通路显著激活。作者团队之前的研究表明,携带Tgf-β1的胃癌衍生EVs重塑腹膜PMN并促进肿瘤腹膜转移。在这项研究中,作者同样证实Tgf-β1是诱导HSCs转化为CAFs表型的EVs的主要成分。体外共培养表明CAFs亦增强了肿瘤迁移,并且Tgf-β1抑制剂消除了这种作用。
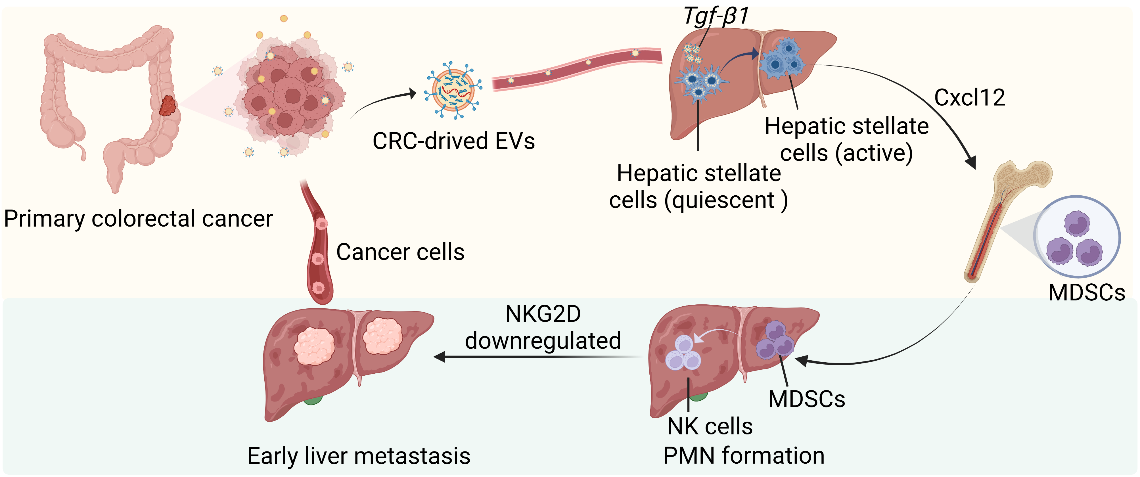
综上所述,研究者首次系统性阐述了肠癌源性EVs重塑肝脏转移前免疫抑制性微环境次序性事件,即携带Tgf-β1的CRC衍生的EVs激活HSCs趋化因子信号通路,诱导HSCs转化为CAFs表型。HSCs激活后,MDSCs进一步被募集到肝脏PMN中,通过下调NKG2D的表达来抑制NK细胞的细胞毒性。最后,CRC衍生的EVs重塑肝脏PMN并促进肿瘤肝转移。
参考文献:
Colorectal cancer-derived extracellular vesicles induce liver premetastatic immunosuppressive niche formation to promote tumor early liver metastasis, Signal Transduct Target Ther. 2023 Mar 6;8(1):102. doi: 10.1038/s41392-023-01384-w.
外泌体资讯网 Signal Transduct Target Ther | 四川大学王自强/韩俊宏:结直肠癌来源的EVs促进肿瘤早期肝转移