乳腺癌是女性癌症相关死亡的主要原因,三阴性乳腺癌(TNBC)约占所有乳腺癌的20%,具有高度侵袭性的临床过程,在年轻女性中更普遍。晚期TNBC的标准治疗方法是化疗,但反应短暂、复发率高。近年来,癌症纳米医学的进展提供了创新的治疗选择,因为纳米制剂在克服传统疗法缺陷方面发挥了重要作用。来自葡萄牙波尔图大学的研究人员发表专题性综述,总结了纳米医学领域治疗TNBC的最新进展,包括新型纳米颗粒、外泌体以及杂交治疗制剂,并讨论了它们在未来临床应用中的缺点和挑战。相关内容以“Special Issue: Nanotherapeutics in Women's Health Emerging Nanotechnologies for Triple-Negative Breast Cancer Treatment”为题于3月28日在线发表在国际纳米材料领域旗舰期刊Small杂志上。
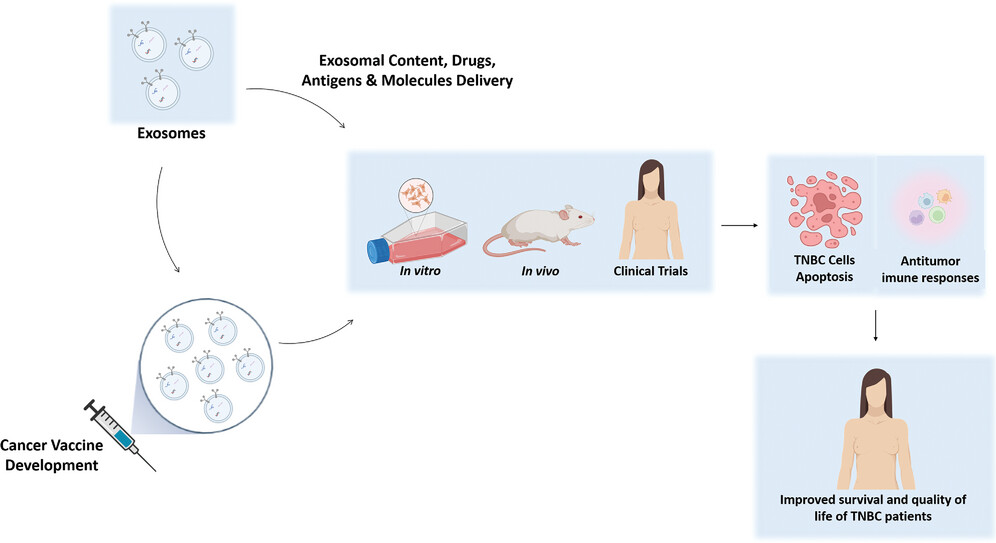
图:基于外泌体的肿瘤疫苗将用于TNBC治疗。外泌体能够将它们的内容物、装载的药物、抗原和分子传递到TNBC细胞,并通过它们的细胞表面标记与它们相互作用。此外,外泌体可以用于或被修饰以开发肿瘤疫苗。因此,外泌体可以在TNBC的体外和体内模型中进行测试,如果疗效和安全性得到保证,也可以在临床试验中进行测试。外泌体治疗使得TNBC细胞凋亡并促进抗肿瘤免疫反应。这种方法改善了TNBC患者的治疗,提高了他们的生存率和生活质量。
在过去20年里,男性和女性的预期寿命均有所增加,这要归功于自21世纪以来世界各地经济和社会稳定程度的提高。对死亡原因的全面研究表明,女性(以及男性)预期寿命的延长主要是由于心血管疾病患者预防和治疗的改善。全世界女性最大的死亡原因是心血管疾病(如中风和冠心病)和癌症,其中最常见的是乳腺癌(24.5%)、结直肠癌(9.4%)、肺癌(8.4%)和宫颈癌(6.5%)。乳腺癌仍然是女性癌症相关死亡的主要原因,2020年报告的新病例超过2,260,000例,占全球诊断出的所有癌症的24.5%(如果包括女性和男性总计,则比例为11.7%),并导致684 996例死亡,因此,如果不考虑性别,乳腺癌是全球癌症总体相关死亡的第五大原因。乳腺癌是154个国家中女性最常诊断的癌症类型,其中中国和美国是两个主要国家,分别占全球诊断病例的17.6%和11.2%。此外,据估计,在2021年,美国女性诊断出的癌症中约有三分之一与乳腺癌相关:在女性诊断出的927910例癌症中有281550例是乳腺癌。
根据分子亚型分类,乳腺癌可分为管腔型(luminal)A、管腔型B、人表皮生长因子受体2 (HER2)型和雌激素(ER)/孕激素受体(PR)阳性等几类。然而,约20%的乳腺癌不表现出这些特征,缺乏HER2、ER和PR的表达,因此被称为三阴性乳腺癌(TNBC)。TNBC是一种特别具有侵袭性的肿瘤亚型,对激素治疗没有反应,在年轻女性中更常见。目前TNBC的治疗方案根据亚型和肿瘤分期进行手术和常规治疗,包括辅助治疗或新辅助治疗,即化疗、放疗(RT)和免疫治疗。然而,约40%的TNBC肿瘤会复发,出现耐药性和转移特征,转移是患者死亡的最大原因(80-90%)。事实上,在美国,TNBC患者的5年总生存率为77%,而其他乳腺癌亚型患者的5年总生存率为93%。此外,化疗和放疗经常对周围的健康组织造成损害和不良的副作用,这甚至增加了更多的危害性。重要的是,缺乏明确的和通用的TNBC治疗分子靶点使患者死于这种疾病的风险更高。总之,这揭示了迫切需要为TNBC患者开发新的治疗方法。
在过去的30年里,肿瘤纳米疗法的发展和应用已经克服了传统疗法留下的固有缺点。纳米技术具有巨大的潜力来打破这些限制,通过避免有效物质降解和增强药物性质(如溶解度、稳定性和循环半衰期),改善抗癌药物的生物分布,通过更有效和更有选择性地将它们输送到肿瘤部位。纳米粒子(NPs)和其他纳米载体类型已被用于抗癌药物和一些治疗分子(如miRNA)的递送,提高了它们的治疗效率,同时降低了它们的全身毒性。一些纳米药物已经被美国食品和药物管理局(FDA)批准用于乳腺癌患者的治疗,包括脂质体(Doxil)和白蛋白结合的NP制剂(Abraxane)。此外,其他脂质体和聚合胶束正在进行化疗药物输送的临床试验。
由于外泌体体积小、装载物质或组成的可调节性、细胞或组织的趋向性,外泌体在肿瘤中比健康组织更能积聚,因此具有巨大的治疗潜力。由于这些特点,再加上外泌体具有内源性来源,具有低免疫原性以及保护毒性药物的体循环驻留,也可用于增强药物对肿瘤的输送。此外,外泌体本身的内容物可能有助于重编程受体细胞,即免疫细胞,从而赋予外泌体的免疫调节潜力,可使乳腺癌患者受益。所有这些特征都促进了新的外泌体和基于NP的TNBC治疗策略的开发,其中有大量的外泌体疗法正在进行临床前和临床试验,甚至获得批准。
在这篇综述里,研究人员总结了纳米医学领域治疗TNBC的最新进展,包括基于NP和外泌体的新型治疗试剂以及杂交系统。同时讨论了NP和外泌体在改善常规肿瘤治疗(包括化疗、RT和免疫治疗)方面的潜力,以及未来临床应用面临的挑战,重点介绍了正在进行的基于纳米医学的临床试验,对TNBC患者临床相关性进行了综合性总结。
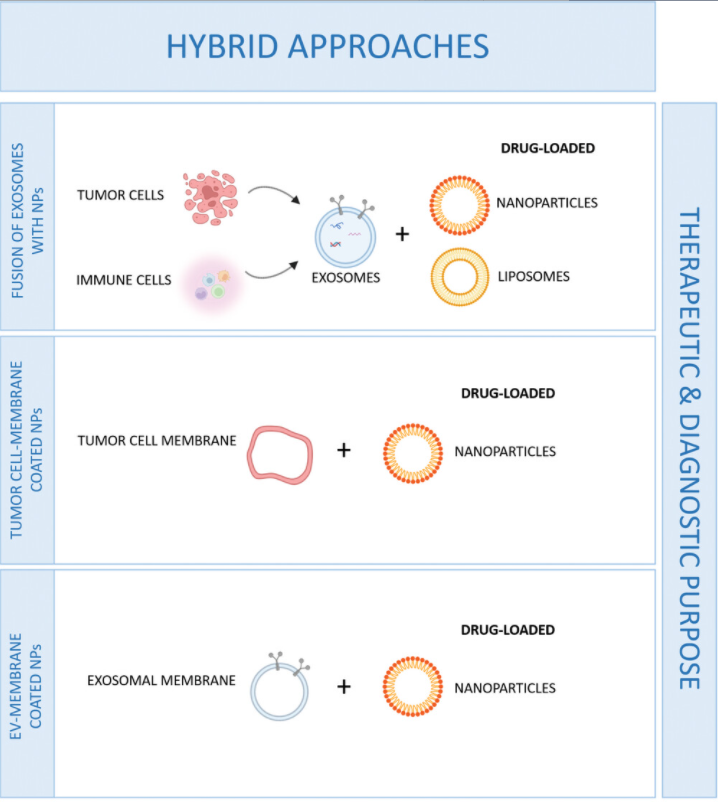
图:结合纳米颗粒、外泌体和外泌体/肿瘤细胞膜用于TNBC治疗和诊断目的的杂交策略。肿瘤细胞或免疫细胞来源的外泌体可以与载药纳米颗粒或脂质体融合。此外,肿瘤细胞膜或外泌体膜可用于载药纳米颗粒的包被。这些方法可以改善TNBC的治疗方案,促进了TNBC的靶向和协同治疗潜力,增强了它们的疗效。
参考文献:Special Issue: Nanotherapeutics in Women's Health Emerging Nanotechnologies for Triple-Negative Breast Cancer Treatment. Small. 2023 Mar 28:e2300666.