细胞外囊泡(extracellular vesicle,EV)是一种由磷脂双分子层包裹的结构,通常携带了母细胞的分子信息(如蛋白质、脂质、代谢产物和核酸),可以指示许多疾病的存在、发展和治疗效果,被认为是最有临床潜力的液体活检标志物之一。然而,由于其高度的异质性,在生物样本中的浓度较低,且常与高丰度的污染物(如脂蛋白)共存, EV的高产率、高纯度分离仍然缺乏有效的方法。因此,亟待开发一种无需复杂处理过程和昂贵仪器的EV分离平台,推动其应用于诊断和治疗的临床转化。
近日,南开大学化学学院刘定斌课题组开发了一种基于磷脂膜特异性识别的EV快速富集方法,并结合蛋白质组学发现了一组潜在的结肠癌生物标志物,研究成果以“Reversible zwitterionic coordination enables rapid, high-yield, and high-purity isolation of extracellular vesicles from biofluids”为题发表在Science Advance上(2023,9,eadf4568)。该研究得到国家重点研发计划项目(no. 2019YFA0210100),国家自然科学基金项目(no. 22174072, no. 21977053,no. 22107053),南开大学中央高校基本科研业务费专项资金(no. 2122018165)的资助。南开大学化学学院李强博士为第一作者,刘定斌教授为论文的唯一通讯作者。
该团队发现,EV 膜表面的磷脂酰胆碱(phosphatidylcholine, PC)与其电荷方向相反的胆碱磷酸(choline phosphate, CP)可通过静电作用形成多价配位结构,且结合力与CP末端的取代基密切相关。基于此,这项工作开发了一种CP 修饰的磁性水凝胶颗粒(简称MB@CP),CP 与EV 膜表面的PC 通过分子间静电作用牢固地结合在一起,从而在外加磁场条件下将EV 高效地从复杂样本中提取出来(图1)。而其他杂质组分(细胞及其碎片通常在临床样本前处理时已去除掉)由于不含有PC 结构,因此不会被MB@CP 捕获。更重要的是,CP-PC 配位键可在42°C断裂,从而将EV从MB@CP 上释放下来,无需加入额外试剂,保障了EV 的生物活性。
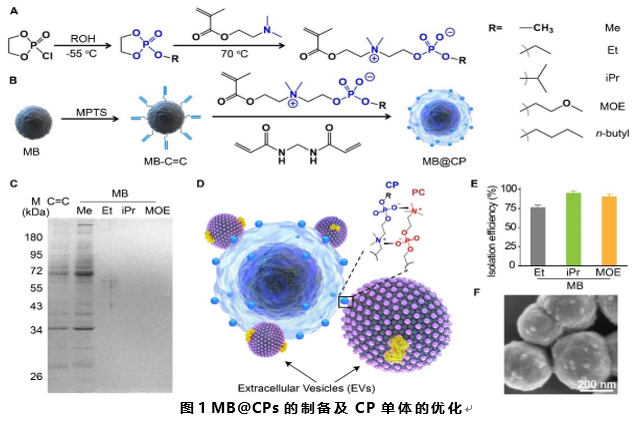
经过一系列筛选,发现异丙基取代的CP功能化磁球(MB@CP-iPr)具有最高的富集效率(96%)。透射电镜(TEM)和纳米示踪分析(NTA)表明,富集到的EV具有经典的囊泡形状和良好的单分散性。此外,划痕实验和荧光共聚焦成像结果也证明了富集到的EV保持了良好的生物学活性,RNA的定量结果也证明其结构完整性,展现了本策略相对于传统的超速离心分离(UC)的巨大优势(图2)。
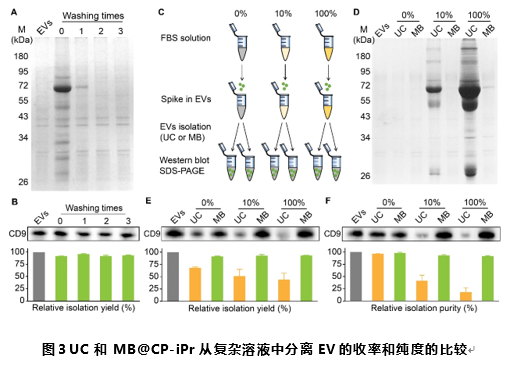
为了确定MB@CP-iPr在复杂环境中捕获EV的分离效率,研究者制备了人工生物流体样品。通过SDS-聚丙烯酰胺凝胶电泳(SDS-PAGE),验证了其优异的抗污染效果(仅富集到超微量的FBS蛋白)和极高的捕获效率;通过Western blotting分析,验证了即使在100% FBS条件下,该策略分离EV的纯度和收率也可达到90%以上(图3)。
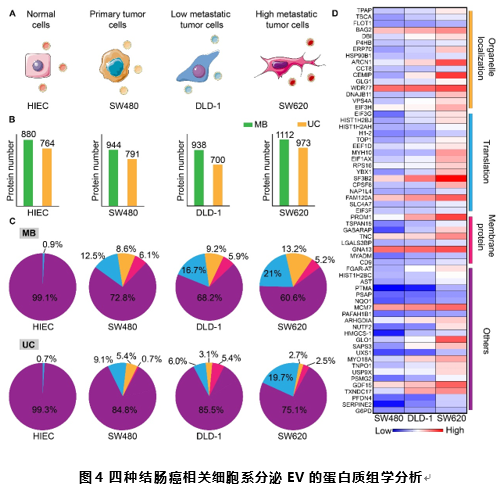
通过无标记定量蛋白质组学分析EV蛋白,并通过基因本体富集分析,发现随着结直肠癌细胞系侵袭性的增加,EV中RNA翻译和细胞器定位的蛋白表达水平大幅上调,而基于UC分离的EV不存在这样的正相关性。此外,通过对EV差异表达蛋白的计算,确定一系列潜在的结肠癌EV标志物。这些结果表明,MB@CP-iPr与组学结合有望发现更多新的癌症标志物(图4)。
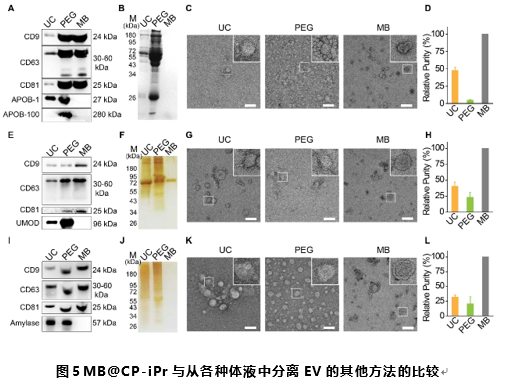
为了验证MB@CP能从不同体液中高纯度和高产量地分离出EV的能力,他们将其与常用EV分离方法(UC和PEG沉淀)进行对比,通过Western blot、SDS-PAGE和TEM等基本方法对相对纯度进行了鉴定。结果表明,UC和PEG从血清中分离出的EV的相对纯度分别为47.47±4.67%和4.86±0.79%(将MB@CP-iPr的富集纯度设置为100%,图5D)。从尿液和唾液样本中分离出的EV也得到了类似的结果(图5H和5L)。
综上,该研究提出了一种快速、高产率、高纯度分离EV的有效策略。这种可逆两性离子配位的EV磁分离不依赖于复杂的操作步骤与昂贵设备,且易于产品化,为EV的基础研究和临床转化应用开辟了道路。当然,该研究中新发现的生物标志物还应通过大型队列开展临床研究,证实其有效性。该团队将采用更多样化的体液,如泪液、脑脊液、胆汁、母乳等,证明MB@CPs在EV分离中的普适性,以满足不同环境下EV研究和应用的需求。
通讯作者简介

刘定斌,国家海外人才计划入选者。2006年本科毕业于兰州大学,2012年博士毕业于国家纳米科学中心(师从蒋兴宇教授),随后在美国国立健康研究院(师从Shawn Chen教授)开展疾病检测研究;2014年加入南开大学化学学院,任研究员/教授。近年来,已以通讯作者在包括PNAS、Sci. Adv.、J. Extracell. Vesicles、JACS、JACS Au、Angew. Chem.、Nano Lett.等国际著名期刊上发表论文90余篇,已获授权专利十余项,并实现了部分专利的成果转化。主持1项国家重点研发计划课题和多项国家自然科学基金项目;受邀担任《Nanotheranostics》副主编/编委、《Targets》编委、《高等学校化学学报》青年编委、中国研究型医院学会细胞外囊泡研究与应用专业委员会委员、中国生物材料学会体外诊断分会委员。
参考文献:
Reversible zwitterionic coordination enables rapid, high-yield, and high-purity isolation of extracellular vesicles from biofluids, Sci Adv. 2023 Apr 14;9(15):eadf4568. doi: 10.1126/sciadv.adf4568. Epub 2023 Apr 14.