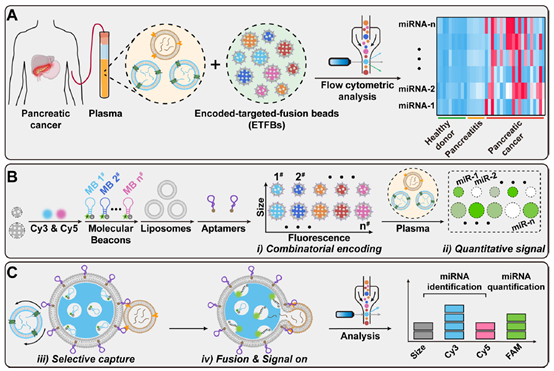
肿瘤来源细胞外囊泡(tEVs)携带的miRNAs(tEV-miRNAs)被认为是胰腺癌癌症早期诊断和治疗监测的重要标记志物。然而,目前检测EVs中miRNA的方法仍存在一些问题,如EVs分离过程中的耗时操作、EV的裂解等易导致EVs损失及miRNA降解。相比之下,膜融合策略可以直接将检测试剂递送至EVs内部,避免了样品处理过程中的偏差、污染和损失。同时,膜融合策略可以利用肿瘤特异性识别分子,实现靶向识别和融合tEVs,以选择性地检测tEVs中的miRNA。然而,膜融合策略尚未用于tEV-miRNA的多重检测,因此仍需要进一步研究。
近日,上海交通大学医学院吴玲玲副研究员团队,提出了一种编码融合策略(encoded fusion strategy),通过制备编码-靶向-融合微球(encoded-targeted-fusion beads, ETFBs),对tEVs进行靶向捕获与融合;基于微球的尺寸-荧光组合编码,及内部包埋的分子信标(MBs),同时检测多种tEVs的miRNAs,实现对胰腺癌的准确诊断。相关成果以“Encoded Fusion-Mediated MiRNA Signature Profiling of Tumor-Derived Extracellular Vesicles for Pancreatic Cancer Diagnosis”为题发表在国际期刊Anal. Chem.上(DOI: 10.1021/acs.analchem.3c00929)。
不同miRNAs的MBs通过脂质体负载到编码微球内部,并在微球表面形成支撑磷脂双分子层(SLBs),最后在SLBs上修饰靶向肿瘤标志物EpCAM的核酸适体,构建编码-靶向-膜融合载体,ETFBs。此策略利用膜融合后miRNA与MBs的杂交反应引起的FAM染料荧光恢复信号进行miRNA定量,同时利用微球的尺寸与荧光组合编码进行miRNAs的种类鉴定,实现对tEV中的多种miRNAs实现定量检测。(图1)
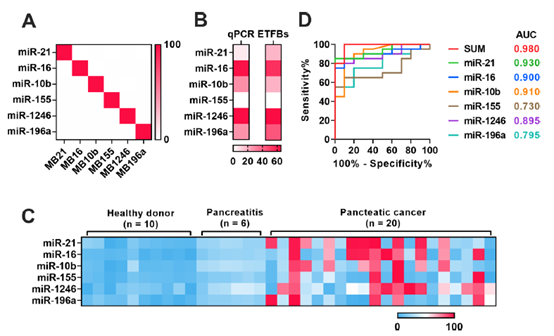 图2 编码融合策略实现对胰腺癌的精确诊断
图2 编码融合策略实现对胰腺癌的精确诊断在对胰腺癌患者临床血浆样本的检测中,6种tEV-miRNAs的综合诊断准确率为98%,显著高于单一tEV-miRNAs的诊断准确率(图2)。表明这种编码融合策略在tEV-miRNA的多重分析方面具有巨大的潜力,为癌症诊断和筛查提供了新的途径。
该工作得到上海交通大学医学院附属仁济医院胆胰外科主任、上海市肿瘤研究所所长刘颖斌教授,扬州大学胡效亚教授及舒韵副教授的大力支持;得到国家自然科学基金、国家重点研发计划、上海地方高水平大学创新研究团队等项目的资助支持。
外泌体资讯网 Anal. Chem.|吴玲玲研究团队:编码融合介导的肿瘤来源细胞外囊泡的miRNA特征分析用于胰腺癌诊断