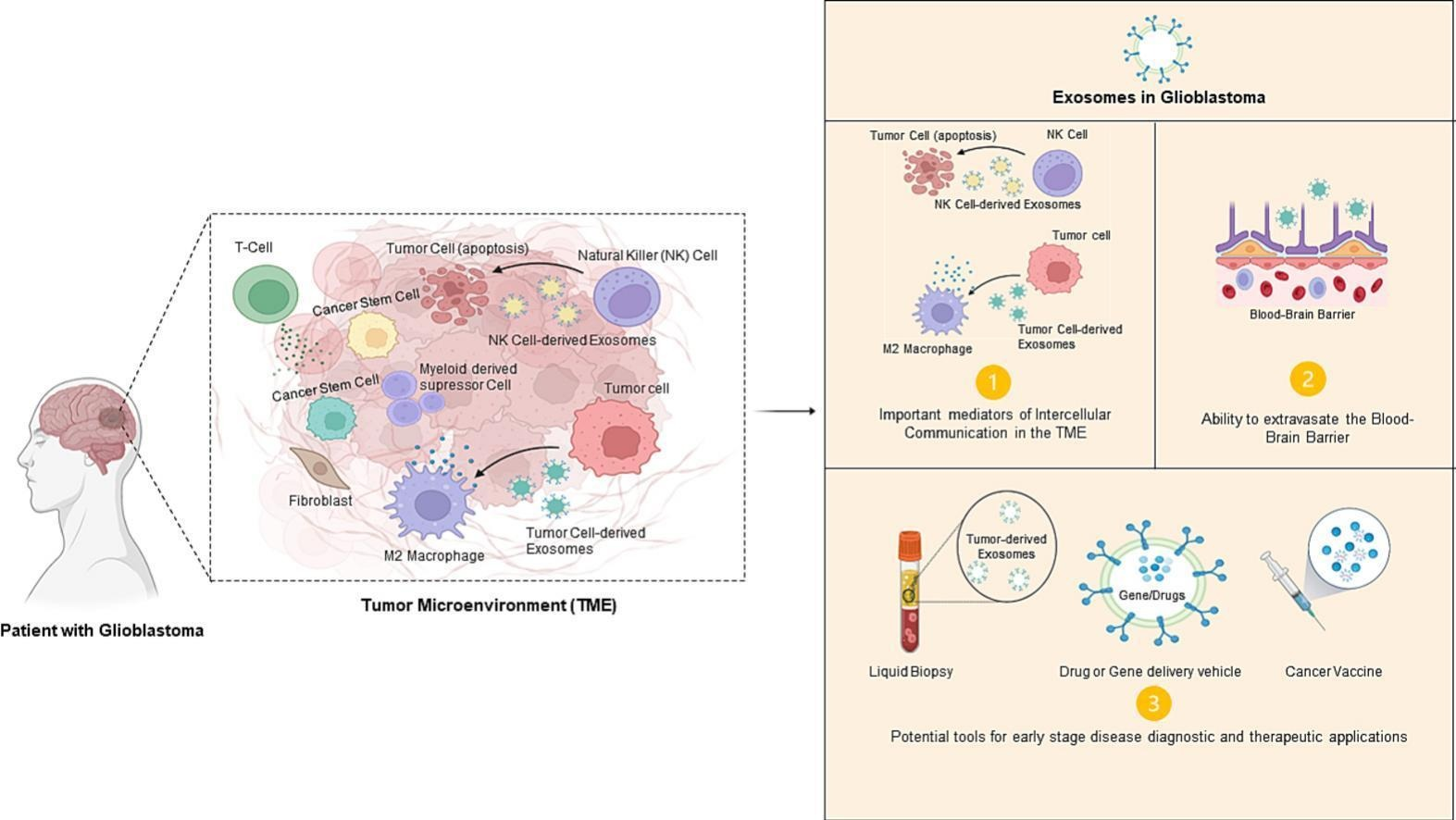
胶质母细胞瘤(GBM)是最具侵袭性的脑肿瘤类型,近年来对分子病理学和细胞信号通路的进展加深了研究者对诱导肿瘤进展的细胞间通讯机制的理解,即细胞外囊泡或外泌体介导的细胞间通讯机制。来自葡萄牙波尔图大学的研究人员发表综述,总结了GBM发生发展与外泌体之间的联系,并期望利用靶向外泌体货物及外泌体穿越血脑屏障的能力,使外泌体成为诊断和治疗工具。相关内容以“Digging the intercellular crosstalk via extracellular vesicles: May exosomes be the drug delivery solution for target glioblastoma”为题于4月29日在线发表在国际药物制剂领域学术期刊Journal of Controlled Release杂志上。
根据肿瘤的细胞起源进行分类,胶质瘤是中枢神经系统(CNS)来源的脑肿瘤。胶质瘤包括起源于星形细胞的肿瘤——星形细胞瘤、间变性星形细胞瘤和胶质母细胞瘤(GBM)、少突胶质细胞(如少突胶质胶质瘤)、室管膜细胞(导致室管膜瘤)和多种细胞起源的肿瘤(混合胶质瘤)。世界卫生组织(WHO)定义了胶质瘤的标准分类,胶质瘤根据其恶性程度分类,由组织病理学标准确定,共分为四级,从一级到四级。I级和II级胶质瘤增生能力差,可手术切除,复发概率低,预后好。III级和IV级胶质瘤通常具有高度侵袭性,生长更为侵袭性,手术往往不足以完全切除肿瘤,增加了复发的可能性。存活率随肿瘤的组织学特征而变化。恶性胶质瘤,包括GBM,约占恶性脑肿瘤的77.5%。虽然GBM是罕见的,但一些研究表明GBM的发病率正在上升。《全球癌症统计2020》显示,脑肿瘤在发达国家男女发病率和死亡率最高的肿瘤中排名第14位。在发达国家,每10万人中男性发病率为4.7,女性发病率为3.6,而在不发达国家,每10万人中男性发病率为2.4,女性发病率为1.7。此外,发达国家的男性死亡率为3.6,女性死亡率为2.8,而不发达国家的男性死亡率为2.1,女性死亡率为1.4。《全球癌症统计2020》报告显示,死亡率与发病率相对接近。发病率的上升是多因素的,可能的因素包括人口老龄化、先进的诊断技术、电离辐射和空气污染等。GBM是一种高度侵袭性的癌症,由于其分子异质性、组织学复杂性、复发可能性和对治疗方法的耐药性,被认为是无法治愈的。很多治疗方法都对GBM无效,并且GBM患者的平均预期寿命近年来并没有显著改善,大约为12-15个月。对于GBM的研究,从活跃或抑制的信号通路到发现干细胞对恶性复发的影响,已经发现了GBM治疗开发中的几个新靶点。新疗法的引入,如基因疗法和癌症疫苗,可能会提供更好的治疗效果。然而,由于血脑屏障(BBB)的存在,脑肿瘤的新治疗方法的开发具有挑战性,导致治疗效果不佳和随后的高死亡率。然而,更高的发病率意味着更高的死亡率,需要开发新的治疗和诊断方法来治疗胶质瘤,特别是GBM。外泌体是几乎所有细胞释放的各种生物液体中的小细胞外囊泡,因此携带其亲本细胞特有的各种生物分子。一些证据表明,外泌体介导肿瘤微环境中的细胞间通讯并穿过血脑屏障,是脑肿瘤等脑病诊断和治疗的重要工具。外泌体在GBM肿瘤微环境中的作用的研究在过去几十年有了长足进展,这些研究提示了外泌体在肿瘤细胞和不同类型免疫细胞之间的细胞间通讯中的作用。此外,破译外泌体的功能可以帮助理解一些癌症特征,如诱导血管生成、逃避炎症或诱导癌症干细胞分化的能力。因此,外泌体可以成为一个有前途的无创诊断平台的重要工具,而且外泌体存在于所有体液中、含有亲代细胞的特定生物成分等优势。在这篇综述中,研究人员回顾了GBM和外泌体之间的一些生物学特性和相互作用,描述了外泌体在GBM肿瘤微环境中的作用及其在非侵入性诊断和治疗方法方面的潜力,即作为药物或基因递送和癌症疫苗的纳米载体。研究人员认为,一系列的体外和体内的治疗应用证明了外泌体作为治疗方法的潜力。然而,外泌体的复杂性可能是一个问题,因为它们的货物研究目前较为粗糙,直接靶向外泌体货物可能存在潜在的脱靶效应。外泌体的临床应用似乎仍然具有挑战性,这表明细胞间通讯的复杂性和进一步研究脑肿瘤中这些机制的必要性。尽管如此,由于外泌体似乎与几种癌症特征有关,并且具有独特的特征,使其成为诊断和治疗GBM的潜在工具,我们相信随着癌症研究的进展,外泌体将成为治疗GBM的重要组成部分。
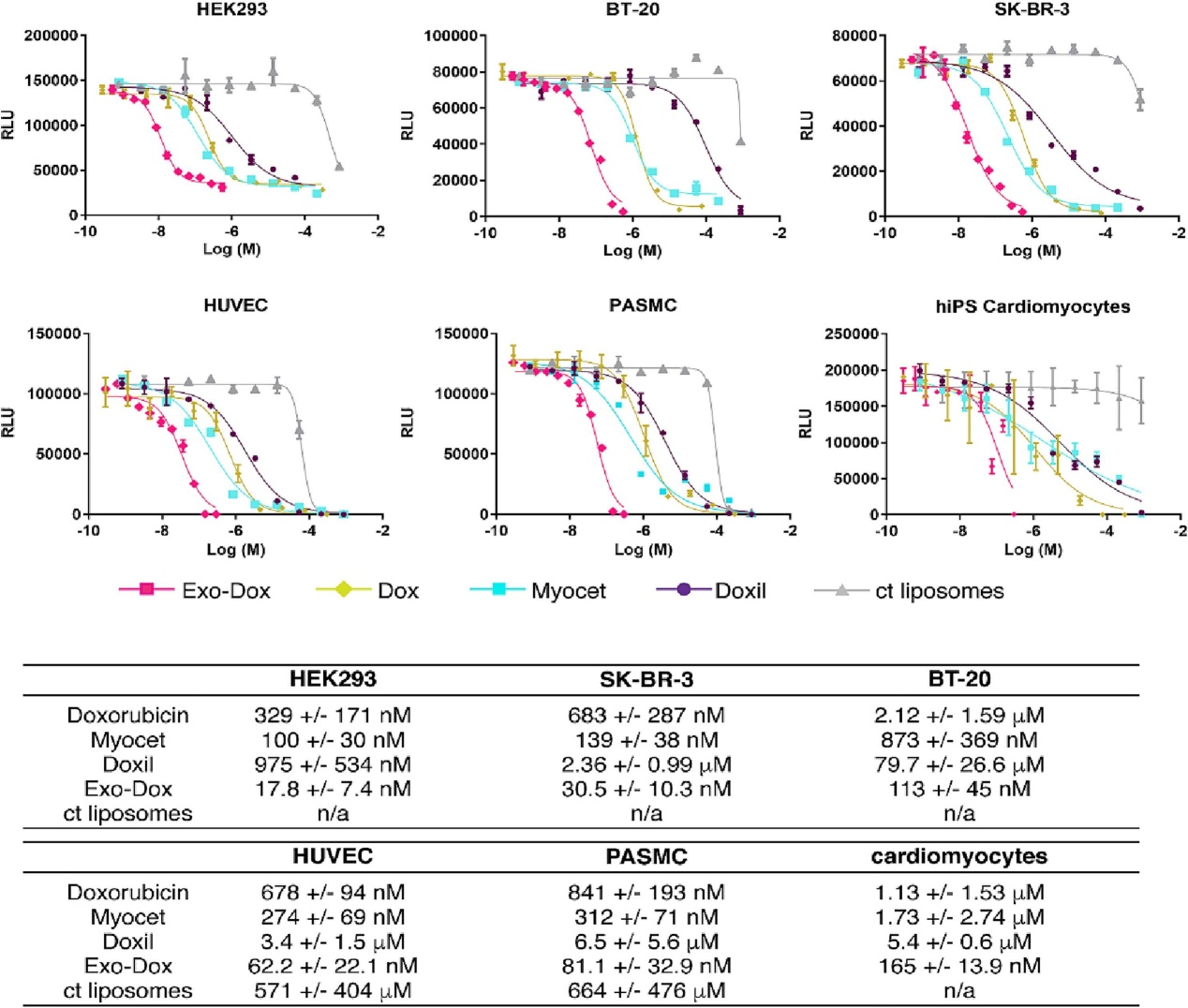
图:外泌体阿霉素Exo-Dox比游离阿霉素Dox、阿霉素脂质体Doxil、非聚乙二醇化的阿霉素脂质体或对照脂质体更有效,通过细胞ATP含量作为发光法细胞活力检测的指标。参考文献:Digging the intercellular crosstalk via extracellular vesicles: May exosomes be the drug delivery solution for target glioblastoma? J Control Release. 2023 Apr 29;358:98-115.