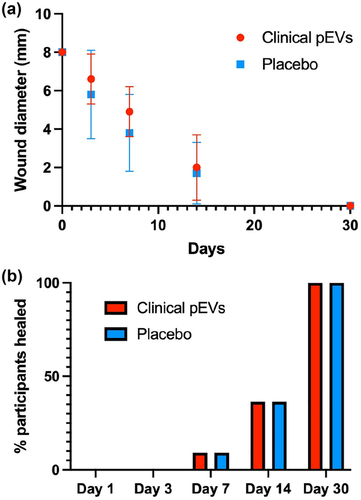
“Delayed wound healing”(伤口延迟愈合)是一个重要的未满足医疗需求领域。慢性伤口影响了发达国家1%至2%的人口,每年在医疗保健方面的花费超过250亿美元。患有血管疾病和糖尿病等并发症的个体患慢性伤口的风险增加。当伤口愈合过程被打乱时,就会出现慢性伤口。正常、健康的伤口愈合包括四个连续、相互重叠的阶段:止血;炎症;细胞增殖;和重塑,最终导致伤口闭合。然而,慢性伤口通常进入持续的炎症状态,并未能通过细胞增殖和重塑阶段愈合。血小板是身体内对损伤的第一反应者,并表现出引起组织生长和修复的显著能力。因此,血小板及其衍生物,包括富含血小板的血浆(PRP)和血小板裂解物,已被研究用于重新启动伤口愈合。然而,临床试验的疗效报告存在差异。其中一个可能的变异源可能是缺乏明确的血小板激活和PRP制备的黄金标准方案。因此,PRP治疗的血小板数量和生长因子含量可能因剂量而异。此外,血浆中可能含有高水平的抗血管生成因子,这些因子可能会抵消血小板有益的促血管生成作用。激活后,血小板释放细胞内储存的生长因子、细胞因子和细胞外基质调节剂。这些因子可以作为游离蛋白释放,但也可以在与母细胞相比富集的形式下在细胞外囊泡(EVs)中释放。EVs是纳米级别的脂质膜包裹颗粒,可将母细胞中的蛋白质、脂质和核酸传递到受体细胞中。EVs由人体内几乎所有类型的细胞释放,包括血小板,作为细胞间信号传递的自然介质。多项研究表明,血小板外囊泡(pEVs)具有改善细胞过程的能力,这些过程对于伤口愈合至关重要,包括增殖、血管生成和免疫调节。pEVs已被证明可以挽救异常成纤维细胞和内皮细胞行为,并重新启动愈合过程,并被证明是血小板治疗有效性的主要介质。此外,EVs在血液中可以高度稳定,并定位到受损组织。然而,目前的EV分离和纯化方法依赖于繁琐、缓慢和不可扩展的过程,限制了pEVs作为伤口愈合药物在临床上的适用性。该研究首次提供了临床级pEVs对人类的安全性和治疗效用的证据。证明了通过一种新型色谱法过程——基于配体的外泌体亲和纯化(LEAP)分离的pEVs保留了其母细胞类型的再生特性。LEAP分离的pEVs诱导成纤维细胞和皮肤内皮细胞的愈合相关增殖、迁移和血管生成行为。对分离的pEVs进行蛋白质组学分析发现存在多种生长因子,pEVs对细胞的响应至少部分是通过它们激活ERK和Akt信号通路介导的。pEVs作为潜在治疗慢性伤口的药物的一步,LEAP分离的pEVs被制成临床级别、异基因、候选治疗产品,并在健康志愿者中进行了随机安慰剂对照的I期临床试验,以评估其对伤口愈合的影响。未观察到显著不良反应。这些结果表明,通过LEAP分离过程制造的pEVs有望作为治疗伤口延迟愈合(如慢性伤口)的药物进行临床研究。(a)伤口愈合速率的图表,显示了经过处理(红色)和未经处理(蓝色)的4毫米穿刺活检诱导伤口的愈合时间。伤口直径定义为垂直直径和水平直径之和。(b)伤口愈合速率的图表,显示了治疗(红色)和未治疗(蓝色)的完全愈合伤口数量,记录在参与者体格检查期间。尽管进行了伤口愈合速率的探索性评估,但健康个体中的4毫米皮肤穿刺活检伤口自然愈合迅速,使得临床pEV治疗和安慰剂之间愈合时间的任何差异都难以观察到。此外,健康个体中的皮肤穿刺活检伤口的愈合与患有基础健康状况(如不愈合的糖尿病性溃疡)的患者的慢性伤口的愈合有很大的不同。健康伤口不应缺乏pEVs携带的生物分子,这可能进一步解释了观察到的生物活性缺乏。相反,患有慢性伤口的患者遭受导致愈合的生物事件抑制,而pEVs可能能够扭转这种情况。例如,在以前的动物研究中,pEVs治疗导致糖尿病性溃疡大鼠模型中伤口愈合速度比未经处理的伤口更快。两项研究之间进一步的差异是,大鼠伤口使用装载pEVs的水凝胶进行治疗,该水凝胶在数天内释放治疗剂量,而不是使用单次注射进行治疗。这些差异应在未来设计用于测试pEVs在定义伤口延迟愈合患者队列中有效性的临床试验中考虑。总之,该研究已经证明了LEAP色谱法适用于从血小板细胞释放物中制造临床级pEVs的可扩展制造,作为伤口愈合的实验性治疗。pEVs在一系列愈合伤口的体外试验中表现出活性,并在I期临床试验中安全地用于健康志愿者的伤口愈合安全性评估。所有伤口都迅速而完全地愈合,未观察到治疗和未治疗伤口愈合时间的差异。尽管在这个健康志愿者队列中,评估有效性的次要终点在这个剂量下没有达到,但在只涉及健康志愿者的安全性评估试验中,这个结果并不出乎意料,因为健康志愿者具有正常迅速的伤口愈合反应。未来临床试验进一步探索pEV治疗在伤口延迟愈合方面的有效性是有必要的。Johnson J, Law SQK, Shojaee M, Hall AS, Bhuiyan S, Lim MBL, Silva A, Kong KJW, Schoppet M, Blyth C, Ranasinghe HN, Sejic N, Chuei MJ, Tatford OC, Cifuentes-Rius A, James PF, Tester A, Dixon I, Lichtfuss G. First-in-human clinical trial of allogeneic, platelet-derived extracellular vesicles as a potential therapeutic for delayed wound healing. J Extracell Vesicles. 2023 Jul;12(7):e12332. doi: 10.1002/jev2.12332. PMID: 37353884; PMCID: PMC10290200.外泌体资讯网 JEV:血小板EVs的首次人体临床试验,伤口愈合治疗应用