糖尿病视网膜病变(diabetic retinopathy,DR)是糖尿病最常见的微血管并发症之一,严重威胁患者的视力。视网膜血管内皮细胞(human retinal vascular endothelial cell,HRVEC)功能障碍及异常新生血管形成是DR进展过程中的主要病理特征,新生血管会导致视网膜水肿、玻璃体出血、牵拉性视网膜脱离等严重并发症。近年来,外泌体(exosome)作为细胞间信号传递的重要媒介引起了广泛关注。玻璃体液内可能存在各种视网膜细胞分泌的外泌体,并在介导视网膜病变病理机制中起一定作用。
近日,南京医科大学第一附属医院眼科谢平、刘庆淮教授团队在Diabetes上发表题为“The exosome-transmitted lncRNA LOC100132249 induces endothelial dysfunction in diabetic retinopathy”的研究论文(2023 Jun 22;db220435),探究了增殖性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)患者玻璃体液来源的外泌体中可能促进视网膜新生血管形成的关键分子及其调控机制。南京医科大学第一附属医院眼科胡仔仲和王婧帆为第一作者,谢平教授和刘庆淮教授为共同通讯作者。
首先,课题收集了PDR患者与黄斑裂孔(macular hole,MH)患者(对照组)的玻璃体液,超速离心法分离其外泌体(分别为PDR-exo和MH-exo)并且刺激视网膜血管内皮细胞(HRVECs),通过EdU、Transwell、Matrigel胶成管实验发现PDR-exo具有促进血管内皮细胞增殖、迁移、成管的效应。
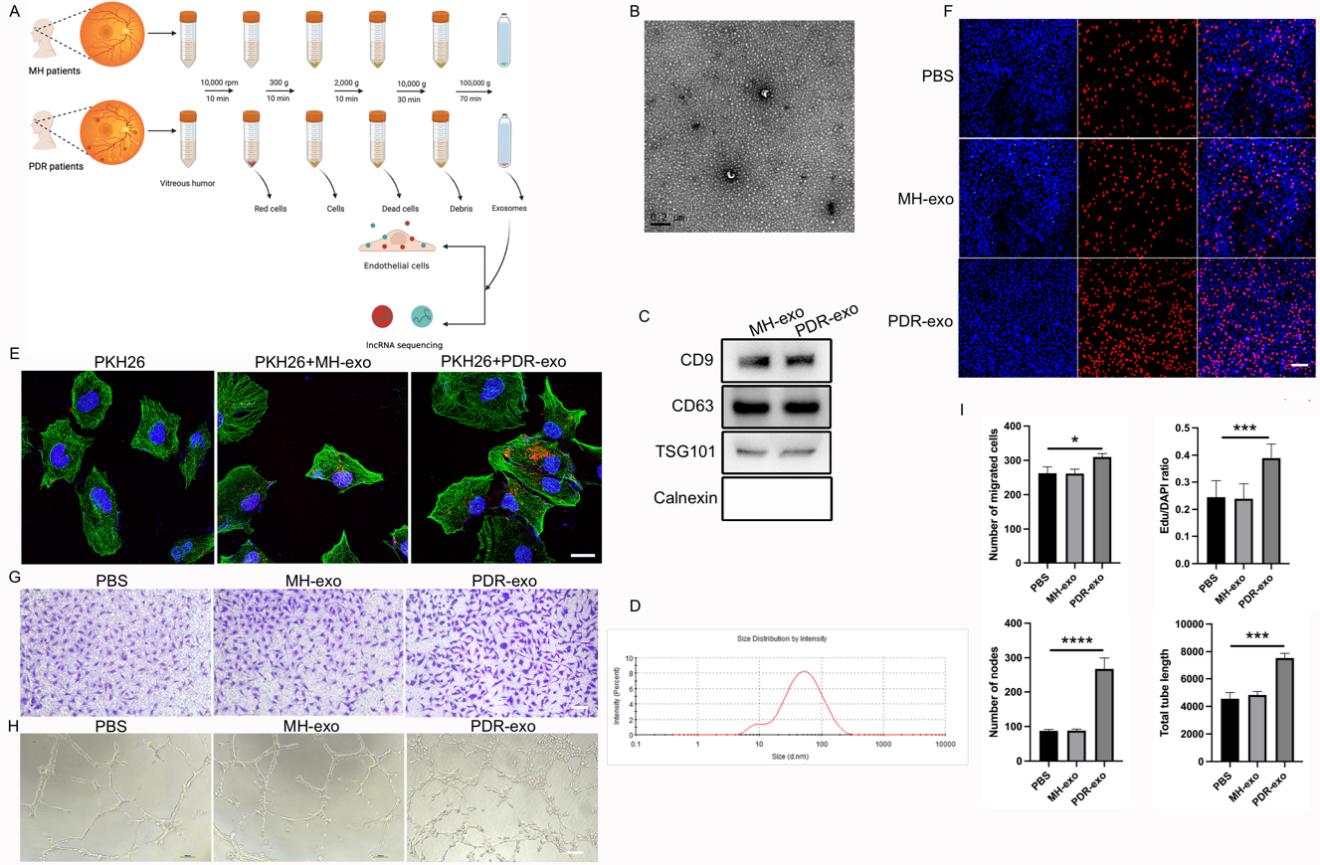 图1:PDR患者和MH患者玻璃体液来源的外泌体鉴定及其对HRVECs的促血管生成作用
图1:PDR患者和MH患者玻璃体液来源的外泌体鉴定及其对HRVECs的促血管生成作用
接下来,通过高通量测序技术挖掘PDR-exo中促进新生血管形成的关键LncRNA并进行RT-qPCR验证,发现LncRNA LOC100132249在PDR-exo中显著上调,溯源发现高糖刺激的HRVECs是其主要来源。
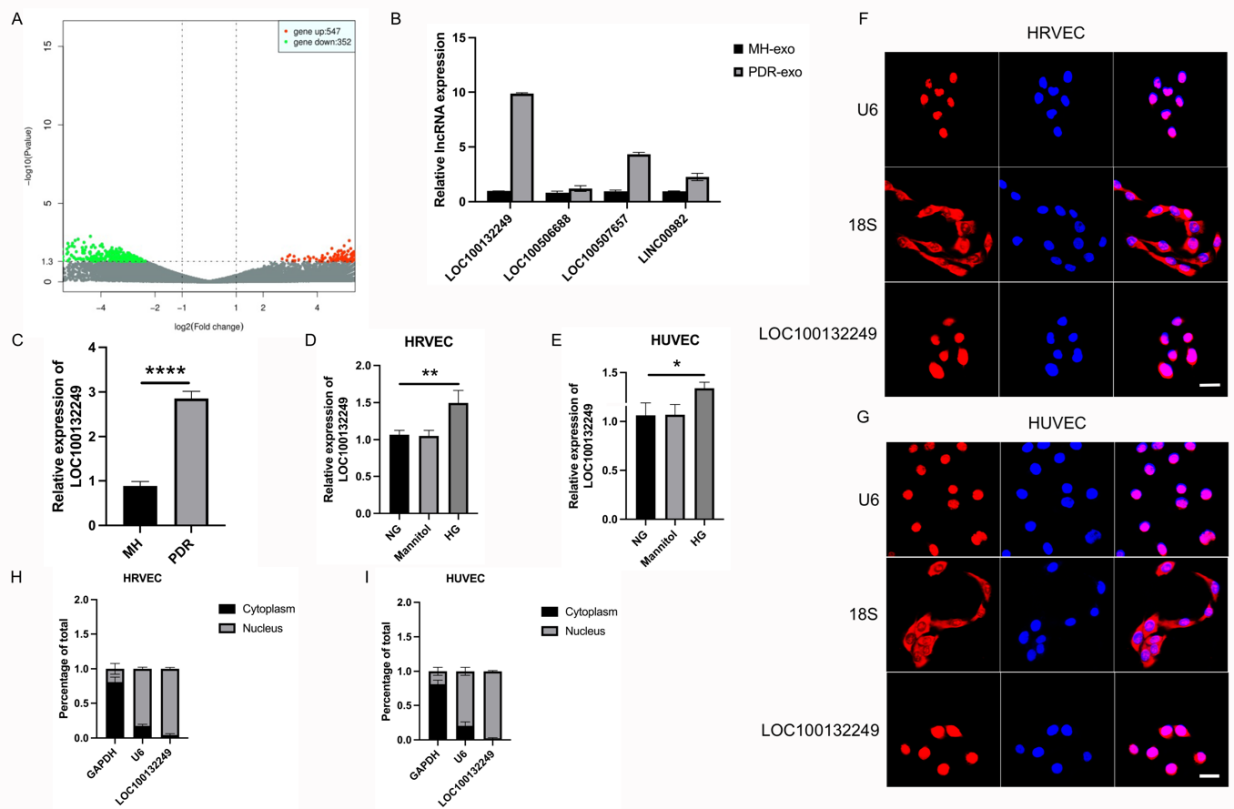 图2: LncRNA LOC100132249在PDR-exo和高糖刺激的HRVECs中富集
图2: LncRNA LOC100132249在PDR-exo和高糖刺激的HRVECs中富集
在细胞层面和氧诱导的视网膜病变(oxygen induced retinopathy,OIR)小鼠模型中进一步验证外泌体传递的LncRNA LOC100132249在体外和体内促进新生血管形成。
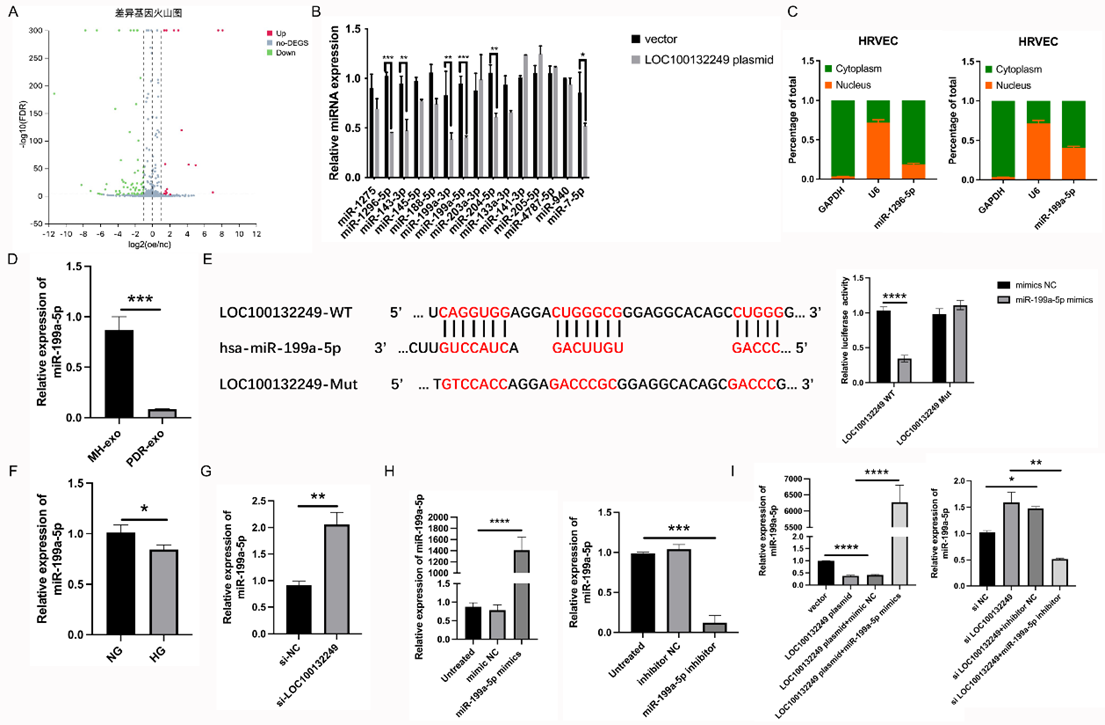 图3:外泌体传递的LncRNA LOC100132249在体内和体外促进新生血管形成
图3:外泌体传递的LncRNA LOC100132249在体内和体外促进新生血管形成
机制上,LncRNA LOC100132249可作为miR-199a-5p的内源性“海绵”调节SNAI1的表达,激活Wnt/β-catenin通路,最终导致血管内皮细胞功能障碍。
 图4: LncRNA LOC100132249可作为miR-199a-5p的内源性“海绵”
图4: LncRNA LOC100132249可作为miR-199a-5p的内源性“海绵”
参考文献:The exosome-transmitted lncRNA LOC100132249 induces endothelial dysfunction in diabetic retinopathy.Diabetes. 2023 Jun 22:db220435.
外泌体资讯网 Diabetes | 南京医科大学一附院眼科谢平/刘庆淮:外泌体传输的lncRNA诱导糖尿病视网膜病变的内皮功能障碍





