由于缺乏针对早期病变的特异性生物标志物,并且这些标志物的水平较低,因此通过液体活检检测早期癌症一直是一个难点。来自美国哈佛大学医学院麻省总医院的研究人员针对输卵管内的前驱病变的高级别浆液性卵巢癌(HGSOC),系统地开发了一种基于细胞外囊泡(EV)的早期检测方法。该方法成功实现了少量的输卵管来源EV的检测,并获取了5种EV生物候选物,将HGSOC与非癌区分开来,得到了89%的灵敏度和93%额特异性;也实现了将非癌、早期HGSOC和晚期HGSOC区分开来。该研究支持了EV在早期癌症检测中的潜在应用。相关内容以“Inaugurating High-Throughput Profiling of Extracellular Vesicles for Earlier Ovarian Cancer Detection”为题于7月23日在线发表在国际综合性学术期刊Advanced Science杂志上。
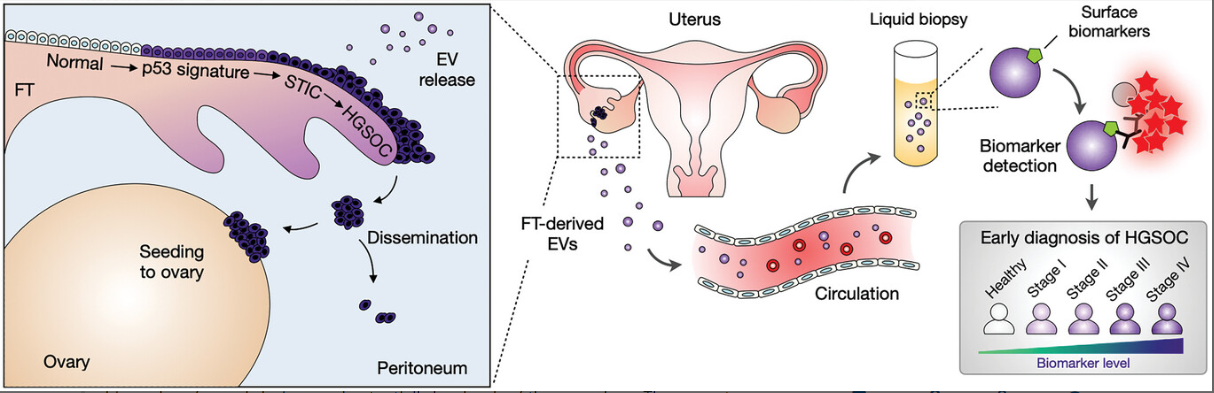
研究设计示意图。高级别浆液性卵巢癌(HGSOC)被认为起源于输卵管(FT)内的前驱病变。因此,来自FT前驱病变的循环EV可以作为早期HGSOC生物标志物。在本研究中,研究人员确定了FT特异性的EV标记物,并在HGSOC患者的血液样本中进行了检测,分析了FT衍生EV的表面标记物在区分早期(I期和II期)和晚期(III期和IV期)HGSOC患者的可用性。
循环生物标志物的分析(或称为液体活检)在癌症诊疗中成为一种新的策略,使临床医生能够通过微创和可重复的测试来检测和监测疾病。循环生物标志物检测潜力已得到证明,特别是在检测晚期癌症患者方面。然而,将液体活检扩大到早期癌症诊断中则面临着技术挑战。这是因为,关于早期病变的特异性生物标志物的信息很少,这些标志物的水平可能在循环中很低。卵巢癌(ovarian cancer,OvCa)是最致命的妇科疾病,同样需要早期生物标志物的检测。在一项大型、多年的筛查试验中,传统的血液检测(如CA125)和影像学检查未能显示出生存优势,主要是因为最常见的OvCa亚型——高级别浆液性卵巢癌(high-grade serous ovarian carcinoma,HGSOC),通常在原发部位扩散后才能检测到。这一事实强调了改进检测方法和基于肿瘤进化的更好的标记物选择的必要性。
越来越多的生物学和临床数据支持,大部分HGSOC起源于远端输卵管(fallopian tube,FT)内的前体病变。晚期HGSOC患者常伴有浆液性输卵管上皮内癌(serous tubal intraepithelial carcinoma,STIC)病变,与肿瘤中发现的TP53突变相同。统计研究表明,近60%的上皮性HGSOC起源于输卵管。通过对FT前体病变的分子标记进行探索和揭示,将为早期HGSOC诊断提供了前景。
近年来,一个有吸引力的生物标志物分析目标是细胞分泌的细胞外囊泡(EVs)。EV反映了肿瘤细胞的分子载货,并在附近的体液中循环。因此,分析EV可以代表一种实时、微创的方式来检测和监测肿瘤分子状态,包括前驱病变,如STICs。肿瘤相关的EVs已经被证明是OvCa生物标志物的有效替代物,用于肿瘤检测和治疗监测。然而,大多数研究主要分析了晚期肿瘤,这使EV标记物偏向于晚期临床表现。可以想象,早期HGSOC病变可能具有不同于晚期肿瘤或细胞培养条件下的分子特征——识别和验证这种EV特征对于提高早期肿瘤诊断至关重要。
在这项研究中,研究人员开发了基于EV的血液检测早期(或小体积的)HGSOC检测。研究人员特别认为,来自前驱病变的EV可以在血液中被识别出来,作为侵袭前或早期HGSOC的循环生物标志物(如示意图所示)。为了验证这一假设,研究人员采用了双管齐下的方法——开发了一种高通量EV测定方法,称为SAViA(Signal Amplifying Vesicles in Array,信号放大囊泡芯片),并首次对来自输卵管的EV进行了已知的分析。结果显示,结合EV物理吸附和酪胺辅助信号增强技术,SAViA分析方法的分析灵敏度比传统免疫分析方法提高了1000倍以上,能够在便于使用的微孔板(386孔)中检测到少量EV(≈600个囊泡)。
通过建立具有致癌突变的FT细胞,并通过蛋白质组学分析其EV,研究人员鉴定了HGSOC特异性EV标记物。随后,在模拟肿瘤发生、进展和转移的原位HGSOC小鼠模型中对这些标记物进行连续监测。SAViA实验显示,在连续抽取的荷瘤小鼠血液中,表达HGSOC标记的EV随着肿瘤的发生而增加,这支持了EV在早期癌症检测中的潜在应用。在随后的临床样本(n = 51)的初步研究中,研究人员进一步完善了HGSOC-EV特征标志物(包括CD24、EpCAM、HE4、TNC、VCAN),实现了89%的诊断敏感性和93%的特异性。同样的5个标志物也有效地将3个临床不同的组分为非癌(n = 14)、早期HGSOC (I期,II期;n = 17)、晚期HGSOC (III期,IV期;N = 20),在区分早期HGSOC与其他HGSOC的特异性为0.91。因此,该方法首次应用于输卵管源性EVs,可能成为一种微创工具,用于监测卵巢癌高危女性,以便及时进行疾病干预。
参考文献:Inaugurating High-Throughput Profiling of Extracellular Vesicles for Earlier Ovarian Cancer Detection. Adv Sci (Weinh). 2023 Jul 23:e2301930.
外泌体资讯网 Adv Sci丨细胞外囊泡的高通量分析用于卵巢癌早期检测