自从1983年被发现,细胞外囊泡(Extracellular vesicles, EVs)便已经从单纯的细胞废物处理系统发展成为一种新的细胞间通讯机制。EVs的外围由磷脂双分子层所组成,其内容物包括蛋白、核酸以及相关代谢产物等。这些具有生物活性的搭载物在乳腺癌及肝细胞癌等实体肿瘤的发生发展过程中发挥了重要作用。
近日,大连理工大学附属肿瘤医院林杰、祝旭东课题组受邀在Front Bioeng Biotechnol(中科院2区,IF=5.7)和Front Endocrinol (Lausanne)(中科院2区,IF=5.2)杂志撰写综述,重点探讨EVs在肝细胞癌(Hepatocellular carcinoma, HCC)以及乳腺癌诊断及治疗中的重要作用。
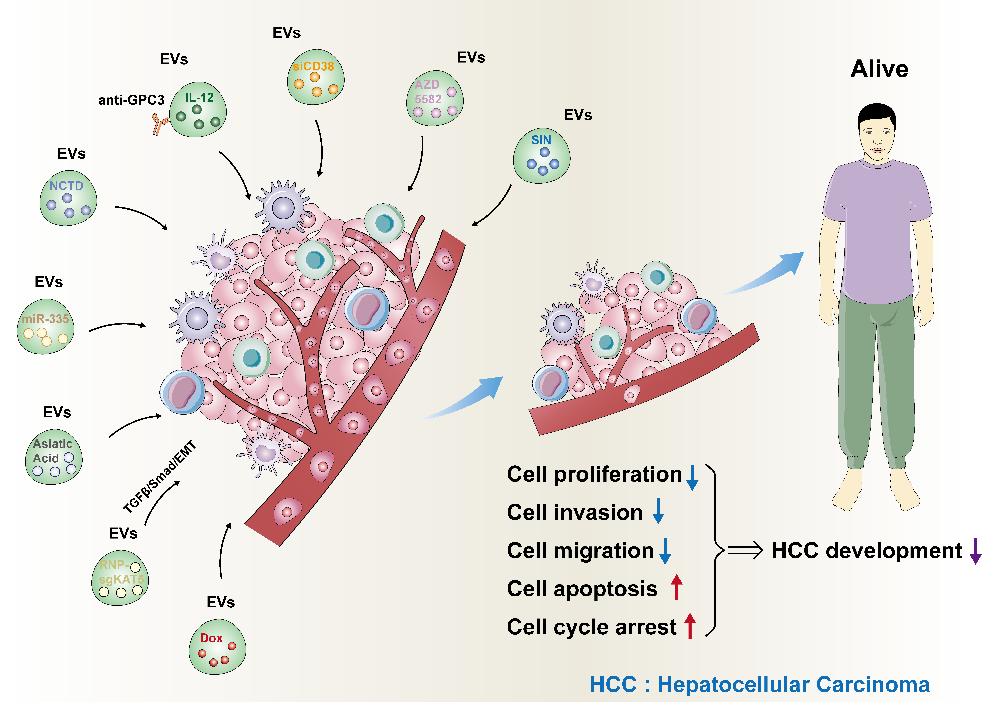
在肝细胞癌中,研究者发现EVs中所搭载的活性物质不仅能够促进HCC的增殖,侵袭,转移以及化疗耐药,还能够作为HCC纳米治疗的潜在靶点。作者总结了9种以EVs为基础的HCC纳米治疗新方法。分别包括EVs包载的SIN, EVs包载的AZD5582,EVs包载的siCD38,EVs包载的IL-12,EVs包载的NCTD,EVs包载的miR-335,EVs包载的Asiatic Acid,EVs包载的sgKAT5,以及EVs包载的Dox。这些包载相关药物的EVs均可显著抑制HCC细胞的增殖、侵袭、迁移、诱导细胞凋亡以及阻滞细胞周期,最终显著抑制HCC的进展(图1)。文章的通讯作者为辽宁省肿瘤医院&大连理工大学附属肿瘤医院普通外科林杰教授,祝旭东博士,第一作者为温州医科大学黄岩医院普通外科王才正医师。
图1
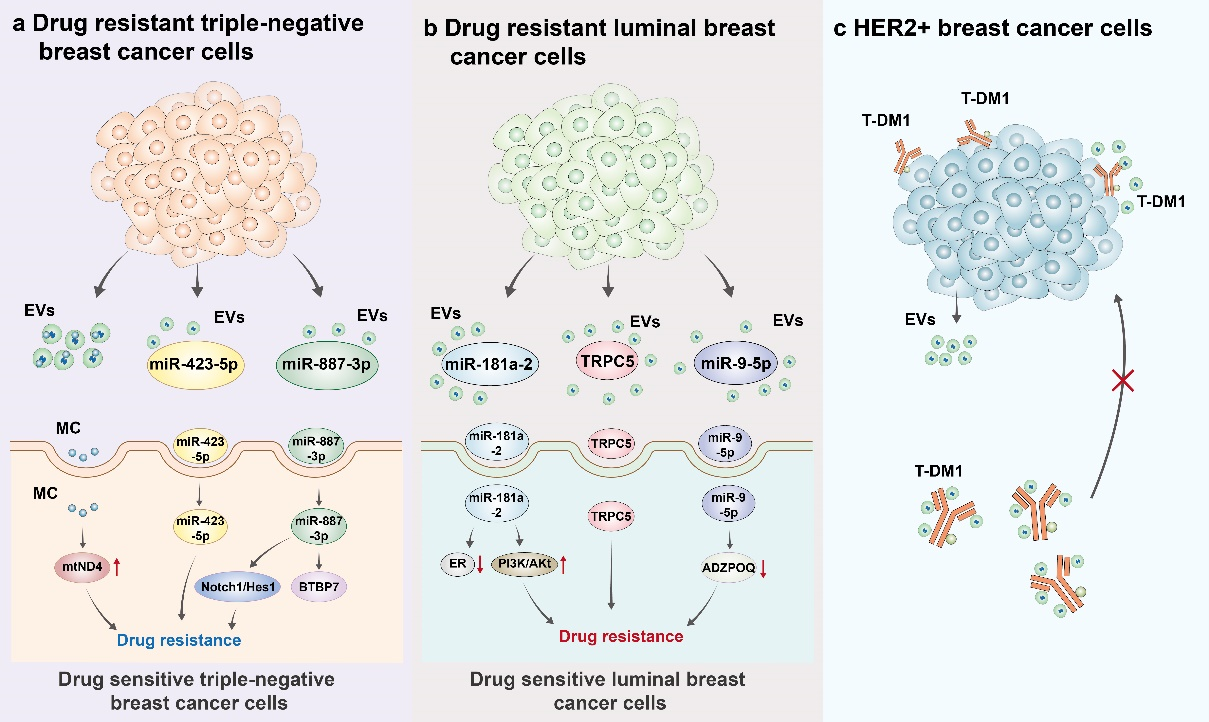
在乳腺癌中,作者重点总结了EVs中具有生物活性的搭载物在将乳腺细胞转化为乳腺癌细胞以及乳腺癌促转移龛形成中的重要作用。乳腺癌细胞衍生出的EVs能够显著的促进肿瘤生长、侵袭、血管生成、促转移龛形成、以及肿瘤转移。EVs还能够调节肿瘤微环境中的成纤维细胞,免疫细胞,以及影响细胞休眠促进肿瘤微环境与肿瘤细胞之间的对话,继而影响乳腺癌进展。另外,EVs中的搭载物可作为乳腺癌诊断标志物并可显著影响三阴性乳腺癌、luminal型乳腺癌以及HER2阳性乳腺癌的治疗耐药(图2)。相关结果将在临床实践中为乳腺癌的诊断和治疗提供理论基础,并开辟其治疗新路径。文章的通讯作者为辽宁省肿瘤医院&大连理工大学附属肿瘤医院普通外科林杰教授,祝旭东博士,第一作者为温州医科大学黄岩医院普通外科张斅颖医师。
图2
参考文献:
[1] Spotlights on extracellular vesicles in hepatocellular carcinoma diagnosis and treatment: an update review. Front. Bioeng. Biotechnol.2023, 11:1215518. doi: 10.3389/fbioe.2023.1215518
[2] Extracellular vesicles in the treatment and diagnosis of breast cancer: a status update. Front. Endocrinol. 2023,14:1202493. doi: 10.3389/fendo.2023.1202493
外泌体资讯网 辽宁省肿瘤医院/大连理工大学附属肿瘤医院林杰、祝旭东团队特约综述:细胞外囊泡在实体肿瘤诊断及治疗中的重要应用