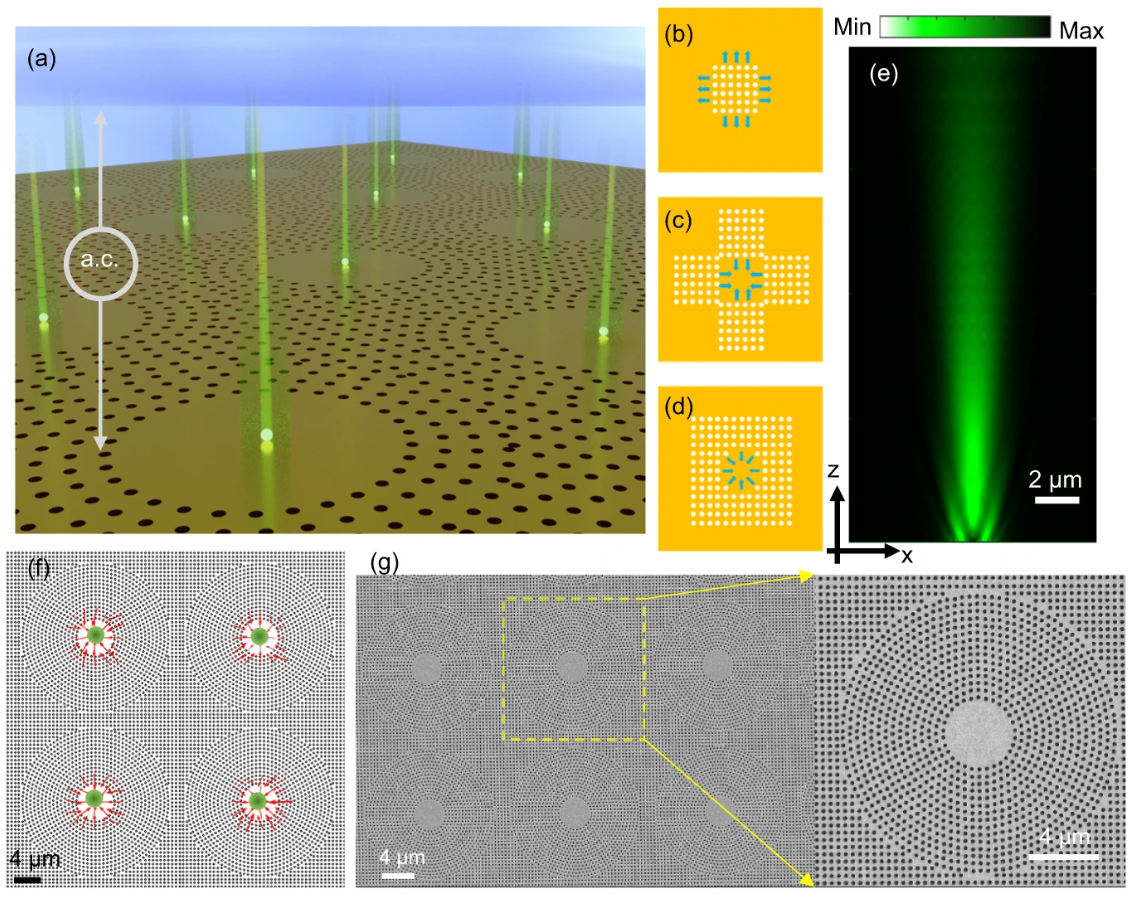
异质性的纳米级细胞外囊泡(extracellular vesicles,EVs)在疾病检测、监测和治疗方面具有重要意义。然而,由于这些纳米尺寸的EV体积小,使用光镊捕获它们一直具有挑战性。等离子体增强光学捕获提供了一个解决方案,然而现有的等离子体镊的吞吐量有限,并且可能需要几十分钟才能捕获低浓度的粒子。来自美国范德比尔特大学的研究人员提出了一种创新的方法,称为几何诱感应的电流体动力镊(GET),克服了这些限制。GET产生多个电流体动力电位,可在几秒钟内平行传输和捕获单个EV。通过在每个GET阱的中心集成纳米级等离子体腔,单个EV可以放置在等离子体腔附近,在激光照射下实现瞬间等离子体增强的光学捕获,而不会产生有害的加热效应。这种非侵入性可扩展的混合纳米镊为高通量等离子体增强的EV光谱开辟了新的视野。相关内容以“Scalable trapping of single nanosized extracellular vesicles using plasmonics” 为题于8月9日在线发表在Nature子刊、国际综合性学术期刊Nature Communications杂志上。
纳米级的细胞外囊泡曾经被认为是细胞排出废物的一种手段,近年来却引起了大量的科学兴趣,因为它们含有重要的生物分子,包括蛋白质、脂质和核酸,并作为细胞与邻近或远处细胞交流的手段。EV在大小、生物成因和分子组成上都是异质的,包括来自成熟并附着在细胞膜上释放的多泡体来源的外泌体(exosomes)、来自细胞膜向外出芽的胞外体(ectosomes)、2018年新发现的外泌颗粒(exomeres)、以及最近发现的直径仅为25纳米的超小颗粒(supermeres)。其中exomeres和supermeres的生物发生机制目前尚不清楚。鉴于它们的异质性,对EV的进一步了解的关键限制之一是缺乏在单个囊泡水平上捕获和分析的合适工具。开发这种能力将为研究大量EV提供手段,以了解它们在单颗粒水平上的大小和分子组成的异质性,并推动转化生物医学应用。
光镊(Optical Tweezers)技术获得了2018年诺贝尔物理学奖,已成为操纵微观生物物体(如细胞、胶体组合和单粒子光谱)的强大工具。在光镊中,使用紧密聚焦的激光束在微观物体上产生强大的梯度力,以稳定地将它们困在激光焦点处。然而,由于光的衍射极限,纳米尺度物体如纳米级EV的低功率稳定捕获一直面临着挑战。基于光镊的拉曼光谱需要高激光功率(~100 mW或更高)来稳定地捕获EV,这有时会导致EV破裂,干扰后续测量。降低激光功率会带来多个问题,包括捕获稳定性不足,使得粒子在信号收集完成之前从光阱中逃逸,以及可以捕获的囊泡大小受到限制。此外,光镊不能保证捕获单个电子粒子,并且经常导致在衍射受限的激光光斑内收集多个电子粒子。此外,将EV装载到光阱中是一个缓慢的过程,可能需要几分钟,这将对分析吞吐量产生不利影响。
针对传统光镊捕获稳定性有限的问题,研究者研究了基于等离子体腔的近场光纳米镊。等离子体腔与传播的光有效耦合,产生远低于衍射极限的增强且空间受限的电磁场。等离子体镊的早期发展依赖于布朗扩散来装载光阱,这是一个缓慢的、不确定的、耗时的过程,使得等离子体镊不适用于低粒子浓度的溶液。先前使用对流和热泳加载捕集器的策略存在粒子聚集的问题,不适用于单粒子捕集。电热等离子体(electrothermoplasmonic,ETP)镊的发展,利用外加交流电场的等离子体加热来诱导电热等离子体流,将粒子输送到等离子体腔,使粒子在几秒钟内快速捕获在被照亮的等离子体纳米结构中。然而,ETP方法需要等离子体加热将粒子传输到电磁热点,这也是过热点的位置,从而对脆弱的生物标本造成光热损伤。如果光热加热被消散,例如使用高导热衬底作为散热器,则局部等离子体诱导的温升就不存在了,这带来的缺点是,电热等离子体流不能再被诱导以使粒子能够传输到捕获点。迄今为止,还没有一种方法能够在确保消除等离子体热点的光热加热的同时,实现在等离子体热点稳定捕获的单纳米物体的快速传输。这种能力的缺乏对利用等离子体光学纳米镊分析像EV这样的纳米尺度生物物体的异质种群带来了障碍。
在这项研究中,研究人员报道了一种几何感应的电流体动力镊(geometry-induced electrohydrodynamic tweezer,GET),它解决了上述挑战,并满足了单个EV捕获的理想纳米机械手的要求。GET可以在等离子体热点附近的几秒钟内对单个纳米级物体(如纳米级EV)进行大规模并行捕获,而无需在捕获点进行光热加热,从而确保捕获点始终是低温上升的位置。GET也是可扩展的,单粒子GET阱的数量取决于通过光刻制造在芯片上定义的阱位置的数量,可以根据需要从数百、数千或数百万不等。通过在每个GET阱的中心整合单个等离子体腔,电流体动力势在几秒钟内将粒子平行放置在等离子体腔附近,当任何GET阱被聚焦激光照射而没有任何有害的光热加热时,可以促进瞬时近场等离子体增强光学捕获。该发现代表了纳米级捕获和光学纳米操作领域的重大发展,解决了在几秒钟内快速并行捕获单个纳米大小的囊泡和粒子的重要任务,瞬时等离子体捕获单粒子分辨率而没有光热损伤的风险,从而为高通量等离子体增强单粒子光谱铺平了道路。
参考文献:Scalable trapping of single nanosized extracellular vesicles using plasmonics. Nat Commun. 2023 Aug 9;14(1):4801.
外泌体资讯网 Nat Commun丨通过等离子体技术捕获单个细胞外囊泡