创伤性脑损伤(TBI)仍然是与损伤相关的残疾和死亡的主要原因,但由于TBI发病机制的复杂性,目前临床上仍缺乏有效的诊治手段。 越来越多的证据表明,细胞外囊泡(EVs)作为新兴候选者,有望成为TBI的诊断标志物以及潜在的治疗靶点。然而,不同的细胞外囊泡亚型对TBI的病理生理的作用差异巨大,甚至完全相反。因此,在细胞外囊泡可用作TBI治疗的靶点之前,有必要根据不同的细胞外囊泡亚型的功能而对其进行分类,以阐明基于EVs治疗TBI的不同策略。
近日,首都医科大学附属北京天坛医院神经外科董信龙医生团队在国际学术期刊Cell Communication and Signaling上发表题为“Roles and therapeutic potential of different extracellular vesicle subtypes on traumatic brain injury”的研究论文(2023 Aug 18;21(1))。论文首次提出病理性细胞外囊泡(PEV)和生理性细胞外囊泡(BEV)的概念以明确不同EVs亚型对TBI的矛盾作用,并提出基于不同EVs亚型的治疗思路,为EVs的临床转化奠定基础。首都医科大学附属北京天坛医院神经外科董信龙医生为论文的第一作者兼通讯作者。
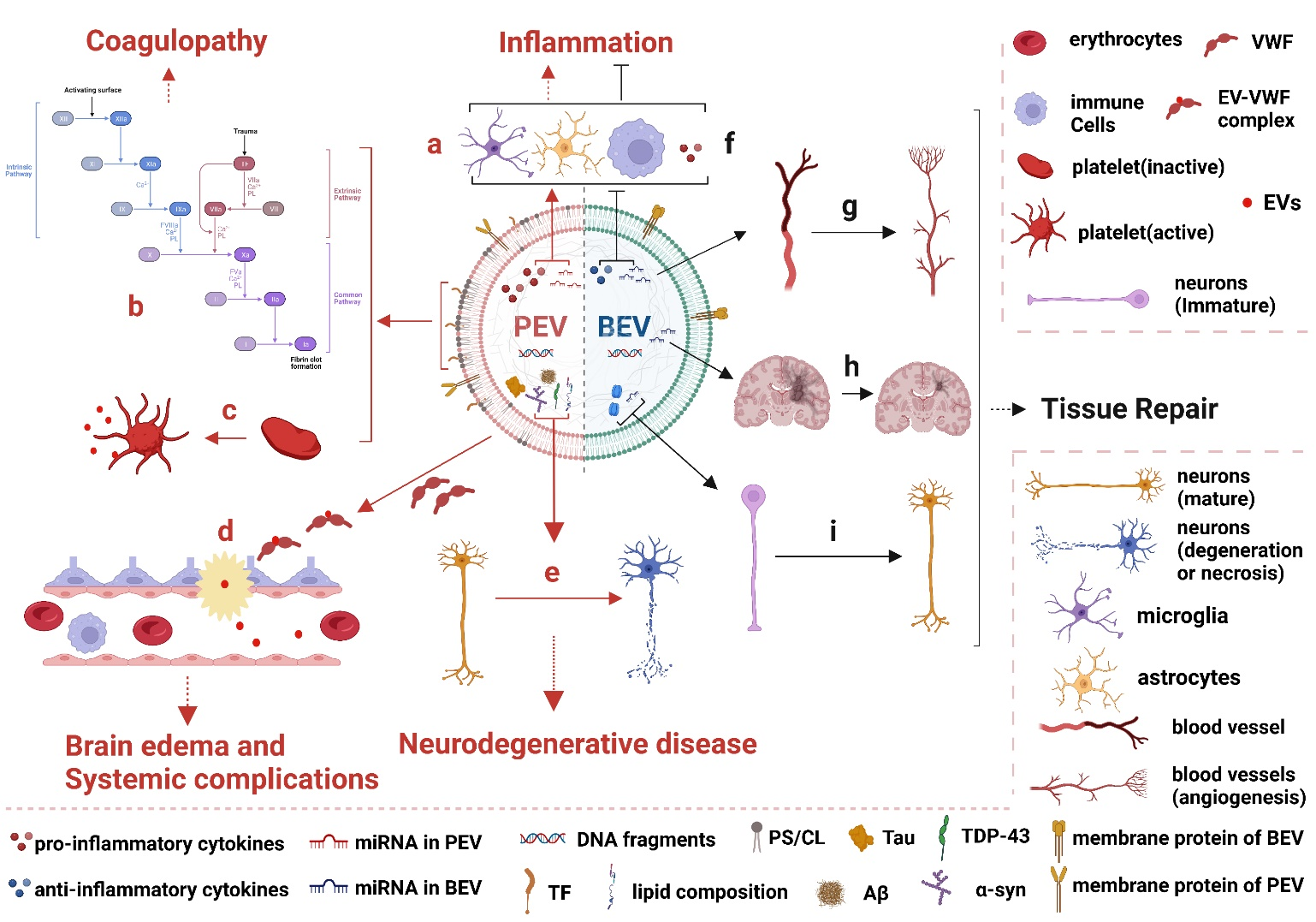
细胞外囊泡(EVs)对脑损伤患者的康复有双重作用,根据其作用的差异,作者团队将EVs分为PEV和BEV。PEV介导TBI继发性损伤的病理生理过程(图1),如炎症反应、凝血功能障碍、血脑屏障破坏和脑水肿、全身并发症和神经退行性疾病(图1a-e)。具体而言,PEV中的miRNA和促炎细胞因子促进神经胶质细胞和免疫细胞的活化和促炎细胞因子的释放(图1a);PEV中的PS/CL和TF触发并加剧凝血级联反应(图1b);PEV中的PS/CL激活血小板并使其释放更多的PEV(图1c);EV-VWF复合体破坏血脑屏障,EVs透过受损的血脑屏障进入外周循环(图1d);PEV通过传递错误折叠的蛋白质从而导致神经元变性和细胞凋亡(图1e)。而BEV抑制TBI继发性损伤的进展,抑制过度炎症,并参与组织修复和机体康复(图1f-i)。如BEV中的miRNA和抗炎细胞因子抑制神经胶质细胞和免疫细胞的活化以及促炎细胞因子的释放(图1f);BEV促进新血管的形成(图1g);BEV中的miRNA抑制神经胶质瘢痕的过度生成(图1h);BEV中的神经营养因子和miRNA促进神经元的生长和成熟(图1i)。
图 1 PEV和BEV对TBI的不同作用和治疗潜力
Abbreviations: Aβ:amyloid β-peptide;α-syn:α-synuclein; BBB: blood-brain barrier; BEV: biological extracellular vesicles; CL: cardiolipin; EVs: extracellular vesicles; PEV: pathological extracellular vesicles; PS: phosphatidylserine; TDP-43: TAR DNA-binding protein of 43 kDa; TF: tissue factor; VWF: von Willebrand factor.
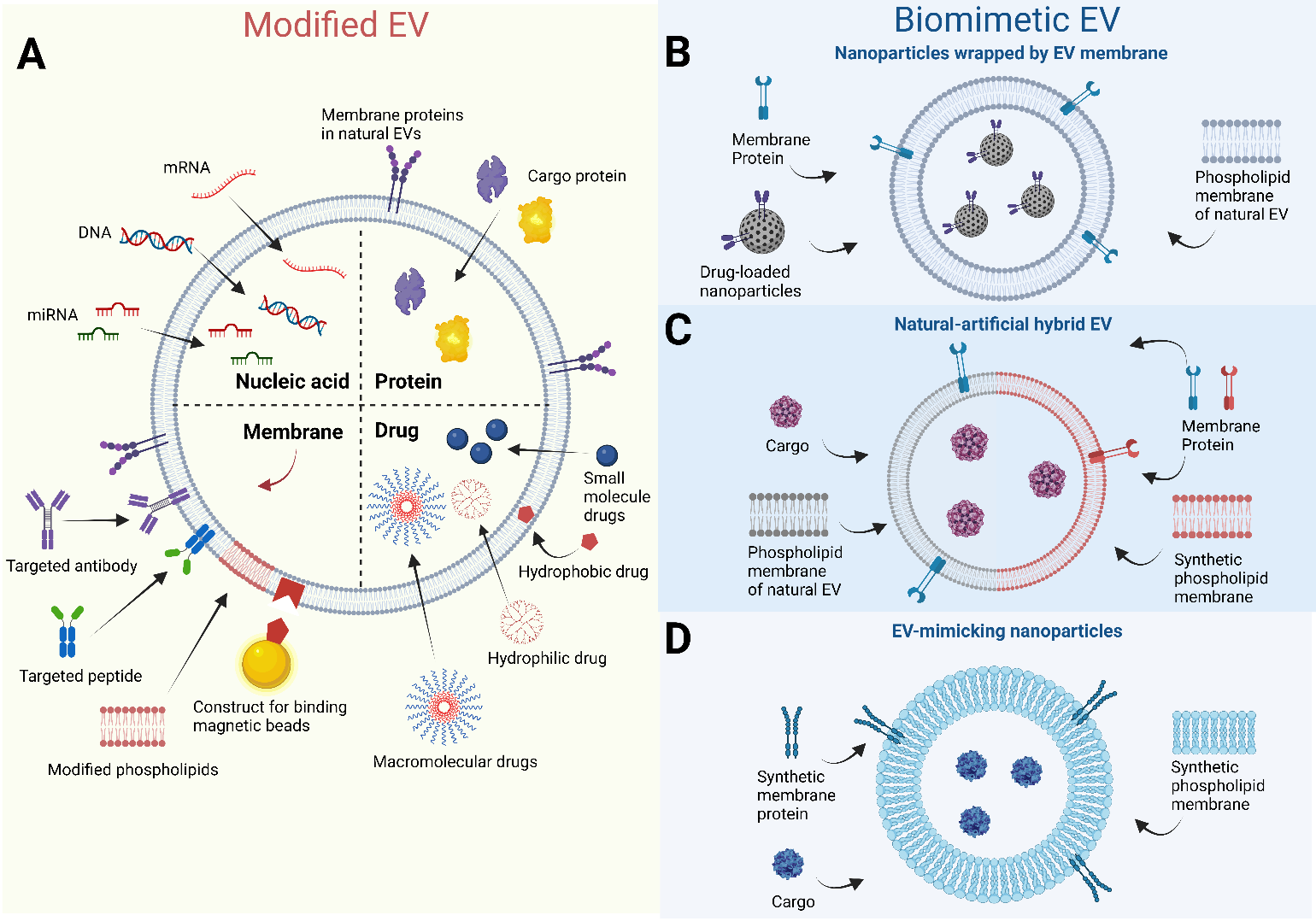
此外,还有一类工程化细胞外囊泡(EEV),这类囊泡经过修饰载药后能以特异性靶向方式参与TBI后的组织修复(图2)。目前改造EEV的主要策略分别为修饰EVs和仿生EVs。修饰EVs是指将核酸、蛋白质和药物装载到EVs中,或使用抗体、肽、磷脂和特殊材料对EVs膜进行修饰(图2A)。仿生EVs主要包括三类(图2B-D):由EVs膜包裹的纳米颗粒(即使用EVs膜来包裹纳米颗粒,图2B),天然-人工混合EVs(即生物膜系统与合成膜重组的EVs,图2C),以及仿EVs纳米颗粒(即利用蛋白质和脂质等生物材料模仿天然EVs合成仿EVs,图2D)。
图 2: EEV的设计和主要类型。 Abbreviations: EVs: extracellular vesicles.
当TBI发生后,神经细胞出现变性和坏死(图3a)并释放PEV(图3b);PEV进一步加重神经细胞损伤(图3a&c);PEV和VWF结合成复合物显著增加血脑屏障的通透性,进一步破坏血脑屏障正常结构(图3d),因此PEV通过受损的血脑屏障进入外周循环;外周循环中的PEV激活血小板并使其释放更多的EVs,而EVs触发并传播凝血级联反应,导致血栓形成并最终导致凝血功能障碍(图3f);同时,循环中的PEV激活免疫细胞以触发炎症反应(图3e)。活化的免疫细胞不仅可以通过受损的血脑屏障进入脑实质(图3h),加剧神经细胞损伤(图3i)和PEV释放(图3b),而且与PEV协同作用,导致受体细胞变性坏死(图3g),最终引起全身并发症;此外,持续的炎症和神经损伤增加了患神经退行性疾病的风险(图3a、b &c)。因此,基于EVs的TBI治疗有两种策略。首先,抑制PEV的功能,例如,通过lactadherin加速PEV的清除(图3j),通过ANV-6L15抑制PEV的促凝功能(图3k),以及通过肝素抑制受体细胞对PEV的摄取(图3l)。其次,可以增加BEV,如免疫细胞/MSC-EV(图3m)或输注EEV(图3n),它们将发挥抗炎作用并促进组织修复。同时,BEV和EEV还可以携带保护因子通过血脑屏障到达脑实质发挥保护作用(图3o)。总之,基于EVs的TBI治疗策略可以有效预防神经细胞损伤和PEV的释放(图3p);此外,BEV和EEV还可以修复受损的神经细胞并促进神经再生(图3q)。
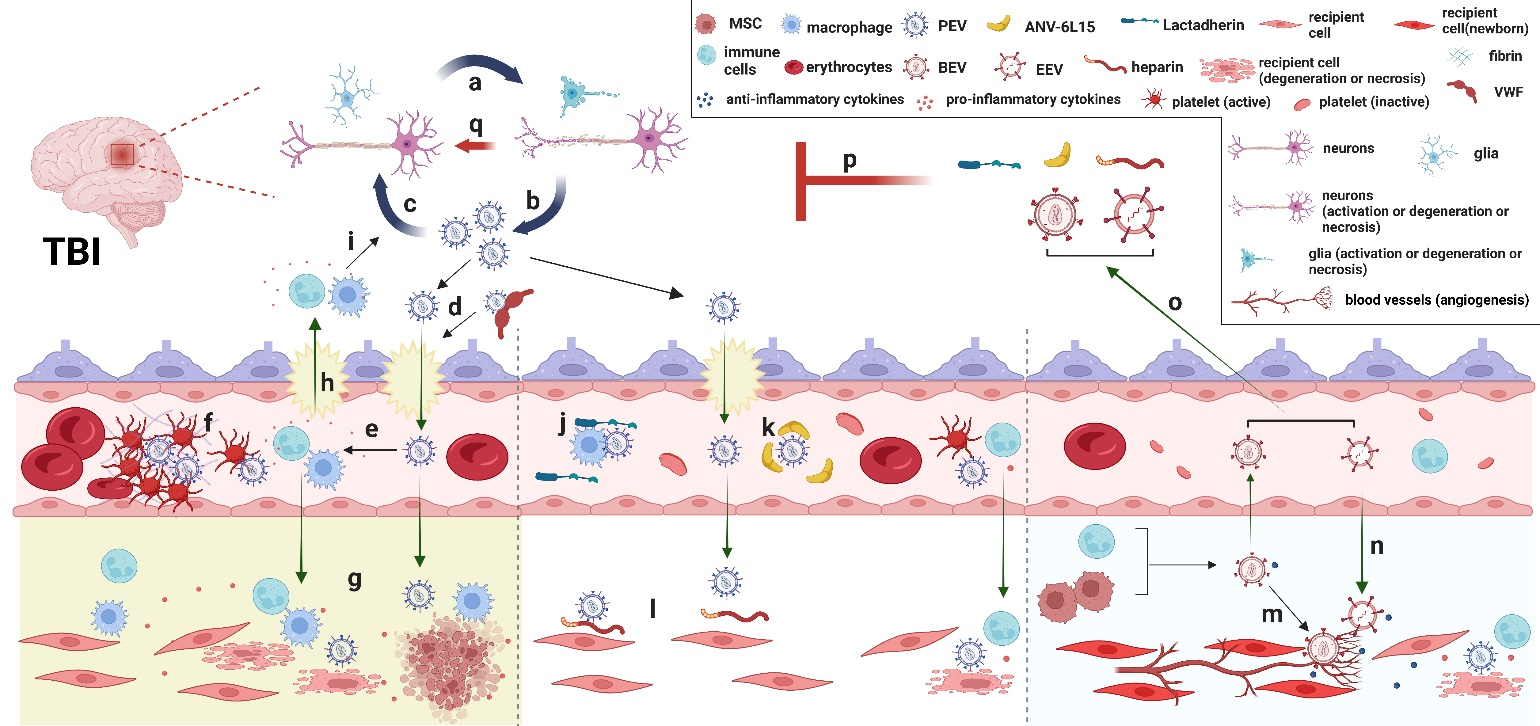
图 3: 基于EVs的TBI治疗策略
Abbreviations: ANV-6L15: ANV-6L15 fusion protein; BBB: blood-brain barrier; BEV: biological extracellular vesicles; EEV: engineered special purpose extracellular vesicles; EVs: extracellular vesicles; MSC: mesenchymal stromal cells; PEV: pathological extracellular vesicles; TBI: Traumatic brain injury; VWF: von Willebrand factor.
综上所述,基于EVs的TBI治疗策略应遵循以下原则:消除或抑制PEV的病理作用,以最大限度地减少其对TBI患者造成的二次损伤,同时促进BEV的修复作用或输注载药的EEV,有针对性地改善TBI患者的预后。此外,EEV的设计必须全面评估EVs内容物和膜结构对TBI的可能影响,从而最大限度地提高其对TBI患者康复的益处。
参考文献:
Roles and therapeutic potential of different extracellular vesicle subtypes on traumatic brain injury. Cell Commun Signal, 2023, 21(1), 211. doi:10.1186/s12964-023-01165-6
外泌体资讯网 Cell Commun Signal |首都医科大学附属北京天坛医院董信龙:不同细胞外囊泡亚型在创伤性脑损伤中的作用及治疗潜力