病理性新生血管的形成是糖尿病视网膜病变(DR)、早产儿视网膜病变(ROP)、年龄相关性黄斑变性(AMD)和视网膜静脉阻塞(RVO)等几种常见的眼部致盲性疾病的典型特征,并伴有视网膜炎症和神经变性。目前的临床治疗包括玻腔注射anti-VEGF药物、视网膜激光光凝和玻璃体切除术。虽然玻腔注射anti-VEGF药物可以抑制视网膜新生血管的进一步形成,但随着临床的应用研究者发现目前仍有部分患者对anti-VEGF药物治疗反应不佳,并且腔注射anti-VEGF药物在眼部及全身存在一些不良反应。因此,需要探索更加安全有效的治疗策略。近日,天津医科大学眼科医院李筱荣教授和张晓敏教授团队于Journal of Nanobiotechnology (JCR Q1 IF:10.2)发表题为 “Enhanced therapeutic effect ofPEDF-loaded mesenchymal stem cell-derived small extracellular vesicles against oxygen-induced retinopathy through increased stability and penetrability of PEDF”的研究论文(DOI: 10.1186/s12951-023-02066-z)。天津医科大学眼科医院李筱荣教授和张晓敏教授为论文的通讯作者,樊蕊嫣博士为第一作者,天津医科大学眼科医院、眼视光学院、眼科研究所为第一单位。该研究初步证实了装载色素上皮衍生因子(PEDF)的间充质干细胞来源的小细胞外囊泡(PEDF-sEVs)在眼底疾病中的潜在应用价值。
色素上皮衍生因子具有抗血管生成、抗炎、抗氧化和神经保护的作用,然而由于生物稳定性较差限制了该药物的临床转化。小细胞外囊泡(sEVs)因其粒径小、免疫原性低和可生物降解等特点被认为是理想的药物载体。在这项研究中,李筱荣教授和张晓敏教授团队通过超声的方法成功地制备了装载PEDF的间充质干细胞的小细胞外囊泡,利用视网膜内皮细胞(HRECs)构建了内皮细胞增殖模型,发现PEDF-sEVs有效地抑制了VEGF诱导的内皮细胞的增殖、迁移及成管,并降低了炎症相关因子的表达,具有显著的抗新生血管和抗炎的作用。在体内实验中,研究人员采用氧诱导视网膜病变(OIR)小鼠模型,发现PEDF-sEVs具有显著的抗新生血管生成、抗炎及神经保护的作用,并且相较于anti-VEGF药物,PEDF-sEVs在OIR小鼠中比表现出了更好的抗炎和神经保护的作用,证明了PEDF-sEVs在治疗眼底新生血管疾病中的潜在治疗价值。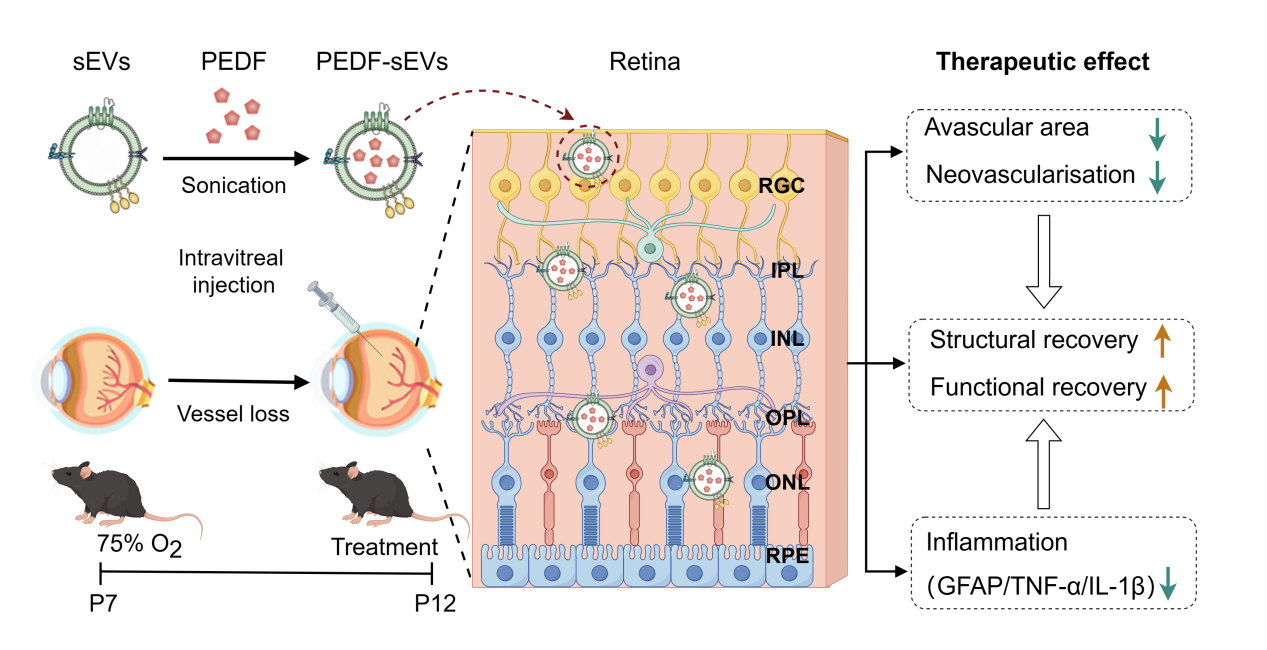
在体内外实验中,PEDF-sEVs比单独的PEDF和sEVs作用效果更显著,为了进一步明确PEDF-sEVs的作用效果,该团队利用DiD和FITC分别标记sEVs和PEDF,通过共聚焦、流式细胞术和ELISA等方法对共孵育的HRECs和玻腔注射的小鼠视网膜组织进行示踪,证明了PEDF-sEVs是一种高效的药物递送系统,可以保护PEDF减少其降解,并显著增强PEDF的组织渗透性,从而增强PEDF的作用效果。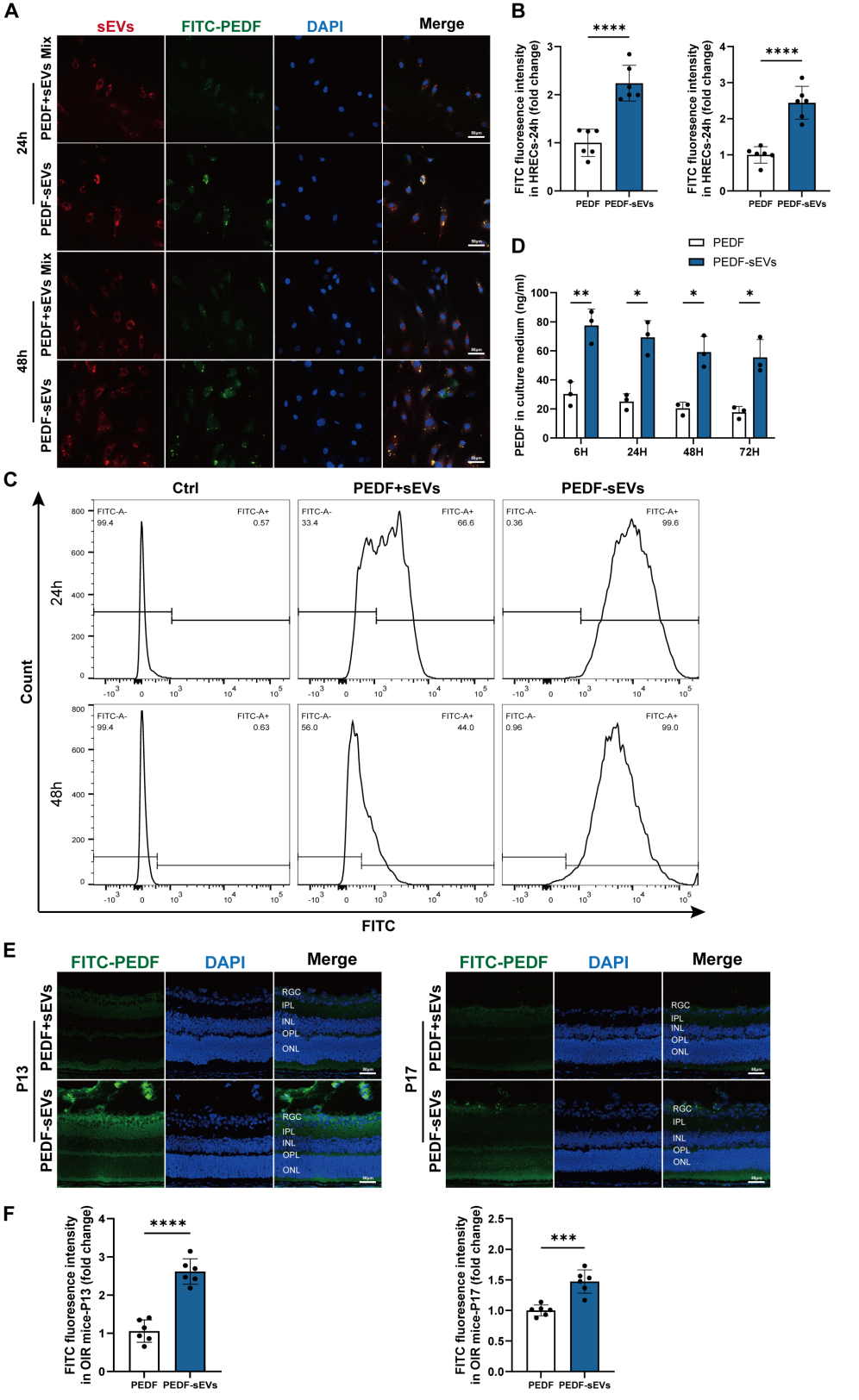
综上,该团队证明了PEDF-sEVs可以增强PEDF的稳定性和组织渗透性,具有显著的抗新生血管生成、抗炎及神经保护的作用,为眼底新生血管疾病的治疗提出了新的策略与方法。Enhanced therapeutic effect of PEDF-loaded mesenchymal stem cell-derived small extracellular vesicles against oxygen-induced retinopathy through increased stability and penetrability of PEDF, J Nanobiotechnology. 2023 Sep 8;21(1):327. doi: 10.1186/s12951-023-02066-z.外泌体资讯网 J Nanobiotechnology|天津医科大眼科医院李筱荣/张晓敏:MSC-sEVs在眼底新生血管疾病中的应用价值







