胰腺导管腺癌(PDAC)是一种严重的癌症类型,其恶性进展是肿瘤与其周围微环境之间多重相互作用的结果。特别是,PDAC的特点是存在免疫抑制的微环境,有利于癌症的生长,对免疫治疗非常有抵抗力。细胞外囊泡(EVs)是生理和病理过程中细胞间通信的不可或缺的介质。来自澳大利亚科廷大学的研究人员总结了目前对肿瘤细胞间通讯和免疫微环境的认识,强调了细胞外囊泡在恶性肿瘤中的作用,讨论了如何将EV在肿瘤免疫逃逸中的作用转化为临床应用。相关综述性内容以“Immune evasion on the nanoscale: Small Extracellular Vesicles in Pancreatic Ductal Adenocarcinoma immunity”为题在线发表于9月23日的国际知名回顾性肿瘤学期刊Seminars In Cancer Biology上。
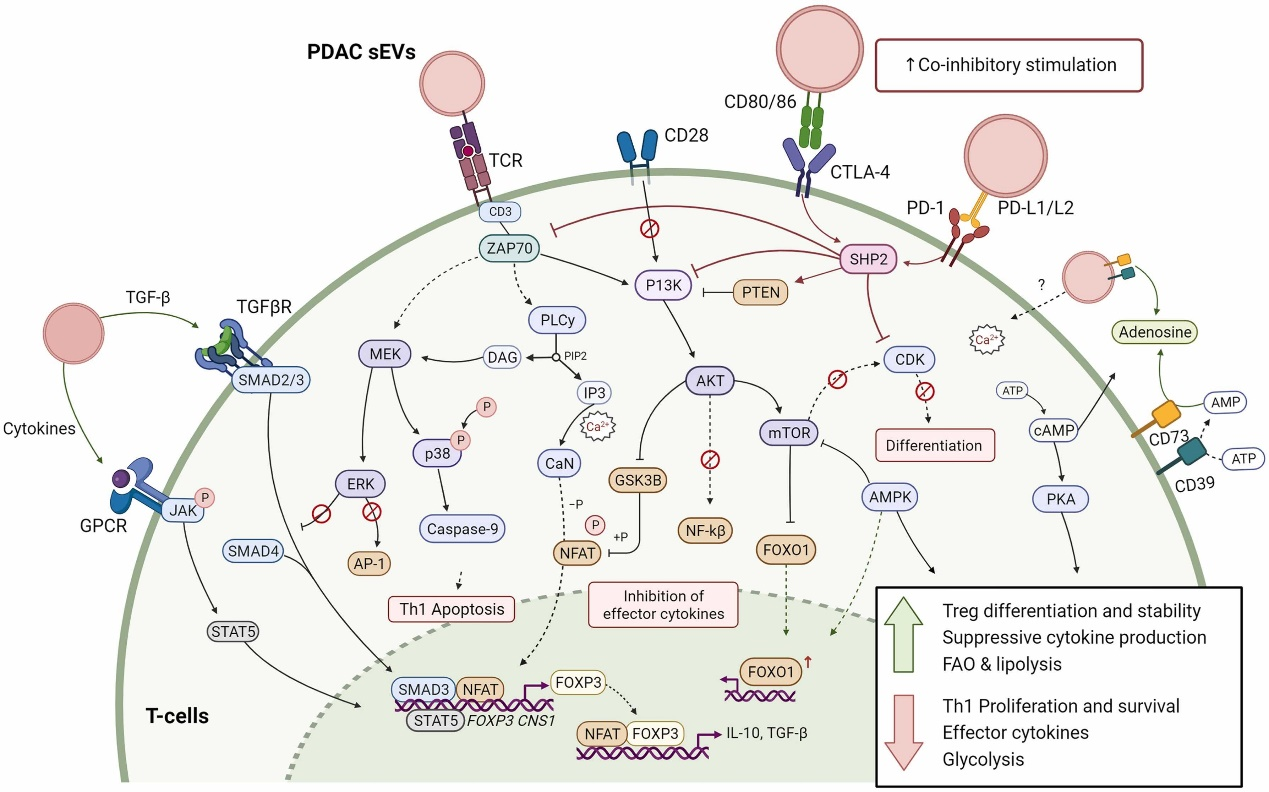
图:肿瘤来源EV介导T细胞免疫抑制中的机制。
胰腺导管腺癌(Pancreatic ductal adenocarcinoma,PDAC)是侵袭性最强的隐形恶性肿瘤之一。在疾病早期阶段,PDAC没有明显的症状,也没有可靠的、可量化的、无创的生物标志物来帮助PDAC在早期被发现。80%的PDAC病例在诊断时表现为局部肿瘤侵袭或远处转移,无法采用手术切除。此外,细胞毒性和免疫疗法(如检查点抑制剂)仅能提供有限的生存益处,并且通常伴有明显的副作用。有趣的是,特异性免疫疗法(如肿瘤抗原抗体、肿瘤蛋白疫苗)与改善PDAC患者的免疫应答和总生存率相关。这表明基于免疫的治疗可以刺激抗肿瘤反应,尽管这些疗法受到低突变负荷和免疫抑制性肿瘤微环境(TME)的限制。例如,髓源性抑制细胞(MDSCs)和肿瘤相关巨噬细胞(TAM)通过抑制T细胞反应促进肿瘤发生和免疫入侵。
肿瘤微环境(TME)内复杂的细胞间通讯网络促进了PDAC的进展。近年来,细胞外囊泡(EVs),特别是小EVs(sEV)因其在TME内介导肿瘤、基质和免疫细胞之间的通讯中的作用而受到重视。sEV是脂质结合的无核颗粒,从所有细胞中释放出来,这些细胞含有源自其起源细胞的蛋白质、脂质、核酸和其他功能性生物分子。不同细胞类型或同一细胞类型在不同条件下释放的sEV在大小和含量上存在差异,这使得这些囊泡具有独特性和高度异质性。此外,sEV的生物发生依赖于主动的货物招募,并提供了亲本细胞胞内环境的“实时”指示物质。
在PDAC中,来自肿瘤细胞的sEV通过转移各种生物分子(包括蛋白质、脂质和核酸)、改变信号转导和改变细胞功能来影响邻近的免疫细胞。例如,PDAC衍生的sEV可以诱导巨噬细胞的肿瘤表型前极化,抑制效应T细胞反应,从而促进免疫抑制和抗肿瘤免疫。因此,了解sEV与免疫细胞之间的通讯可能为提高PDAC免疫治疗的疗效提供新的策略。
在这篇综述中,研究人员总结了PDAC中小EV(sEV)在免疫反应、免疫逃避和癌症进展方面的现有知识。此外,研究人员还讨论了sEV作为筛选和预测疾病进展的生物标志物的地位,以及它们作为增加肿瘤治疗反应、帮助患者更好生存的治疗载体的潜力。
研究人员认为,PDAC具有高致死率和难治性,目前广泛的研究集中在了解驱动PDAC的致癌行为和增加其对治疗的反应。不幸的是,尽管在该领域取得了重大进展,但PDAC仍然定义不清,缺乏明确的、非侵入性的诊断或预后标记物,治疗干预方面也没有什么进展。由肿瘤相关细胞(如基质细胞和免疫细胞)释放的sEV在由TME决定的分子谱中是独特的。这些信息提供了前所未有的进入肿瘤核心的途径,被证明对理解微环境中细胞的致癌行为至关重要,因此可以作为疾病进展、可能的并发症和预后的标志。鉴于肿瘤发生的性质,PDAC特异性生物标志物尚未建立,目前已确定的生物标志物要么无法证明一致性,要么也在不同起源的癌症中都可以观察到。因此,建立sEV的多组学方法来识别和分级PDAC肿瘤可能会提高检测的敏感性,对治疗结果有显著预测价值。
原发肿瘤和免疫细胞之间EV介导的通讯的了解,为更好地诊断或治疗PDAC提供了许多机会。例如,通过影响其释放或摄取,或通过阻断其携带的特定介质来抑制癌症源性EV,可以避免癌症源性EV对免疫细胞的影响,或潜在地增强免疫治疗的效果。这意味着有必要收集更多关于EV所携带货物的特定目标的信息,并提高我们对EV释放和受体细胞摄取机制的认识。至于EV作为生物标志物的潜在应用,为了在血液采集的基础上收集可重复的信息,仍有许多问题需要解决。污染物的存在、所收集样本的低浓度以及由于存在不同的EV亚群而缺乏特异性仍然是EV作为生物标志物在临床大量使用的障碍。尽管如此,EV是目前为数不多的新的可行选择之一,可用于开发诊断和治疗具有挑战性的癌症(如PDAC)的有效工具。
参考文献:Immune evasion on the nanoscale: Small Extracellular Vesicles in Pancreatic Ductal Adenocarcinoma immunity. Semin Cancer Biol. 2023 Sep 23:S1044-579X(23)00126-8.