近年来,基于肿瘤新生抗原的个体化免疫治疗受到肿瘤治疗领域的广泛关注,然而临床试验结果显示:基于肿瘤新生抗原肽疫苗激活广谱T细胞免疫应答效率较低,特别是对肿瘤新生抗原缺乏有效的特异性识别,是个体化免疫治疗面临的挑战。其中肿瘤新生抗原淋巴结靶向递送效率有限,导致免疫细胞摄取、识别及提呈能力弱。如何提高肿瘤新生抗原肽疫苗淋巴结递送效率,增强肿瘤新生抗原免疫原性,对基于肿瘤新生抗原的个体化肿瘤免疫治疗具有重要意义。
近日,天津医科大学医学技术学院&基础医学院尹海芳教授团队在国际权威期刊Molecular Therapy在线发表了题为“Complete remission of tumors in mice with neoantigen-painted exosomes and anti-PD1 therapy”的研究成果(2023 Nov 1:S1525-0016(23)00598-1)。该研究首次报道了基于血清来源外泌体介导肿瘤新生抗原个体化免疫治疗的新策略。天津医科大学基础医学院博士研究生张杨和青年教师左冰峰为文章的共同第一作者,尹海芳教授为通讯作者。
在前期的研究工作中,尹海芳教授课题组一直致力于DC细胞来源外泌体(DEX)在肿瘤免疫治疗中的研究。然而,DEX存在着DC细胞获取困难,培养繁琐,技术难度大等局限性,极大限制了其临床应用。在这项工作中,尹海芳教授团队基于课题组创建的外泌体表面功能化修饰平台技术(Sci Transl Med,2018),利用外泌体锚定肽-CP05分别将多种肿瘤新生抗原共负载于血清来源外泌体表面,获得新型功能化生物纳米疫苗。首次证实了自体血清来源的外泌体通过皮下免疫的方式能够促进肿瘤新生抗原疫苗的淋巴结靶向递送,增强DC对抗原高效摄取和交叉提呈,提高肿瘤新生抗原的免疫原性,激活肿瘤新生抗原特异性抗肿瘤免疫应答效应,有效抑制小鼠黑色素瘤和结肠癌肿瘤的生长。
更为重要的是,研究人员将负载MC38新抗原Adpgk和Reps1的血清外泌体疫苗EXOA&R联合免疫检查点抑制剂PD-1抗体治疗后发现,联合治疗进一步增强了抗肿瘤免疫原性,三分之二的结肠癌核瘤小鼠出现肿瘤的完全清除,并在二次荷瘤后,仍实现了百分之百的存活,诱导了长效的肿瘤特异性T细胞免疫记忆。同时,研究人员利用人3D肿瘤球技术,在人结肠癌3D肿瘤球模型上创新性探究了其临床适用性,彰显了血清来源外泌体介导新抗原个体化免疫治疗的应用潜力。
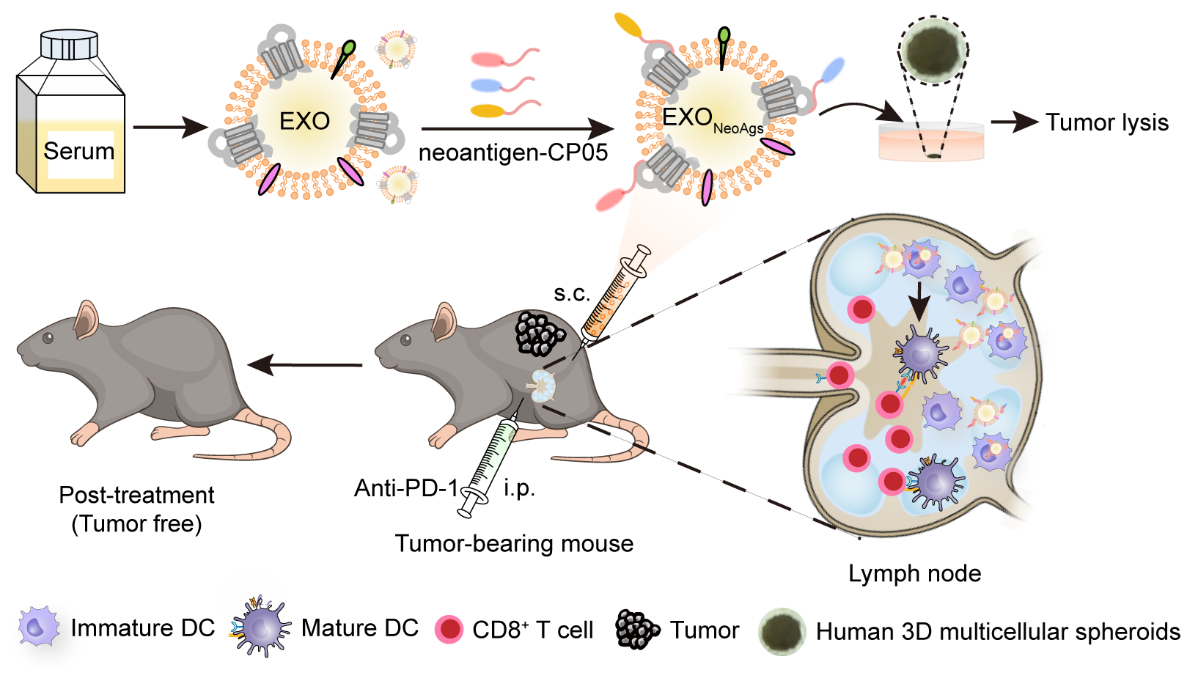 图. 血清来源外泌体介导新抗原个体化肿瘤免疫治疗示意图
图. 血清来源外泌体介导新抗原个体化肿瘤免疫治疗示意图
该研究首次证明了自体血清来源外泌体通过皮下免疫的方式能够促进肿瘤新生抗原疫苗淋巴靶向递送,增强DC细胞对抗原高效摄取和交叉提呈,从而增强疫苗免疫原性,介导有效的抗原特异性免疫应答效应。同时,在人肿瘤模型上也验证了其临床适用性,显示了血清来源外泌体作为新抗原疫苗运输载体介导肿瘤个体化免疫治疗的应用潜力。为基于肿瘤新生抗原的个性化免疫治疗提供了新策略。该研究得到了国家自然科学基金委重点项目及其他省部级等基金支持。
参考文献:
Complete remission of tumors in mice with neoantigen-painted exosomes and anti-PD1 therapy, Mol Ther. 2023 Nov 1:S1525-0016(23)00598-1. doi: 10.1016/j.ymthe.2023.10.021.





