外泌体(Exosomes, Exo)是由细胞内的多泡体与胞膜融合后,释放到细胞外基质中的“天然脂质纳米囊泡”,其直径为30-150 nm,包裹了来源细胞的蛋白、核酸、脂质等物质,经循环系统到达其他细胞与组织,发挥远程调控作用。因此,Exo常被视为天然的药物载体和液体活检标志物。事实上,Exo磷脂膜结构不仅可以保护其内部分子,还是高活性的配位化学位点,可与锆基金属有机框架(MOF)配位组装成功能纳米复合物,如信号放大器。基于上述思路,广西医科大学 “广西药物精准检测与筛选重点实验室”杨帆课题组近日在肿瘤外泌体(tExo)检测研究领域取得新进展,研究成果以“Exosome-tuned MOF signal amplifier boosting tumor exosome phenotyping with high-affinity nanostars”为题,发表在期刊Biosensors and Bioelectronics上 (2023 Nov 11:245:115828)。
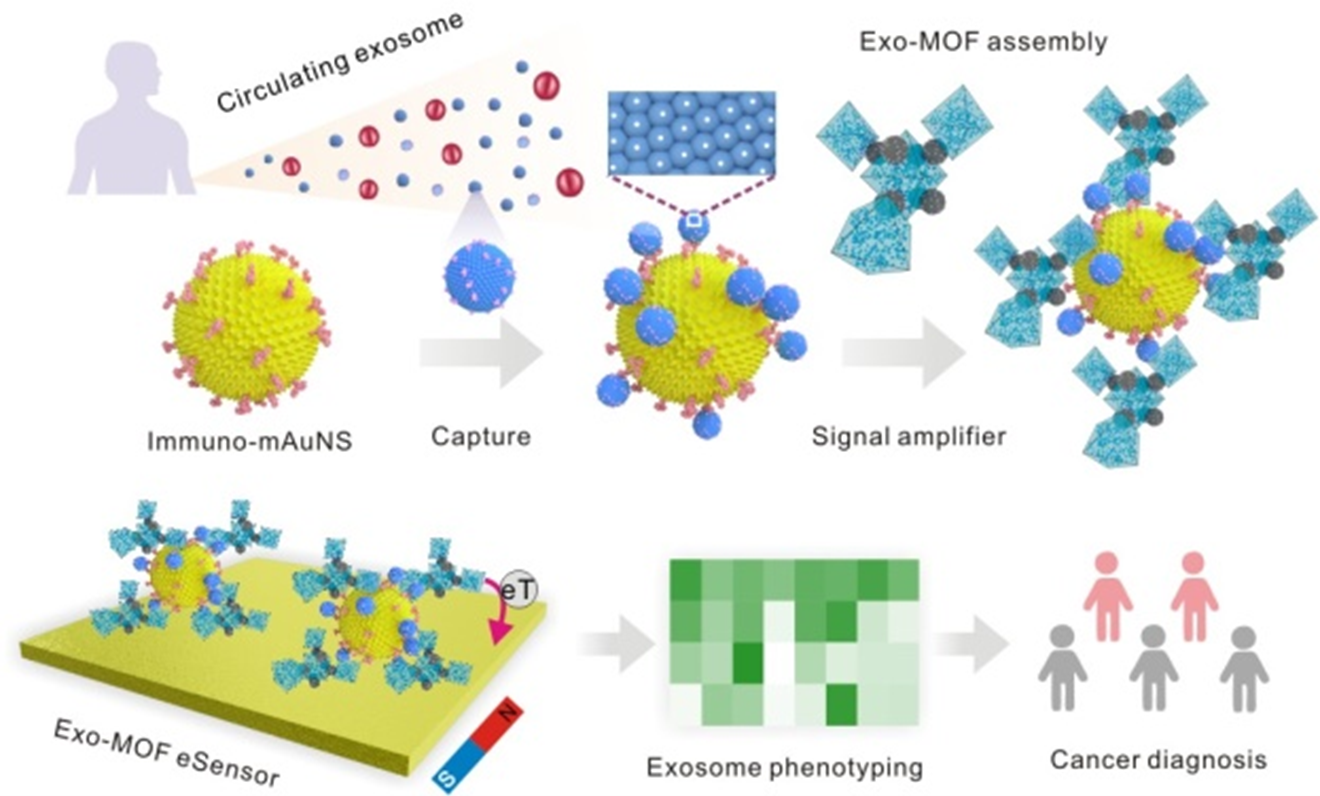
该研究团队利用正常细胞衍生的Exo来调控MOF组装成信号放大器(Exo-MOF),并协同高亲和力的纳米星(Immuno-mAuNS),实现了肿瘤来源外泌体(tExo)单颗粒水平的超灵敏表型鉴定。其特点是(1)利用Exo和封装有大量氧化还原分子(亚甲基蓝)的MOF之间的特异性配位作用,组装了一个超级氧化还原信号放大器Exo-MOF;(2)分散的免疫磁性纳米星以“无人机”方式快速捕获血浆样本中的靶标tExo,经磁场富集,解决了固态电极表面受限的分子传质问题。Exo-MOF联合免疫磁性纳米星提高了传感器(eSensor)在tExo检测中的灵敏度、特异性和速度。该方法可以检测多种癌症细胞来源的tExo,并揭示了不同Exo表面蛋白表达谱的异质性。此外,eSensor还可以在临床样本中准确区分癌症患者和健康个体(AUC=1),为生物材料组装和精准诊疗提供了新的思路。Exosome-tuned MOF signal amplifier boosting tumor exosome phenotyping with high-affinity nanostars, Biosens Bioelectron. 2023 Nov 11:245:115828. doi: 10.1016/j.bios.2023.115828.原文链接: https://doi.org/10.1016/j.bios.2023.115828外泌体资讯网 Biosens Bioelectron|广西医科大学“广西药物精准检测与筛选重点实验室”杨帆课题组在肿瘤外泌体检测领域取得新进展