11月份国内新出的细胞外囊泡/外泌体领域论文不完全统计有329篇。IF>10的有77篇。本期主要内容包括:非小细胞肺癌的淋巴转移、肌肉与骨骼的串扰、精子线粒体数量与生育力、肺纤维化、脊髓损伤修复、神经内分泌前列腺癌、缺血性损伤的血运重建、双靶向细胞纳米囊泡优化癌症免疫治疗、牛磺酸与前列腺癌、软骨代谢与衰老、肿瘤衍生微粒的个性化疫苗、染色质DNA进入细胞外囊泡的机制、血清来源外泌体介导肿瘤新抗原个体化免疫治疗新策略、树突状细胞EVs治疗重症肌无力新策略等方面内容。内容十分丰富,不容错过。全部文献列表及部分文章原文可在外泌体之家论坛同名贴下下载。
1.北京协和医院李单青&中山大学陈长昊:SUMO化触发的ALIX激活调节细胞外囊泡 circTLCD4-RWDD3以促进非小细胞肺癌的淋巴转移Diao, X., et al. (2023). "SUMOylation-triggered ALIX activation modulates extracellular vesicles circTLCD4-RWDD3 to promote lymphatic metastasis of non-small cell lung cancer." Signal Transduct Target Ther 8(1): 426. IF=39.3淋巴结(LN)转移是非小细胞肺癌(NSCLC)的主要转移途径之一,被认为是患者预后不良的主要原因之一。尽管淋巴管生成已被公认为介导LN转移的关键过程之一,但涉及淋巴管生成和LN转移的调节机制在NSCLC中仍不清楚。该研究采用高通量测序技术鉴定了一种新的环状RNA(circRNA),circTLCD4-RWDD3,该RNA在LN转移性NSCLC的细胞外囊泡(EVs)中显著上调,并与NSCLC多中心临床队列中患者的OS和DFS恶化呈正相关。下调EV包装的circTLCD4-RWDD3的表达抑制了NSCLC的淋巴管生成和LN转移,无论是体外还是体内。机制上,circTLCD4-RWDD3与hnRNPA2B1物理相互作用,并通过上调UBC9介导hnRNPA2B1的K108残基的SUMO2修饰。随后,circTLCD4-RWDD3诱导的SUMO化hnRNPA2B1被ALIX的SUMO相互作用基序(SIM)识别,并激活ALIX招募ESCRT-III,从而促进circTLCD4-RWDD3进入NSCLC细胞源性EVs的分选。此外,EV包装的circTLCD4-RWDD3被淋巴内皮细胞内吞,激活PROX1的转录,导致NSCLC的淋巴管生成和LN转移。重要的是,通过突变ALIX中的SIM或hnRNPA2B1的K108残基阻断EV介导的circTLCD4-RWDD3传递,抑制了NSCLC的淋巴管生成和LN转移。该研究发现揭示了SUMO化hnRNPA2B1诱导的EV包装circTLCD4-RWDD3在促进NSCLC LN转移中的精确机制,表明EV包装的circTLCD4-RWDD3可能是LN转移性NSCLC的潜在治疗靶点。
2.【综述】国家纳米中心孙佳姝:用于细胞外囊泡分析的DNA纳米材料Deng, J., et al. (2023). "DNA-Based Nanomaterials for Analysis of Extracellular Vesicles."Adv Mater: e2303092. IF=29.4细胞外囊泡(EV)是由细胞产生的纳米囊泡,包含大量分子载体,如蛋白质和核酸,发挥着细胞间通讯和生理和病理过程中的重要作用。EV作为无创生物标志物用于疾病诊断和预后已受到广泛关注。由于其识别蛋白质和核酸靶标的能力,具有出色的可编程性和可修饰性的基于DNA的纳米材料为检测EV携带的分子载体提供了有前途的工具。在这个角度上,总结了使用各种基于DNA的纳米材料进行EV分析的最新进展,可以广泛地分为三类:线性DNA探针,DNA纳米结构和混合DNA纳米材料。回顾了不同类型的DNA纳米材料的设计、构造、优缺点以及它们检测EV的性能。还讨论了DNA纳米材料在EV分析领域中的挑战和机遇。
3.四川大学廖立、田卫东:骨骼肌来源的细胞外囊泡运输糖酵解酶以介导肌肉与骨骼的串扰Ma, S., et al. (2023). "Skeletal muscle-derived extracellular vesicles transport glycolytic enzymes to mediate muscle-to-bone crosstalk."Cell Metab 35(11): 2028-2043.e2027. IF=29肌肉起源的信号对于理解肌肉和骨骼之间的相互作用以及开发治疗退行性骨病的方法至关重要。该报道确定了骨骼肌分泌多种细胞外囊泡(Mu-EVs)。这些Mu-EVs通过血液循环到达骨骼,被骨髓间充质干/基质细胞(BMSCs)吞噬。Mu-EVs促进了BMSC的成骨分化,并保护小鼠免受废用性骨质疏松的影响。Mu-EVs的数量和生物活性与骨骼肌的功能密切相关。蛋白质组学分析揭示了Mu-EVs中的许多蛋白质,其中一些可能调节骨代谢,特别是糖酵解。随后的研究表明,Mu-EVs通过向这些细胞输送乳酸脱氢酶A,促进了BMSC的糖酵解。总之,这些发现揭示了Mu-EVs在BMSC代谢调节和骨形成刺激中发挥着至关重要的作用,为治疗废用性骨质疏松提供了一种有前途的方法。
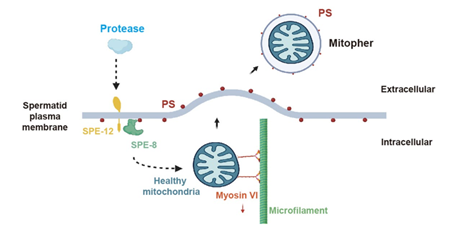
4.西湖大学唐鸿云、北京大学黄小帅:细胞外囊泡调节精子线粒体数量与生育力Liu, P., et al. (2023). "Mitopherogenesis, a form of mitochondria-specific ectocytosis, regulates sperm mitochondrial quantity and fertility."Nat Cell Biol 25(11): 1625-1636. IF=21.3
前期报道:https://www.exosomemed.com/15450.html
5.空军军医大学金发光、杨国栋:利用外泌体配方进行促纤维化巨噬细胞靶向递送线粒体保护剂以减轻肺纤维化Zhang, W., et al. (2024). "Profibrogenic macrophage-targeted delivery of mitochondrial protector via exosome formula for alleviating pulmonary fibrosis."Bioact Mater 32: 488-501. IF=18.9肺纤维化(PF)是一种毁灭性的肺部疾病,治疗选择有限。在这种病理过程中,促纤维化巨噬细胞亚群发挥着关键作用,因此对该亚群的表征至关重要。该研究揭示了肺部线粒体质量较高的巨噬细胞(Mø(mitohigh))与纤维化之间的正相关性。在CD206(+)M2的Mø(mitohigh)亚群中,通过流式细胞术和RNA-seq分析确定了表达动力蛋白1样(Drp1)较高的亚群,开发了一种基于外泌体的治疗干预方案,该方案由路径探测器和治疗剂组成。一种名为“外泌体(MMP19)(Exo(MMP19))”的路径探测器外泌体被构建出来,在表面上显示基质金属蛋白酶-19(MMP19),以局部分解纤维化肺部中过度的细胞外基质(ECM)。一种名为“外泌体(治疗)(Exo(Tx))”的治疗性外泌体被设计出来,在表面上显示D-甘露糖,同时包裹siDrp1。先前的Exo(MMP19)递送降解了过度的ECM,为Exo(Tx)递送到Mø(mitohigh)铺平了道路,在那里Exo(Tx)抑制了线粒体分裂并缓解了PF。本研究不仅确定了Mø(mitohigh)为促纤维化巨噬细胞,而且还提供了一种通过配制外泌体的组合来逆转PF的有效策略。
6.【综述】浙江大学赵斌:外泌体处于机械传感和肝脏肿瘤发生的十字路口Tang, M., et al. (2023). "Exosome at the crossroads of mechanosensing and liver tumorigenesis." Sci Bull (Beijing). IF=18.9
7.山东大学魏志坚等:雪旺细胞外泌体和甲强龙复合贴剂用于脊髓损伤修复Zhu, B., et al. (2023). "Schwann Cell-Derived Exosomes and Methylprednisolone Composite Patch for Spinal Cord Injury Repair." ACS Nano 17(22): 22928-22943.IF=17.1脊髓损伤(SCI)可能会导致感觉和运动功能的永久性丧失,目前还没有有效的临床治疗方法。由于损伤后涉及的复杂病理过程,临床实践中非常迫切需要协同治疗。该研究设计了一种纳米纤维支架透明质酸水凝胶贴片,以非侵入性方式释放外泌体和甲基泼尼松龙到受伤的脊髓。该复合贴片在稳定外泌体形态和对神经细胞的毒性方面表现出良好的生物相容性。同时,该复合贴片在体外研究中增加了M2型巨噬细胞的比例,并减少了神经元凋亡。在体内,SCI大鼠的功能和电生理表现在复合贴片覆盖血肿表面时得到了显著改善。该复合贴片通过将巨噬细胞极化从M1型到M2型来抑制炎症反应,并通过抑制SCI后神经元凋亡来增加神经元的存活率。该复合贴片的治疗效果可以归因于TLR4/NF-κB、MAPK和Akt/mTOR通路。因此,该复合贴片提供了一种药物-外泌体双重释放系统,可能为SCI患者提供一种非侵入性的临床治疗方法。
8.上海交通大学仁济医院薛蔚等:ELAVL3/MYCN正反馈环路为神经内分泌前列腺癌提供了治疗靶点Ji, Y., et al. (2023). "The ELAVL3/MYCN positive feedback loop provides a therapeutic target for neuroendocrine prostate cancer." Nat Commun 14(1): 7794. IF=16.6神经内分泌前列腺癌是一种快速进展和致命的疾病,其特征为早期内脏转移、预后差和治疗选择有限。揭示致癌机制可能会促进潜在的治疗途径的发现。该研究证明RNA结合蛋白ELAVL3在神经内分泌前列腺癌中特异性上调,并且ELAVL3的过度表达足以诱导前列腺腺癌的神经内分泌表型。在机制上,ELAVL3受MYCN转录调节,随后结合并稳定MYCN和RICTOR mRNA。此外,ELAVL3被证明在细胞外囊泡中释放并通过细胞间机制诱导腺癌细胞的神经内分泌分化。药物抑制ELAVL3,如已获FDA批准的吡维酮帕莫酸,有效抑制肿瘤生长,降低转移风险,并改善神经内分泌前列腺癌小鼠模型的生存率。该结果确定了ELAVL3作为前列腺癌神经内分泌分化的关键调节因子,并提出了一种药物再利用策略,用于靶向治疗。
9.中山大学药学院冯敏等:通过NO增强的细胞外囊泡增强周细胞-内皮相互作用,驱动缺血性损伤小鼠模型的血运重建Guo, L., et al. (2023). "Enhanced pericyte-endothelial interactions through NO-boosted extracellular vesicles drive revascularization in a mouse model of ischemic injury." Nat Commun 14(1): 7334. IF=16.6尽管医疗和外科治疗有所改进,但是相当一部分的重度肢体缺血(CLI)患者被认为“无法进行再血管化手术”。本研究构建了一种通过在干细胞衍生的纳米尺度细胞外囊泡上装饰NO纳米笼来增强和激活一氧化氮(NO)的纳米囊泡再生工具包(n-BANK)。该研究结果表明,n-BANKs可以在内皮细胞中储存NO,以便在周转细胞招募CLI再血管化时释放。值得注意的是,n-BANKs使内皮细胞能够触发eNOS激活并形成管状结构。随后,eNOS衍生的NO强烈招募周转细胞投资新生内皮细胞管,从而产生成熟的血管。因此,n-BANKs在CLI后完全再血管化了雌性小鼠,从而实现了肢体保护和恢复运动功能。鉴于n-BANK通过诱导周转细胞-内皮细胞相互作用来创建功能性血管网络,具有在再血管化中降低CLI相关截肢的潜在治疗潜力,这可能影响再生医学。
10.中国医学科学院:工程设计高亲和力双靶向细胞纳米囊泡以优化癌症免疫治疗Zhang, L., et al. (2023). "Engineering high-affinity dual targeting cellular nanovesicles for optimised cancer immunotherapy." J Extracell Vesicles 12(11): e12379. IF=16双重免疫检查点的双重靶向比单一靶向实现了更好的治疗效果,因为它能够协同促进肿瘤免疫。然而,大多数双重靶向策略通常依赖于抗体,面临抗体的缺点,如穿透固体肿瘤能力差和亲和力不足。为了应对这些挑战,该研究设计了一种细胞膜,其中显示了由SIRPα和PD-1变体组成的融合蛋白,野生型分子的高亲和共识(HAC),并用其制备了纳米囊泡(NVs)。通过禁用SIRPα/CD47和PD-1/PD-L1信号,HAC NVs分别显著保留了巨噬细胞和T细胞的吞噬作用和抗肿瘤作用。体内研究表明,与表达野生型融合蛋白的NVs相比,HAC NVs具有更好的肿瘤穿透能力和更高的结合亲和力,能够与肿瘤细胞上的CD47和PD-L1结合。令人振奋的是,HAC NVs通过CD47和PD-L1的双重阻断表现出了出色的治疗效果和生物安全性。本研究提供了一种新型的抗肿瘤免疫逃逸生物材料,更重要的是提供了一种多靶向治疗的生物仿生技术。
11.上海交通大学仁济医院方煜翔等:牛磺酸抑制前列腺癌中肿瘤细胞和肿瘤相关巨噬细胞之间的串扰介导的铁死亡Xiao, H., et al. (2023). "Taurine Inhibits Ferroptosis Mediated by the Crosstalk between Tumor Cells and Tumor-Associated Macrophages in Prostate Cancer." Adv Sci (Weinh): e2303894. IF=15.1肿瘤相关巨噬细胞(TAM)在肿瘤治疗抵抗中发挥着至关重要的作用。虽然铁死亡对肿瘤细胞的致命作用已经得到了充分的报道,但TAM如何抑制肿瘤中铁死亡的作用尚未得到明确的定义。本研究表明,TAM分泌的牛磺酸通过激活肝X受体α/硬脂酰辅酶A去饱和酶1(LXRα/SCD1)通路,在前列腺癌(PCa)中抑制铁死亡。通过抑制牛磺酸转运蛋白TauT的牛磺酸摄入,可以恢复肿瘤对铁死亡的敏感性。此外,LXRα激活miR-181a-5p及其结合蛋白FUS的转录,增加肿瘤来源的细胞外囊泡(EVs)中miR-181a-5p的招募。观察到巨噬细胞似乎是miR-181a-5p富集的EV的受体细胞。巨噬细胞中miR-181a-5p的摄入促进了它们的M2极化,并通过抑制其靶基因lats1的表达增强了牛磺酸的输出,从而失活了河马通路,并导致Yes相关蛋白(YAP)核转位,转录激活了M2极化相关基因,如ARG1和CD163以及牛磺酸转运基因TauT。总之,这些发现表明,PCa细胞和TAM之间存在相互作用,形成了一个正反馈环路,以通过TAM分泌的牛磺酸和肿瘤EV传递的miR-181a-5p抑制PCa中的铁死亡。
12.台湾大学:超灵敏的肿瘤细胞外囊泡蛋白的空间分布检测Cheng, C. A., et al. (2023). "Ultrasensitive and High-Resolution Protein Spatially Decoding Framework for Tumor Extracellular Vesicles." Adv Sci (Weinh): e2304926. IF=15.1前期报道:https://www.exosomemed.com/15511.html
13.南方医科大学珠丁长海、汤苏安:骨关节炎患者髌下脂肪垫中的细胞外囊泡会损害软骨代谢并诱导衰老Cao, Y., et al. (2023). "Extracellular Vesicles in Infrapatellar Fat Pad from Osteoarthritis Patients Impair Cartilage Metabolism and Induce Senescence."Adv Sci (Weinh): e2303614. IF=15.1髌脂垫(IPFP)与膝骨关节炎(OA)的发展和进展密切相关,但其潜在机制尚不清楚。该研究发现来自OA患者的IPFP可以分泌小型细胞外囊泡(sEVs)并将其输送到关节软骨细胞中。通过GW4869抑制内源性骨关节炎IPFP-sEVs的释放,显著缓解了IPFP-sEVs诱导的软骨破坏。体外功能分析表明,IPFP-sEVs显著促进了软骨细胞的细胞外基质(ECM)分解代谢并诱导了细胞衰老。进一步证明了IPFP-sEVs在人和小鼠软骨外植物中诱导了ECM降解并加重了小鼠实验性OA的进展。从机理上讲,IPFP-sEVs中高度富集的let-7b-5p和let-7c-5p对于通过直接降低衰老负调节因子lamin B受体(LBR)来介导有害效应至关重要。值得注意的是,小鼠关节内注射抗反义物抑制let-7b-5p和let-7c-5p增加了LBR表达,抑制了软骨细胞衰老并改善了实验性OA模型的进展。本研究揭示了IPFP-sEVs在OA进展中的功能和机制。针对IPFP-sEVs的let-7b-5p和let-7c-5p的靶向可以为OA治疗提供潜在策略。
14.德州大学王吉华:EVLncRNAs 3.0——经过低通量实验验证的手动策划的功能性长非编码RNA的更新综合数据库Zhou, B., et al. (2023). "EVLncRNAs 3.0: an updated comprehensive database for manually curated functional long non-coding RNAs validated by low-throughput experiments."Nucleic Acids Res. IF=14.9
15.华中科技大学杨坤禹:将辐照肿瘤衍生微粒设计为个性化疫苗以增强抗肿瘤免疫力Sun, Y., et al. (2023). "Engineering irradiated tumor-derived microparticles as personalized vaccines to enhance anti-tumor immunity."Cell Rep Med: 101303. IF=14.3抗原呈递细胞的不足激活、T细胞以及肿瘤微环境(TME)中高度免疫抑制的条件是限制癌症疫苗有效性的重要因素。研究表明,个性化和广泛的抗原库完全激活了抗肿瘤免疫力,并且抑制转化生长因子(TGF)-β的功能有助于T细胞的迁移。该研究引入了一种疫苗策略,通过工程化放射性肿瘤细胞衍生的微粒子(RT-MPs),这些微粒子具有个性化和广泛的抗原库,以诱导全面的抗肿瘤效应。受到严重急性呼吸综合症冠状病毒2(SARS-CoV-2)的刺激蛋白的促炎症作用和TGF-β受体2(TGFBR2)与TGF-β之间的高亲和力的鼓舞,该研究开发了带有SARS-CoV-2刺突蛋白和TGFBR2的RT-MPs。这种刺突蛋白和高TGFBR2表达诱导先天免疫反应,改善免疫抑制的TME,从而促进T细胞的激活和浸润,最终抑制肿瘤生长。该研究提供了一种生产有效的个性化抗肿瘤疫苗的策略。
16.湖南大学谭拥军:转录因子FOXM1将染色质DNA定向到细胞外囊泡Zhang, Y., et al. (2023). "Transcription factor FOXM1 specifies chromatin DNA to extracellular vesicles."Autophagy. IF=13.3细胞外囊泡DNA(evDNAs)对于各种疾病具有重要的诊断价值,并促进了遗传物质的细胞间转移。该研究确定了转录因子FOXM1作为指导染色质基因或DNA片段(称为FOXM1-chDNAs)定向到细胞外囊泡(EVs)的介质。FOXM1在细胞核中与MAP1LC3 / LC3结合,而FOXM1-chDNAs(例如DUX4基因和端粒DNA)则由FOXM1结合并转移到细胞质中,然后通过涉及LC3的分泌性自噬在溶酶体抑制(SALI)过程中释放到EVs中。破坏FOXM1表达或SALI过程会影响FOXM1-chDNAs纳入EVs。通过EVs可以将FOXM1-chDNAs传递给受体细胞,并在携带功能基因的受体细胞中表达。这一发现提供了转录因子FOXM1如何将染色质DNA片段指定为EVs的示例,揭示了其对从核染色质形成evDNAs的贡献。它为进一步探索evDNAs在生物过程中的作用,例如水平基因转移,提供了基础。
17.中国科学院深圳先进技术研究院蔡林涛:表达Siglec-10伪装AIE光敏剂的工程细胞外囊泡可将巨噬细胞重编程为活性M1表型并呈递肿瘤相关抗原,用于光动力免疫治疗Sun, Z., et al. (2023). "Engineered Extracellular Vesicles Expressing Siglec-10 Camouflaged AIE Photosensitizer to Reprogram Macrophages to Active M1 Phenotype and Present Tumor-Associated Antigens for Photodynamic Immunotherapy." Small: e2307147. IF=13.3
18.四川大学童南伟:多功能DNA水凝胶促进糖尿病牙槽骨缺损重建Peng, G., et al. (2023). "Multifunctional DNA-Based Hydrogel Promotes Diabetic Alveolar Bone Defect Reconstruction." Small: e2305594.IF=13.3
19.南京医科大学等:富含miR-29a的BMSC外泌体多功能可注射水凝胶微粒,通过调节成骨和血管生成来增强骨再生Pan, S., et al. (2023). "Multifunctional Injectable Hydrogel Microparticles Loaded with miR-29a Abundant BMSCs Derived Exosomes Enhanced Bone Regeneration by Regulating Osteogenesis and Angiogenesis." Small: e2306721.IF=13.3
20.南京医科大学徐泽宽:幽门螺杆菌感染的胃癌细胞来源的细胞外小泡通过miR-1246的转移诱导淋巴管生成和淋巴重塑Lu, C., et al. (2023). "Small Extracellular Vesicles Derived from Helicobacter Pylori-Infected Gastric Cancer Cells Induce Lymphangiogenesis and Lymphatic Remodeling via Transfer of miR-1246." Small: e2308688. IF=13.3
21.天津医科大学尹海芳团队:血清来源外泌体介导肿瘤新抗原个体化免疫治疗新策略Zhang, Y., et al. (2023). "Complete remission of tumors in mice with neoantigen-painted exosomes and anti-PD-1 therapy." Mol Ther. IF=12.4前期报道:https://www.exosomemed.com/15469.html
22.山东第一医科大学第一附属医院段瑞生团队:树突状细胞来源的细胞外囊泡治疗重症肌无力新策略Zhou, Y., et al. (2023). "Extracellular vesicles encapsulated with caspase-1 inhibitor ameliorate experimental autoimmune myasthenia gravis through targeting macrophages."J Control Release 364: 458-472. IF=10.8前期报道:https://www.exosomemed.com/15558.html
23.广东医科大学附属医院李鹏/林颢:葛根来源的类外泌体样纳米囊泡通过增强自噬缓解骨质疏松Zhan, W., et al. (2023). "Pueraria lobata-derived exosome-like nanovesicles alleviate osteoporosis by enhacning autophagy."J Control Release 364: 644-653. IF=10.8前期报道:https://www.exosomemed.com/15545.html
24.南京医科大学贾瑞鹏/周六化、东南大学徐华:脂肪间充质干细胞来源的小型细胞外囊泡用于膀胱组织工程Yang, T., et al. (2023). "Negatively charged bladder acellular matrix loaded with positively charged adipose-derived mesenchymal stem cell-derived small extracellular vesicles for bladder tissue engineering."J Control Release 364: 718-733. IF=10.8前期报道:https://www.exosomemed.com/15506.html
25.江南大学附属医院黄朝晖/生物工程学院吴志猛团队:工程化外泌体靶向治疗恶性肿瘤新策略Gong, L., et al. (2023). "An off-the-shelf small extracellular vesicle nanomedicine for tumor targeting therapy."J Control Release 364: 672-686.IF=10.8前期报道:https://www.exosomemed.com/15540.html篇幅有限,仅介绍其中少数文献。
如需全部文献列表及部分文章原文,请至外泌体之家论坛同名贴下载。(搜索:外泌体之家;或网址:www.exosome.com.cn)以上,11月份国内细胞外囊泡/外泌体领域研究进展的月总结整理。感谢大家关注!愿有所收获。下个月见!
外泌体资讯网 国内外泌体领域进展总结(2023年11月)