细胞外囊泡(EVs) 含有蛋白质、核酸和脂质,在肿瘤形成、转移和侵袭过程中发挥着重要作用。循环肿瘤细胞(CTCs)是从原发肿瘤脱落并进入血液系统的肿瘤细胞。研究表明,EVs和CTCs在肿瘤远处转移过程中关系密切。原发肿瘤脱落后释放到血液中形成CTCs,这些肿瘤细胞被称为“种子”,在类似“土壤”的远处靶器官中定植和生长,而肿瘤和非肿瘤来源的EVs则可在肿瘤转移过程中充当“肥料”。已有许多文章总结了EVs在肿瘤转移中的作用,但还没有综述全面讨论肿瘤从原发灶到远处部位转移过程中EVs对CTCs的作用。2023年11月30日,来自四川大学华西医院甲状腺外科的雷建勇团队,在国际期刊Molecular cancer (IF: 37.3)上发表题为“The role of extracellular vesicles in circulating tumor cell-mediated distant metastasis”的综述(doi: 10.1186/s12943-023-01909-5),总结了在肿瘤转移过程中细胞外囊泡(EVs)对循环肿瘤细胞(CTCs)的多种作用机制,包括EVs增强CTCs的脱落、在循环中保护CTCs以及决定CTCs的远处转移方向,以便更好地为肿瘤的早期诊断、治疗和预后提供信息。四川大学华西医院甲状腺外科雷建勇副教授为文章的通讯作者,硕士研究生郭思吟为文章的第一作者。
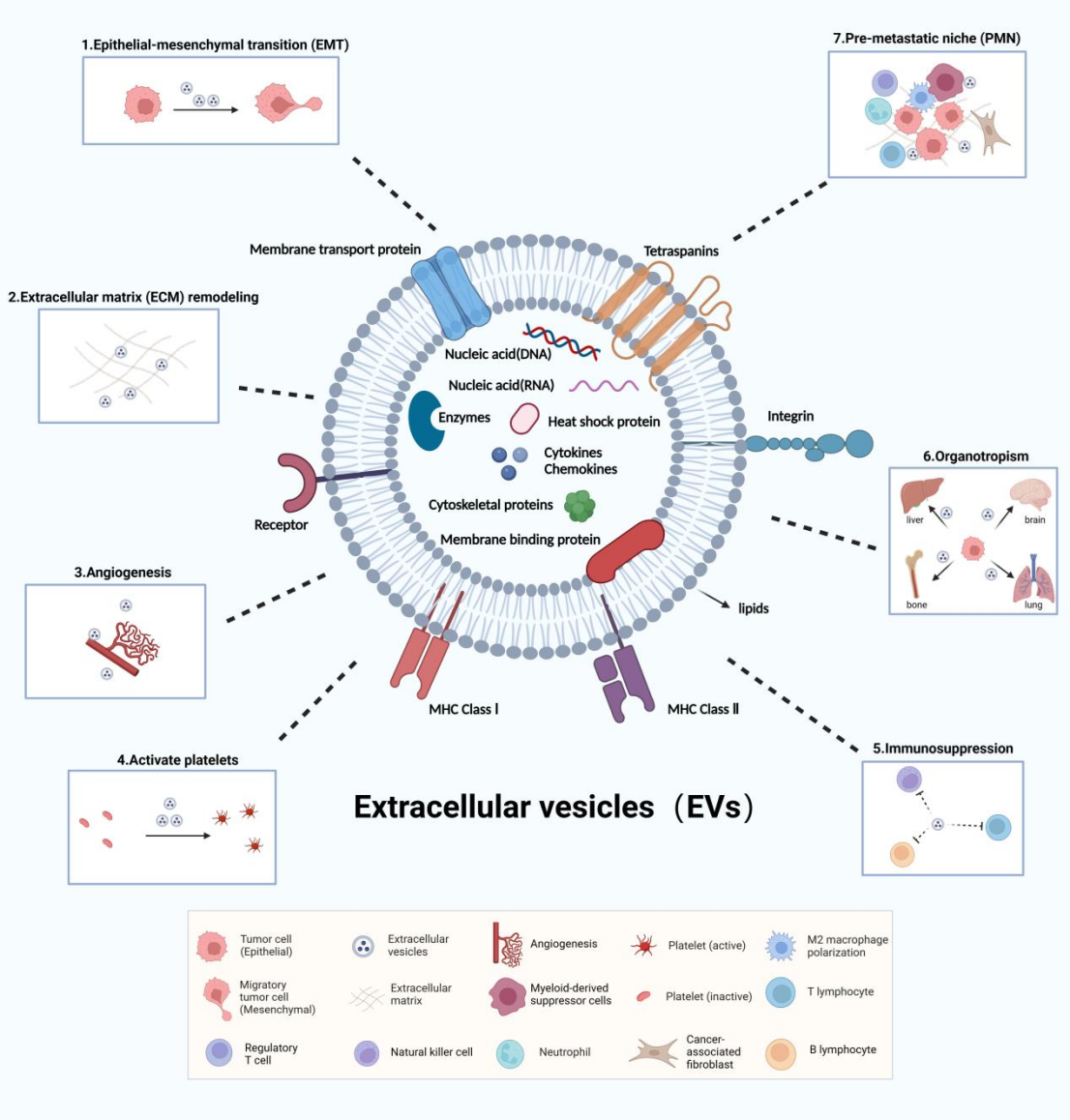
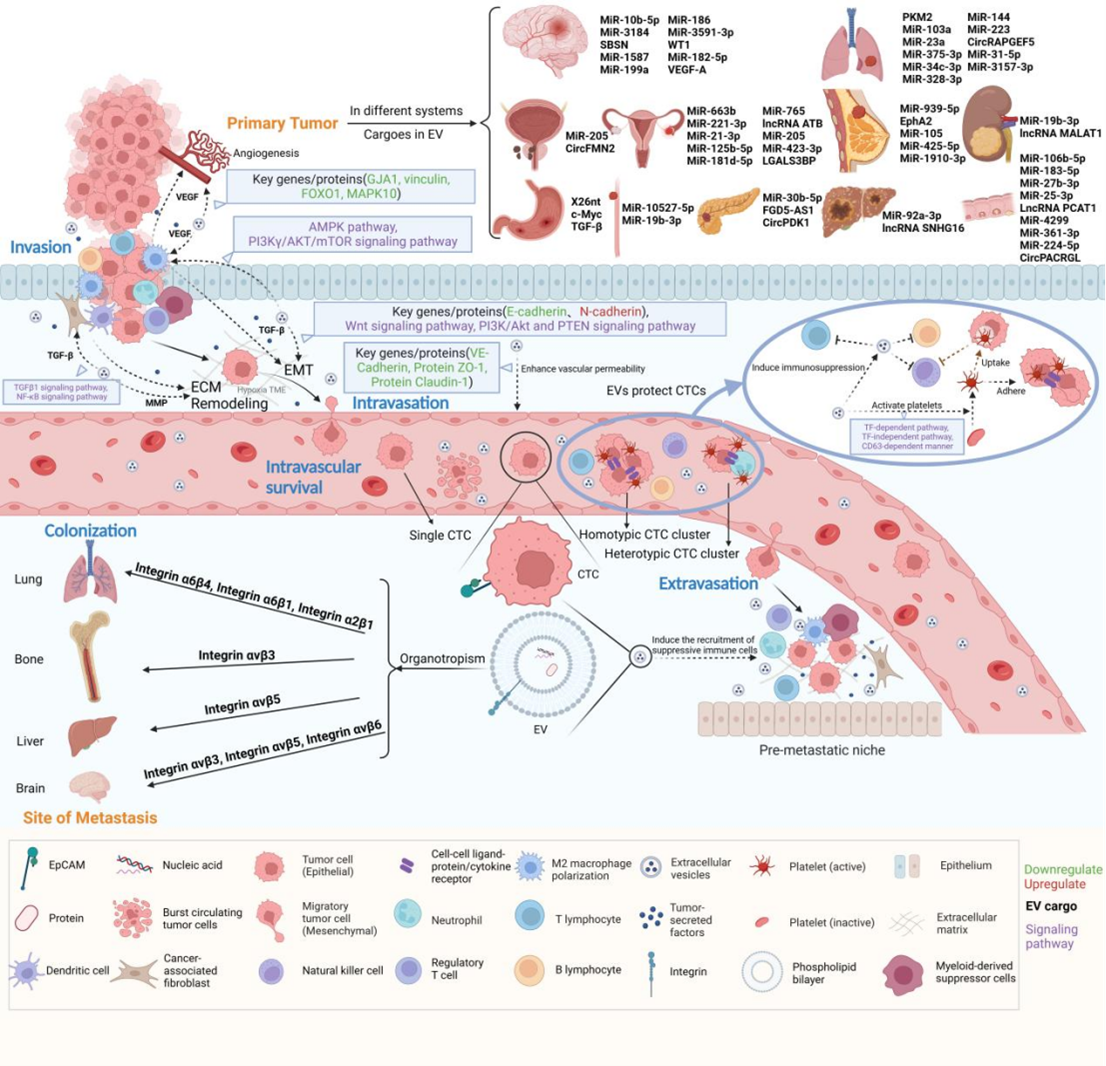
液体活检是一种新兴的肿瘤诊断技术,通过采集体液样本,主要分析循环肿瘤DNA(ctDNA)、CTCs和EVs,从而检测标本中与肿瘤相关的分子标记物,用于肿瘤的检测和监测。在液体活检的几种标记物中,CTCs和 EVs具有良好的稳定性和检测灵敏度,可反映肿瘤细胞的侵袭性、转移潜力和预后。近年来,EVs和CTCs已被普遍用作液体活检的标记物,用于肿瘤诊断、监测、预后判断、肿瘤分类和亚型鉴别。肿瘤转移对疾病进展和预后非常重要。研究表明,EVs可在肿瘤转移过程中保护CTCs。CTCs可被视为“种子”,而EVs携带的货物则可被视为“肥料”,EVs可影响CTCs在类似“土壤”的远处靶器官中定植和生长。换言之,CTCs是肿瘤细胞的一种存在形式,可通过循环到达远处器官并定植,而各种细胞来源的EVs可携带核酸和蛋白质等相关分子,影响细胞行为并促进CTCs介导的转移。文章首先介绍了EVs的结构及其在肿瘤转移中的作用(如图1),接着重点阐述了EVs在肿瘤转移过程中对CTCs的作用(如图2)。在原发灶,EVs 可通过促进上皮-间充质转化(EMT)和细胞外基质(ECM)重塑,以及促进血管生成和增加血管通透性来增强 CTCs 的脱落;在转移过程中,EVs 通过激活血小板和诱导免疫抑制保护 CTCs;最后,EVs 决定 CTCs 的转移方向,参与转移前生态位(PMN)的形成,促进CTCs的转移和定植(如图3)。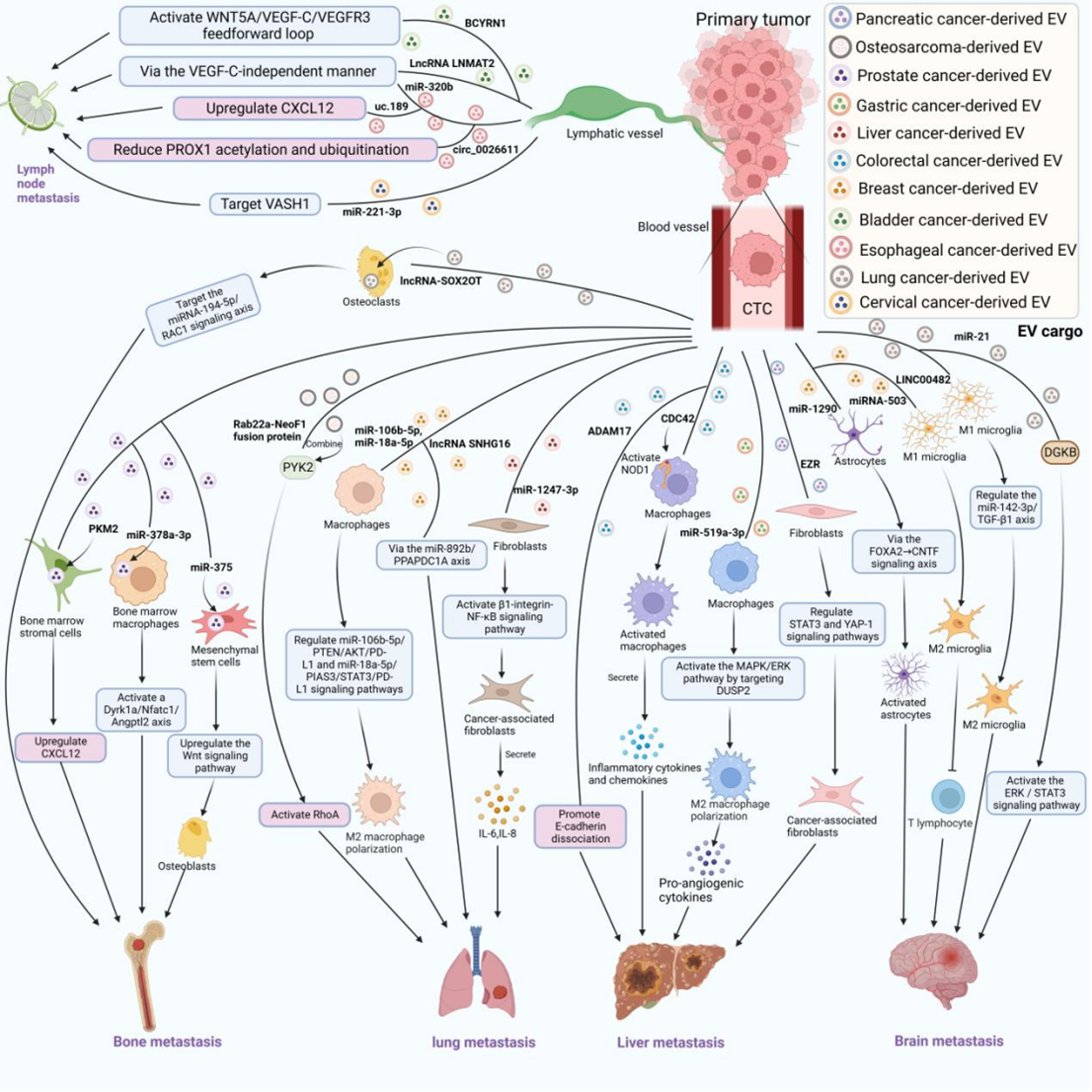
图3 EVs决定CTC在不同远处转移部位的定植
对这些机制的了解可以启发我们对肿瘤转移产生更深入的认识,并促进我们对肿瘤预防、诊断和治疗策略的思考。进一步研究EVs在CTCs介导的转移过程中的作用,还将有助于在液体活检中发现新的生物标志物,从而有利于开发更创新、更精准的肿瘤疗法,为癌症患者提供更多帮助。
The role of extracellular vesicles in circulating tumor cell-mediated distant metastasis. Mol Cancer. 2023 Nov 30;22(1):193. doi: 10.1186/s12943-023-01909-5. PMID: 38037077; PMCID: PMC10688140.外泌体资讯网 Mol Cancer | 四川大学华西医院雷建勇团队:细胞外囊泡在循环肿瘤细胞介导的远处转移中的作用