最近坛子里有几位朋友询问exosome-free FBS的制备方法,hzangs在每个帖子都做了回答。为了方便大家了解这方面的技巧,hzangs在这里做一个略微的总结并提供一份简要的protocol给大家参考。面对诸多大牛,可能我的叙述有不严谨的地方,班门弄斧还请各位多多指正。
很多朋友目前都在尝试从细胞培养上清中分离外泌体,这就存在一个问题:使用正常培液养细胞再换无血清培液收外泌体,还是直接使用exosome-free FBS配制培液用于培养细胞收外泌体?hzangs打开自己endnote里的文献集,从上自下打开数篇CNS及子刊的paper,参考了一下(PMID:24735924、25417103、25985394、26524530、26106858),所有的这些CNS及子刊的paper均是使用exosome-free FBS培养细胞再收上清分离exosomes的。由此可见,在高质量的paper里,大家更倾向于使用含有exosome-free FBS培液来培养细胞收上清分离exosomes。至少肿瘤研究方面是这样的!
既然很多高质量的paper都在使用exosome-free FBS配制的培液培养细胞收外泌体。作为追风者的我虽然没有能力发这些高质量的paper,但是单位里还是有设备让我在方法上接近高质量paper的。自我安慰一下,哈哈!![]()
废话这么多,那就开始分享一下一些paper里提到过的使用超速离心机制备exosome-free FBS的方法吧。目前常见的有两种方法,一种是先配置20%FBS的培液,然后培液超速离心去除exosomes后用于细胞培养,另一种是直接FBS长时间超速离心去除exosomes后再用于配制培液养细胞。考虑到工作量以及机器的使用频率,hzangs选择了后者,当然这也是很多paper里选择的方法。下面我就来分享一下大概的制备流程。至于分离效果,我们在最后秀数据讨论。如何使用这些exosome-free FBS 我们也在后面说。
材料及设备:FBS、超速离心机、超速离心机转子、50ml离心管、0.45um滤器、10ml或20ml注射器。
- 你需要将FBS融化成液体,这是必须的。

- 之后你需要将FBS分装到超速离心管中,上机超离120000g 14-16h。PS:一般hzangs会在这一步选择过夜超离,因为晚上使用超速离心机的人很少很少,这样既不会耽误别人的实验,也节省自己的时间。
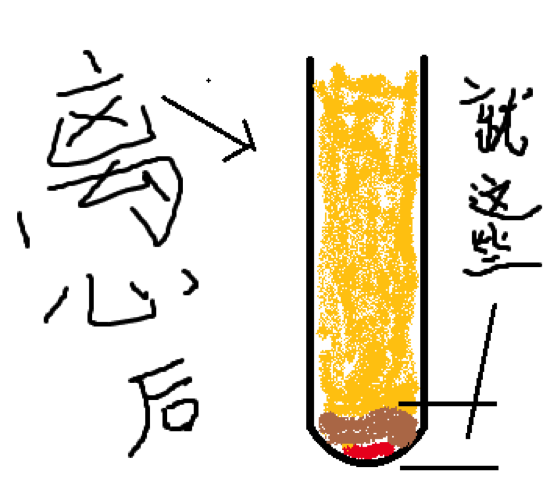
- 你需要收集离心管里约90%的上清。注意,这里不要倒,一定要使用移液器从上方吸出来。最好用十几毫升的那种pipette,方便省时还易操作。你需要贴着液面吸取FBS,以避免扰动底部的沉淀,请参见下图:
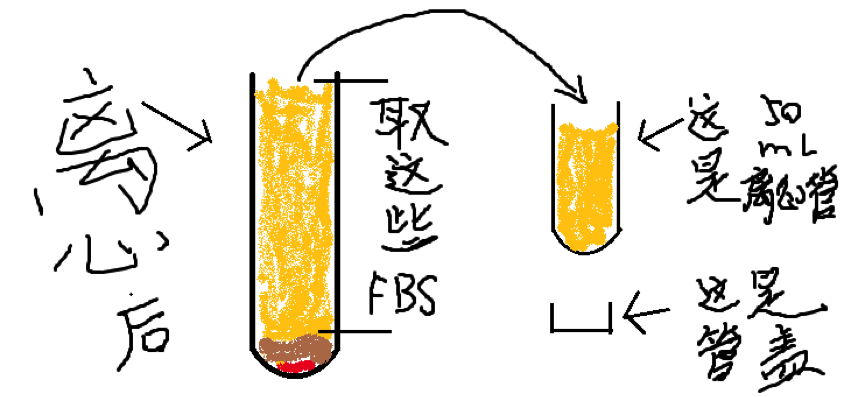
(PS:大家有没有被hzangs的绘画功底所折服,反正我自己已经被折服了,大家就凑合看吧。 哈哈哈哈哈哈)
- 转移到50ml离心管的FBS混匀后使用45um的滤器过滤即可得到无菌的exosome-free 的FBS。冻起来,随用随取。
先别急着扔。这部分血清还有其他用处。你可以收起来备用。依据hzangs的师弟实践得出真知,这部分血清可以用于冻存细胞,或者有哪些细胞状态不好,可以用这部分血清配制培液养一养,细胞会长得生龙活虎,明显比一般的FBS培养的细胞涨势迅猛!
可能还有朋友比较担心,这样制备的exosome-free FBS是否会残留大量的exosomes。我们可以参考一下beckman所提供的数据。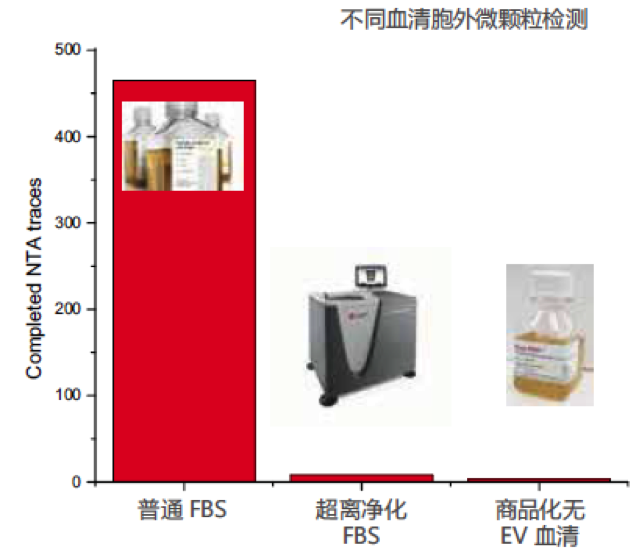
这个数据上可以看出,超离后的FBS含有的粒子数目明显低于普通FBS,与商品化的exosome-free FBS相近。
培养细胞收上清很麻烦。该如何操作比较简便呢?
hzangs分享一下自己的方法给大家作参考。以培养肿瘤细胞为例。通常会先铺50%密度的细胞到培养皿中,然后加入exosome-free FBS配制的培液,培养72小时。hzangs的细胞刚好是72h从50%长到100%,之后吸取上清用于外泌体分离,细胞消化下来继续按照50%的密度铺板,继续使用exosomes-free FBS配制的培液培养,72h后就又可以收一次了。
Hzangs的分享到此结束。有实验条件的朋友可以尝试一下。如有其它问题,大家可以到坛子里的同名贴下留言给我。谢谢大家~
版权归外泌体之家所有,欢迎转载,但请注明出处和原文链接!
原文下载和讨论请点击:http://www.exosome.com.cn/forum.php
外泌体资讯网 exosome-free FBS的制备策略及使用技巧