细胞外囊泡(EV)是介导短距离和长距离细胞间通讯的生物纳米颗粒,可传递生物活性载荷。短距离通讯发生在间质中,而长距离通讯被认为需要通过血液循环进行运输才能到达远端部位。细胞外囊泡治疗通常通过系统注射,诊断方法通常依赖于检测血液中器官来源的EV。然而,EV进入和退出循环的机制尚不清楚。近日,Nature Nanotechnology杂志(IF=38.3)上发表一篇综述,讨论了淋巴系统和通过细胞内和细胞间途径穿越内皮屏障的运输作为EV进入和退出血液循环系统的潜在途径。
细胞外囊泡(EV)是介导短距离和长距离细胞间通讯的细胞释放的纳米颗粒。许多研究已经报道了血液中器官特异性EV的存在,然而,这些EV离开间质的机制仍然大多未知。同样,已经证明系统性给予的EV可以到达特定的器官,但是穿过内皮屏障的证据仍然不清楚。EV领域的指数级增长和新兴治疗和诊断EV基础产品的加速发展,突显了了解EV在体内的运输的迫切需要。因此,可以认为EV运输现象是所需功能的最关键组成部分,因为错误的空间环境是徒劳的,可能是有害的。该综述探讨了EV进入和退出血液循环的潜在纳米级过程。大多数器官的毛细血管具有非窗孔连续内皮衬里,只能通过水、小分子溶质和气体。相比之下,如肝脏和脾脏等器官具有不连续的内皮衬里,允许大分子和纳米级颗粒在间质空间和血液循环之间穿越。同样,同一器官中存在各种亚型的内皮也很常见。例如,肾脏包含几种具有不同结构和作用的内皮细胞类型。中等和大型血管中发现的肾脏内皮细胞形成非窗孔连续层,通过细胞间连接相互连接,并朝着血流方向延伸。相比之下,肾小球的内皮细胞具有众多的窗孔和厚的糖基化层,这有助于肾小球的滤过屏障的过滤特性。近曲小管毛细血管的内皮细胞具有窗孔,并被由糖蛋白制成的薄膜覆盖,这有助于邻近小管上皮细胞的液体和物质的重吸收和分泌。器官内和器官间的内皮细胞异质性可能对EV穿越内皮屏障的机制产生重大影响,该综述讨论了可能的路线。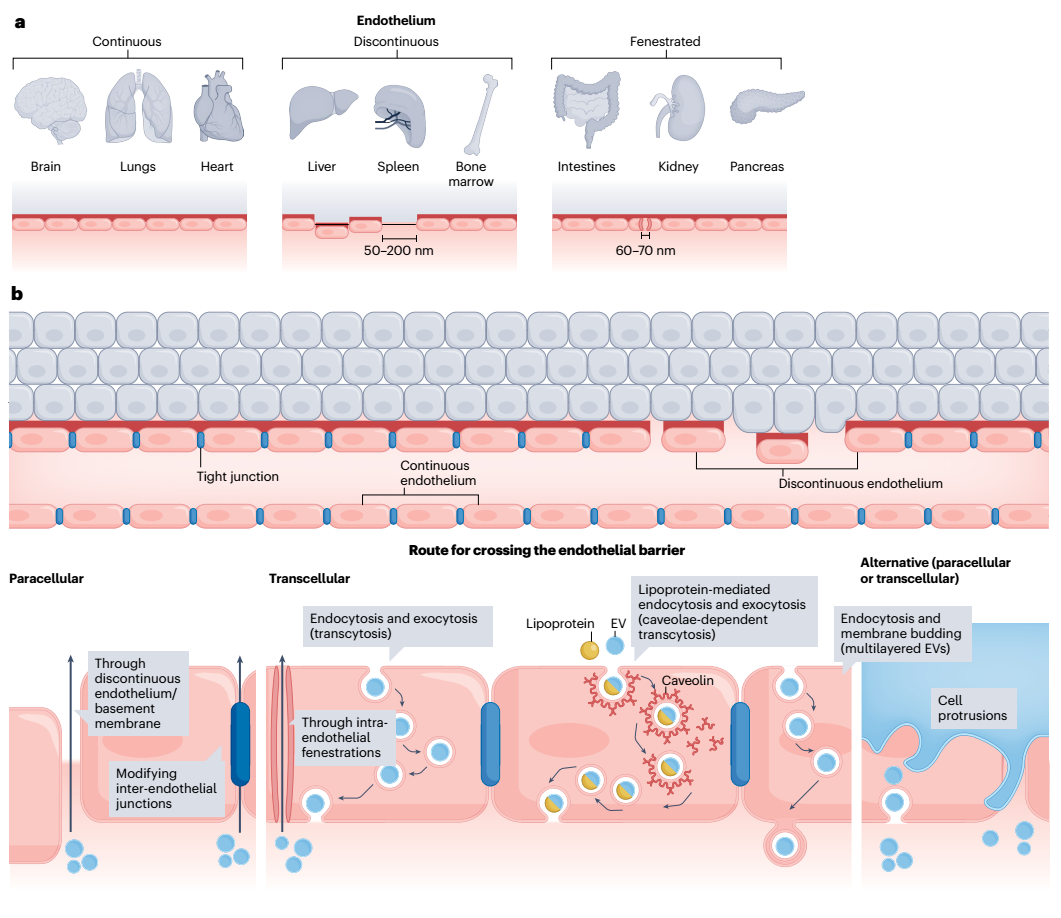
图1、EV进入和退出血液循环的潜在途径。a,内皮的一般类型。值得注意的是,某些器官(如肾脏)中可能存在多种内皮。b,细胞外囊泡可以通过细胞内或细胞间运输途径穿过内皮屏障。在细胞间运输的情况下,EV可以通过内皮细胞之间的间隙通过,这可能是器官中突出的运输途径,如肝脏。细胞外囊泡也可以修改内皮细胞之间的连接以实现细胞间运输。在细胞内运输的情况下,EV可以通过内皮细胞内的窗孔通过或使用各种跨膜途径。结合脂蛋白以劫持空泡介导的跨膜途径也可能被利用。细胞外分泌独立的跨膜运输机制也是可能的,从而通过膜芽生长释放多层EV。最后,细胞突起可能被利用作为细胞外囊泡跨越内皮屏障的替代途径。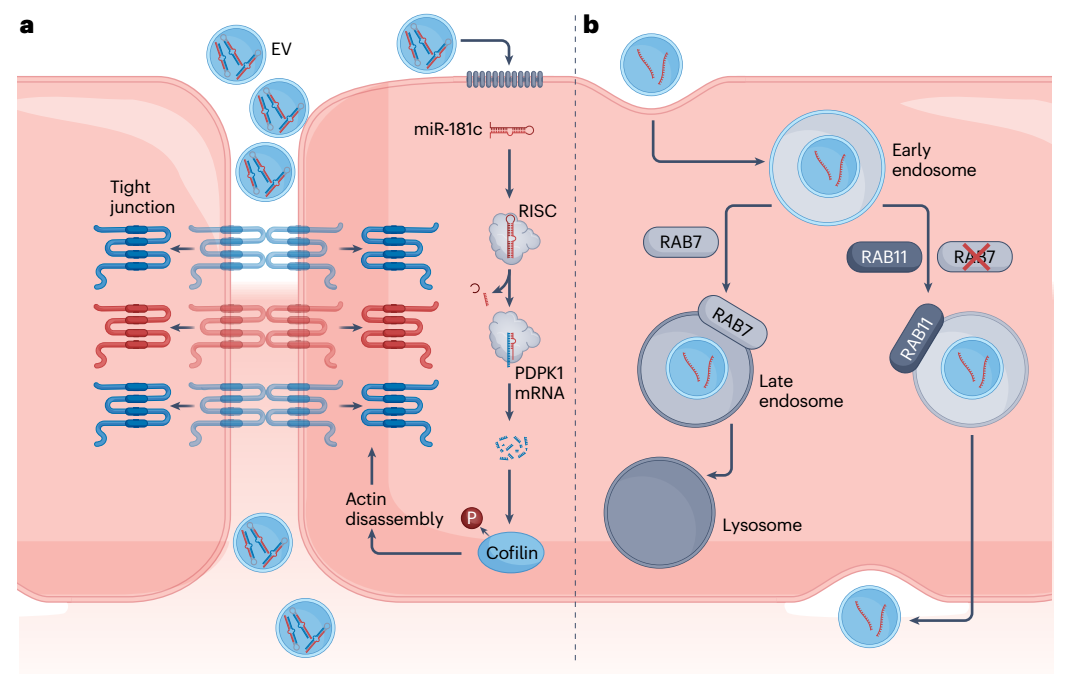
图2、癌细胞来源的EV穿越血脑屏障内皮的机制。a,癌症EV相关的miR-181c通过下调参与cofilin磷酸化的蛋白质PDPK1的表达来调节紧密连接的完整性。由于这个过程导致的cofilin去磷酸化增加最终肌动蛋白丝的解聚,将附着的紧密连接蛋白从它们的跨膜位置转移到细胞质中,导致血管通透性增加,使EV的细胞间运动增加。b,已发现乳腺癌来源的EV在内吞作用后抑制RAB7相关的降解途径,将自己重定向到RAB11相关的回收途径。这使得EV可以通过内皮细胞的基底侧膜进入间质的跨膜运输。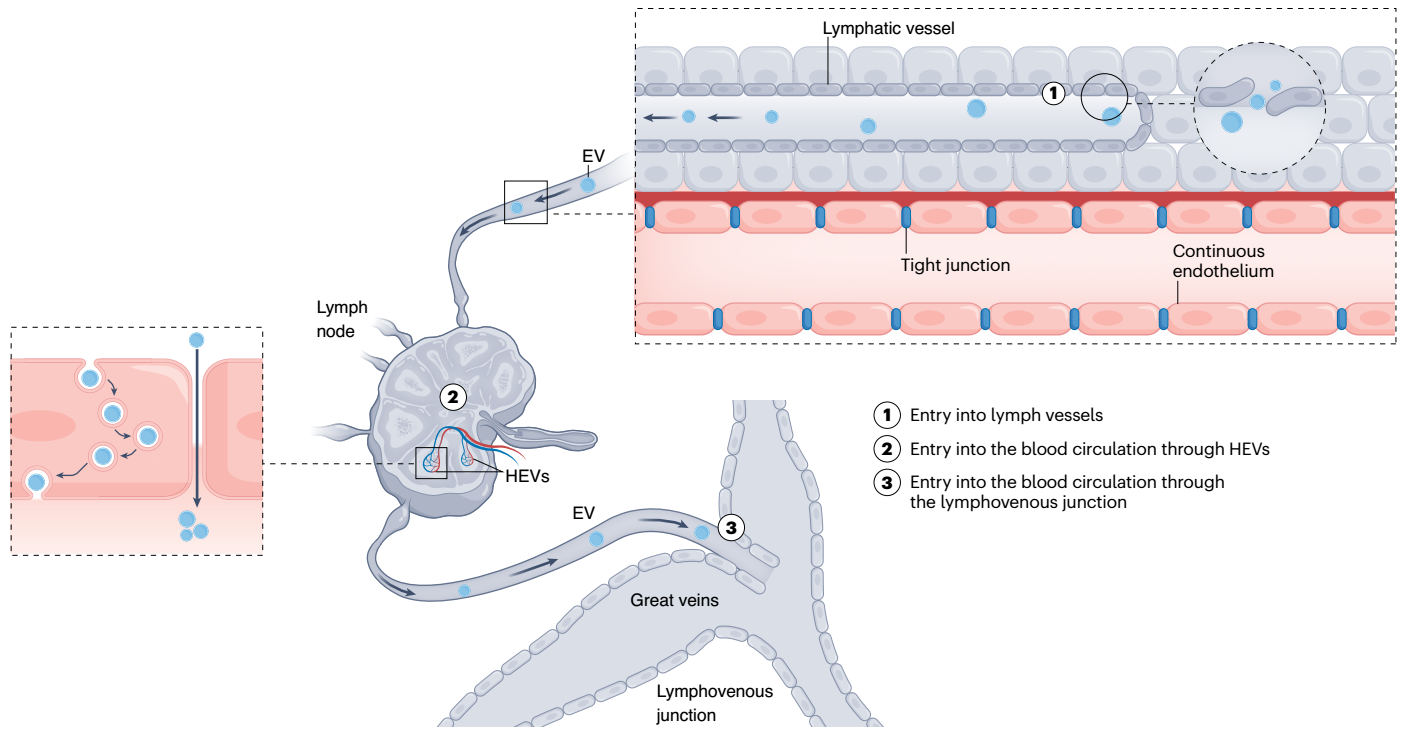
图3、EV通过淋巴系统进入血液循环的潜在途径。细胞外囊泡可以通过淋巴内皮中的液压敏感连接(瓣膜)从间质中退出,形成微米级间隙,随后通过淋巴结中的高内皮静脉(HEV)或通过流入大静脉的淋巴静脉交界处进入血液循环。综合来看,EVs在间质、淋巴系统和血液循环之间交流的可能机制有很多。虽然已经描述了细胞间隙和细胞内转运的个别示例,但在生理和病理情况下,对EV进出血液循环的全面理解仍然缺乏。该综述强调了研究EV跨越血管屏障的运输的迫切需要,这对于理解超越局部间质的细胞间通信以及利用EV生物学进行诊断和治疗用途至关重要。在治疗方面,了解EV运输可以帮助选择最有效的给定应用程序的管理路线。皮下、腹膜和肌肉注射途径可能会增强淋巴运输,就像合成纳米颗粒所证明的那样。然而,对于淋巴引流后EV命运的了解不足,限制了利用给药方式来改善运输和治疗效果的开发。此外,EV物理特性(如大小)对其与血管屏障的相互作用的影响仍然大多未知,阻碍了理性设计理想治疗方案。在动物模型中,小型EV(约<100nm)和大型EV(约>200nm)在给药时表现出不同的分布和积累特征。例如,一项生物分布研究的系统评价表明,在给药后的第一小时内,小型EV的沉积升高在肝脏和肾脏中观察到,并在2-12小时内在肺和脾脏中观察到,而大型EV则在肺(第一小时)和肝脏(2-12小时)中积累增加。然而,介导不同生物分布特征的EV运输现象和血管相互作用仍然不清楚。了解EV运输对于诊断应用也很重要。例如,根据淋巴运输的重要性,可以通过从淋巴结中采样EV并筛查与疾病相关的蛋白质、核酸和脂质来提高诊断能力。总之,淋巴因其很可能是EV交流的主要路线,因此在诊断和治疗目的上提供了一个有前途的途径。Iannotta D, A A, Kijas AW, Rowan AE, Wolfram J. Entry and exit of extracellular vesicles to and from the blood circulation. Nat Nanotechnol. 2023 Dec 18. doi: 10.1038/s41565-023-01522-z. PMID: 38110531.外泌体资讯网 Nat Nanotechnol:细胞外囊泡进出血液循环的方式