近日,皖南医学院非编码RNA基础与临床转化安徽省重点实验室吕坤教授团队揭示了M2巨噬细胞外泌体在病毒性心肌炎中的保护作用及其机制,相关研究成果于2023年12月28日发表在著名学术期刊Redox Biology (中科院一区,Top期刊, IF: 11.4)。论文题目为: “M2 macrophage exosome-derived lncRNA AK083884 protects mice from CVB3-induced viral myocarditis through regulating PKM2/HIF-1α axis mediated metabolic reprogramming of macrophages”,论文链接:https://doi.org/10.1016/j.redox.2023.103016。
病毒性心肌炎是由病毒感染引起的一种非缺血性炎症性疾病,占心肌炎的绝大多数,已成为影响人类健康的一类重要的心血管感染性疾病。大量研究证实,巨噬细胞极化与病毒性心肌炎密切相关。该团队之前的研究表明,M1巨噬细胞能显著加重心肌炎,而M2巨噬细胞则能有效缓解心肌炎症。然而,M2巨噬细胞减轻心肌炎症的具体分子机制在很大程度上仍不清楚。
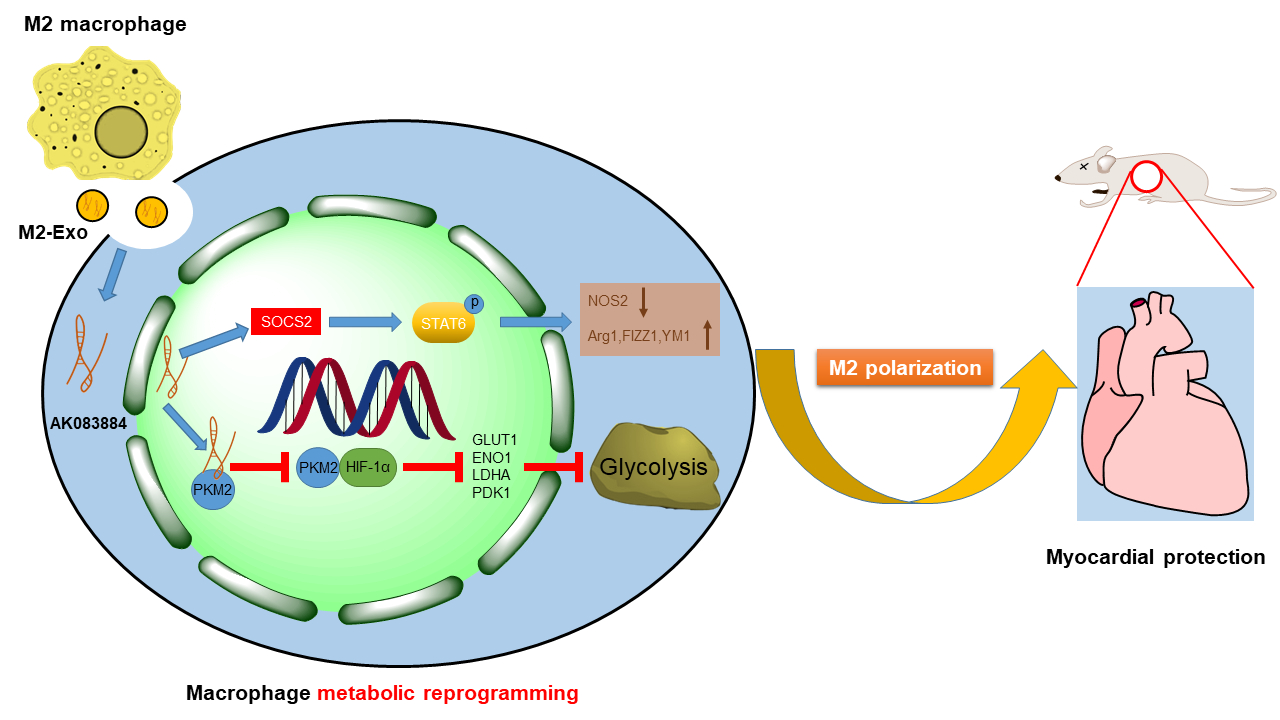
在这项工作中,研究者证实,M2巨噬细胞通过分泌包含长链非编码RNA (lncRNA) AK083884的外泌体促进病毒性心肌炎小鼠心脏浸润巨噬细胞M2极化,从而减轻心肌炎小鼠心肌炎症程度,发挥保护作用。机制上,一方面,AK083884通过调控其临近基因SOCS2表达,激活下游STAT6的磷酸化,促进巨噬细胞M2相关基因的表达;另一方面,AK083884通过竞争结合PKM2,阻断PKM2与HIF-1α的相互作用,进而抑制巨噬细胞的糖酵解作用,促进M2巨噬细胞的重编程(图1)。该研究揭示了M2巨噬细胞外泌体中的AK083884通过影响代谢重编程调节巨噬细胞极化的重要作用,证实了外泌体中lncRNA作为信号转导物的潜力,鉴定了心肌炎进程中的新的调控靶点,为心肌炎的靶向治疗提供了一个潜在的治疗途径。
图1 M2巨噬细胞外泌体来源的lncRNA AK083884通过调节PKM2/HIF-1α轴介导的巨噬细胞代谢重编程,缓解心肌炎症
皖南医学院非编码RNA基础与临床转化安徽省重点实验室张莺莺教授、2020级硕士生朱良宇、李雪琴副教授为该论文的共同第一作者,实验室主任吕坤教授、副主任朱小龙副研究员为该论文的共同通讯作者。该研究工作得到了国家自然科学基金(82170368, 82072370, 82100019)、安徽省自然科学基金杰青项目(2108085J44)、中国高校产学研创新基金(2023HT008)等课题的资助。
参考文献:
M2 macrophage exosome-derived lncRNA AK083884 protects mice from CVB3-induced viral myocarditis through regulating PKM2/HIF-1α axis mediated metabolic reprogramming of macrophages, Redox Biol. 2023 Dec 28:69:103016. doi: 10.1016/j.redox.2023.103016.