近年来,癌症的诊断和治疗取得了显著进展,但癌症的早期诊断仍然是一个挑战。根据GLOBOCAN 2020年的研究,2020年全球约有1930万新癌症病例和近1000万人死于癌症。细胞外囊泡(EVs)是处于生理和病理状态细胞分泌的产物。由于其稳定的双层结构和携带不同来源的信息,肿瘤相关细胞外囊泡可以传递大量的肿瘤细胞信息,已被认为是一种新型的癌症精准诊断的生物标志物。建立低成本、快速及灵敏的肿瘤来源细胞外囊泡检测方法对于癌症的早期筛查和临床诊断具有重要意义。近日,桂林理工大学李建平/桂林医学院秦韬团队在国际著名学术期刊Analytical chemistry发表题为“An electrochemiluminescent sensor based on glycosyl imprinting and aptamer for the detection of cancer-related extracellular vesicles”的研究成果(2024, 13;96(6):2550-2558)。结合糖基印迹技术与CD63适配体双识别,研究者构建了一种低成本、快速及灵敏检测肿瘤相关细胞外囊泡的传感器。论文第一作者为桂林理工大学博士生蒋泽军。文章通讯作者秦韬副教授主要从事恶性肿瘤发生发展及相关出凝血机制方面的研究工作,李建平教授主要从事电化学分析、化学与生物传感器方面的研究工作。
该工作利用糖基印迹聚合物(GIP)对糖蛋白表面糖基识别和适体对糖蛋白识别的双重识别作用,构建了检测肿瘤患者血浆中EVs的电化学发光(ECL)传感器。以EVs表面特征的三糖糖基Neu5Ac-α-(2, 6)-Gal-β-(1-4)-GlcNAc为模板分子,3-氨基苯基硼酸为功能单体,通过电聚合法形成糖基印迹膜。糖基被洗脱后,印迹膜特异性识别和吸附样品中的EVs,然后加入CD63适配子-Ru(bpy)32+与EVs表面的CD63糖蛋白结合,从而实现对EVs的二次识别。最后,根据标记的Ru(bpy)32+的ECL信号对EVs进行定量检测。印迹膜捕获的EVs越多,孵育后得到的探针越多,ECL信号越强。在优化的条件下,ECL信号与EVs浓度在9.5×102-9.5×107个/mL范围内呈良好的线性关系,检出限低至641个/mL。GIP传感器可以高精度区分癌症患者和健康对照组的EVs含量,而且制备成本低、灵敏度高、使用方便,有望用于癌症的早期检测和诊断。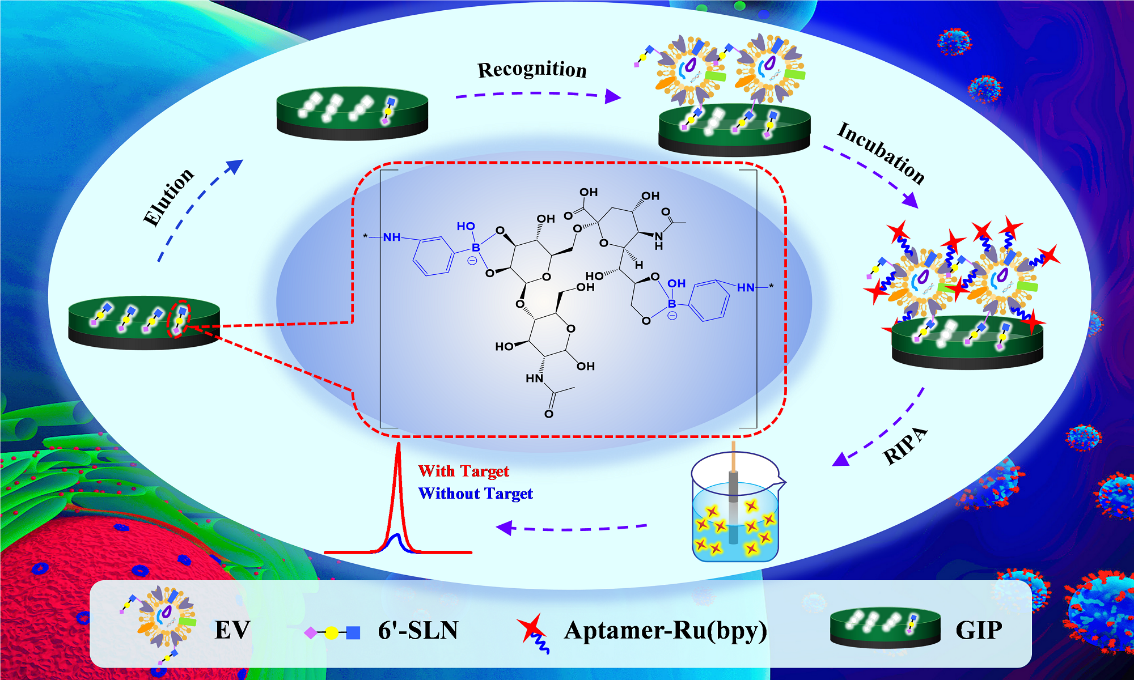
图1 基于GIP膜和适配体双重识别外泌体的电化学发光检测使用整体印迹方法已经开发出来一些检测EVs的分析方法,这类方法直接使用EVs作为模板。然而,外泌体作为粒径为30-150 nm的囊泡,没有刚性结构,容易变形,在制备过程中很难在分子印迹聚合物中形成规则的空穴,从而影响外泌体在样品中的选择性再吸附。此外,由于其体积大、易碎性,也很难进行洗脱、再吸附等操作。糖基印迹是近年来发展起来的一种新型蛋白质印迹技术。蛋白质的糖基化是肿瘤细胞的重要特征。利用EVs表面标志蛋白CD63的特征糖基作为模板分子制备糖基印迹膜重吸附EVs,不仅解决了整体印迹难以印迹和洗脱的问题,而且克服了高传质阻力的困难,捕获了携带特异性糖基片段的EVs,建立了肿瘤来源EVs的定量分析方法。综上所述,该研究利用糖基化印迹技术构建了一种高效检测肿瘤相关EVs的电化学发光传感器。该传感器可以区分癌症患者和健康人的血浆,可以作为临床诊断的初步筛查平台。An Electrochemiluminescent Sensor Based on Glycosyl Imprinting and Aptamer for the Detection of Cancer-Related Extracellular Vesicles, Anal Chem. 2024 Feb 13;96(6):2550-2558. doi: 10.1021/acs.analchem.3c04991.外泌体资讯网 Anal. Chem.|桂林理工大学李建平/桂林医学院秦韬:糖基印迹和适配体双识别的电化学发光传感检测细胞外囊泡






