合成纳米颗粒如脂质纳米颗粒(LNPs)被广泛用作药物传递载体。然而,它们存在一些缺点,包括低生物相容性和不利的免疫反应。天然存在的细胞外囊泡(EVs)具有作为自身的、安全的和多功能纳米囊泡载体的潜力。然而,将大型生物分子装载到EVs中仍然是一个挑战。来自丹麦奥胡斯大学的研究人员提出了一种控制装载方法,使用DNA介导和可编程融合的EVs与载有信使RNA(mRNA)的脂质体之间进行融合。这种融合的EV-脂质体颗粒(EVLs)具备较大的生产规模,改善了mRNA递送效率和表达效率,成为细胞外囊泡介导的RNA治疗递送的重要工具。相关内容以“Programmable RNA Loading of Extracellular Vesicles with Toehold-Release Purification”为题在线发表于4月26日的国际知名化学学术期刊Journal of the American Chemical Society杂志上。
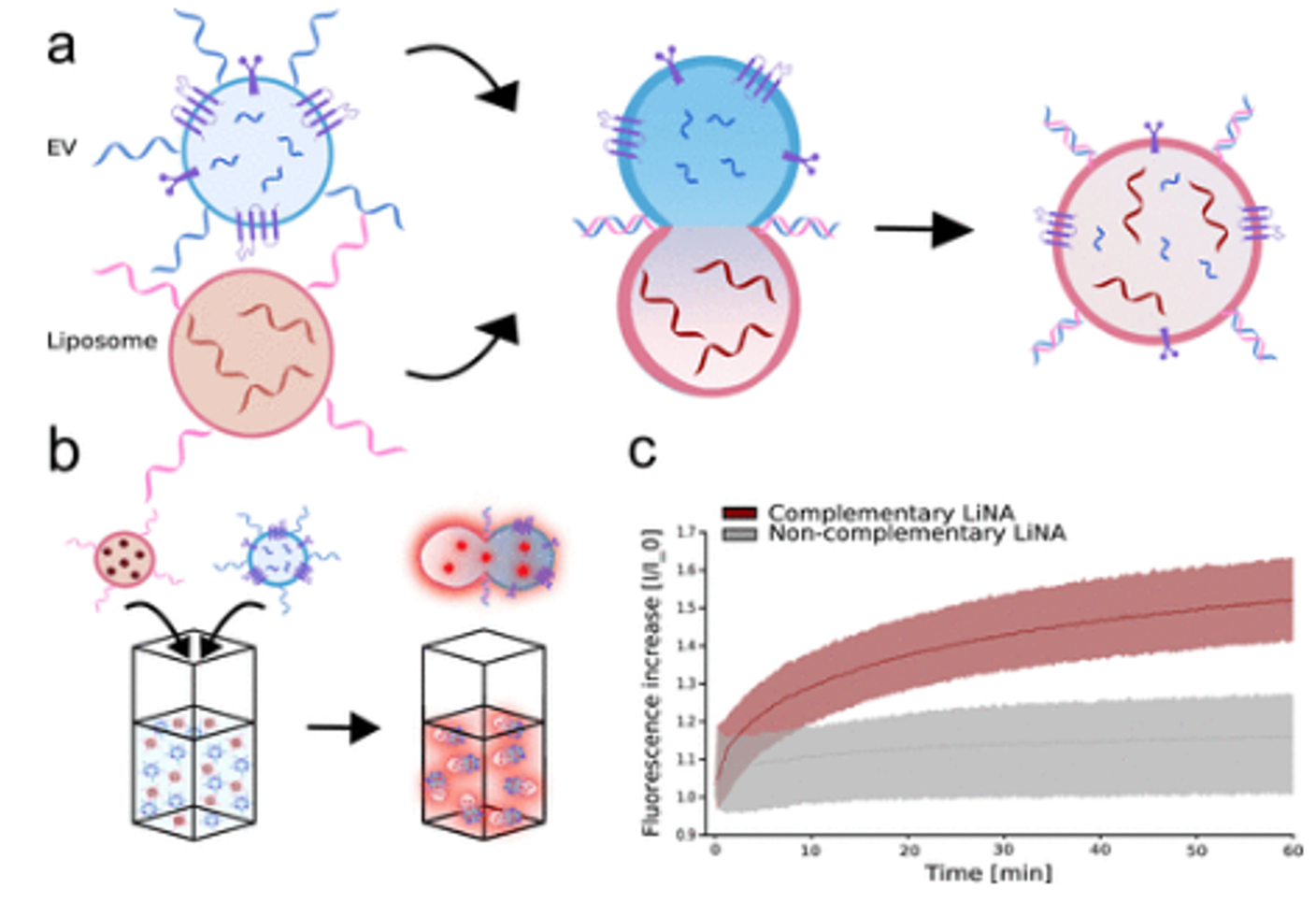
脂质纳米颗粒(LNPs)在制药行业表现出巨大成功,作为能够运输各种治疗剂的传递载体。LNP包括脂质体和脂质复合物,过去30年来已被广泛应用于美国和欧洲的23种以上批准产品的传递平台中。近年来,核酸治疗已经展示了在预防和治疗众多疾病方面的突破性成果。值得注意的是,已经批准了六种siRNA基因治疗药物,并且还有更多正在研发中。信使RNA(mRNA)治疗也在广泛应用的一系列应用中显示出潜力,包括癌症免疫治疗、蛋白质替代治疗、基因编辑和来自新冠(COVID-19)疫苗的病毒疫苗。mRNA是一种易于快速降解的负电荷大分子,这就是为什么封装是至关重要的原因。为此,LNP-mRNA配方已经取得了巨大成功,特别是在疫苗平台中。LNP配方通常由30-50%的可电离脂质、磷脂、胆固醇和聚乙二醇(PEG)锚定脂质组成,通过RNA的负电荷与脂质的正电荷之间的自组装而自发形成。pH依赖性可电离脂质在LNP-mRNA配方的发展中发挥了关键作用,与永久带电的阳离子脂质相比,它具有改善了的功效和毒性特性。然而,尽管安全性得到了提高,但这些脂质仍然与高毒性相关联;因此,不良临床效应和长期免疫原性都会被考虑。此外,由脂质锚定的PEG通常用于避免聚集并确保循环时间延长,但与一系列潜在副作用相关,包括免疫原性、过敏反应、药代动力学行为的意外改变、从循环中摄取以及由肝脏库普弗细胞清除导致载荷的生物降解性低。细胞外囊泡(EVs)是天然存在的纳米颗粒,起源于内体系统,并且可从几乎所有细胞类型中分泌出来。EV含有大量各种各样的小RNA、DNA、脂质和蛋白质,已知可用于介导细胞间的通讯,无论是局部通讯还是远距离器官间的信号传递。因此,EVs被发现具有固有的靶向能力、克服天然屏障的能力,并且具有治疗效果。因此,EVs在临床上既有自身的价值,也作为药物传递实体,并且已经被证明在RNA传递方面比合成LNP基础系统更有效。然而,EVs的货物装载仍然具有挑战性。EVs可以通过工程化母细胞进行装载,但EV装载的基础细胞内机制了解不足,通常表现出低效率。EVs也可以被外源性修改或装载,这被广泛用于装载小分子和较短的核酸片段。目前已报道了多种策略,包括电穿孔或简单共培养。这些策略可能导致聚集和免疫反应,与未封装的游离货物的高浓度相关。目前,安全有效地将更大分子,如mRNA,装载到EVs中仍然是一项巨大挑战。在这项研究里,研究人员提出了一种新颖、高效、可编程且温和的细胞外囊泡装载策略,利用DNA连接的EVs与载有mRNA的脂质体之间的融合。该方法利用脂质体作为mRNA封装的初始载体。为了实现融合,研究人员在脂质体表面外部功能化脂质化DNA(LiNAs),并将与LiNA互补的序列在EVs上功能化。此外,EVs还与额外的与生物素-DNA手柄互补的LiNA序列功能化,用于表面固定化。这几乎完全使脂质体与表面锚定的EVs 1:1融合,然后通过简单且非破坏性的去除非融合的脂质体。融合的仿生脂质体-EV(EVL)产品随后可以通过使用可编程链置换反应以纯形式释放并收集。研究人员进一步证明了这种策略可以通过使用磁珠作为固体支持来扩大规模,将EVLs的生产规模扩大一百万倍。将EVL颗粒传递到细胞中会显著增加mRNA传递和表达水平,证明了EV介导的传递与合成系统(如脂质体或LNPs)相比的优越性。例如,与HEK293-H细胞中的脂质体或LNPs相比,使用EVLs进行mCherry mRNA的封装、转染并改善了其翻译效率。因此,本研究所提出的仿生EVL平台可能为更具生物相容性、安全性和高效性的治疗RNA传递提供了一种新策略。参考文献:Programmable RNA Loading of Extracellular Vesicles with Toehold-Release Purification. J Am Chem Soc. 2024 May 8;146(18):12410-12422.




