中国生物研究院安文林实验室团队于2024年7月11日在Pharmaceutics期刊上发表了题为“Large-Scale Isolation of Milk Exosomes for Skincare”的研究论文。该研究通过采用切向流过滤技术,成功实现了牛奶外泌体大规模制备,获得了高纯度的牛奶外泌体。研究结果表明,牛奶外泌体不仅安全无毒性,还能被皮肤角质细胞有效吸收,并在在动物实验中展现出有良好的的透皮效果。更为重要的是,牛奶外泌体在保护皮肤屏障、抗炎、美白、抗氧化方面表现出显著的效果。这些发现不仅为牛奶外泌体在化妆品和皮肤护理领域的应用提供了坚实的科学依据,也预示着其在这些领域具有巨大的开发潜力和应用前景。该文章的第一作者是安文林实验室团队的武雪和申久恒,通讯作者是中国生物研究院的汪旭东博士和安文林主任。
研究背景
1983年,Johnstone在体外培养绵羊网织红细胞时发现一种被称为外泌体的生物膜囊泡,形状呈球形或圆盘形。外泌体是胞内多泡体与细胞膜融合后,释放到细胞外的膜性小囊泡,大小在30到200nm之间,主要为磷脂双分子层结构,携带来源细胞特异性的蛋白质、脂质和核酸,是细胞间信号传输和物质递送的载体。
外泌体存在于血液、血清和血浆、尿液、脑脊液、眼泪、牛奶等多种体液中。在这些来源中,牛奶因外泌体产量大、含量高且容易获得被极大地关注。牛奶由大约87%的水、4-5%的乳糖、3%的蛋白质、3-4%的脂肪、0.8%的矿物质和0.1%的维生素等成份组成。外泌体在牛奶的总质量中的比例微乎其微,但因其富含功能性核酸、蛋白、糖类等,在免疫防御、生长和生理调节、牛的疾病诊断等方面发挥着重要作用。
传统上,大量生产外泌体依赖于细胞培养,成本高昂。然而,牛奶中的外泌体丰富且易于分离,为我们提供了一种低成本的外泌体来源。牛奶外泌体可以通过内吞作用进入细胞质,释放其所携带的多种内容物。牛奶外泌体不仅能促进皮肤角质层的合成和重建,增强皮肤屏障功能,还具有显著的抗炎、抗氧化活性,抑制黑色素生成的作用。从细胞间通信介质到有效的护肤成分,牛奶外泌体的潜力正逐渐被挖掘,为皮肤健康带来革命性的改变。
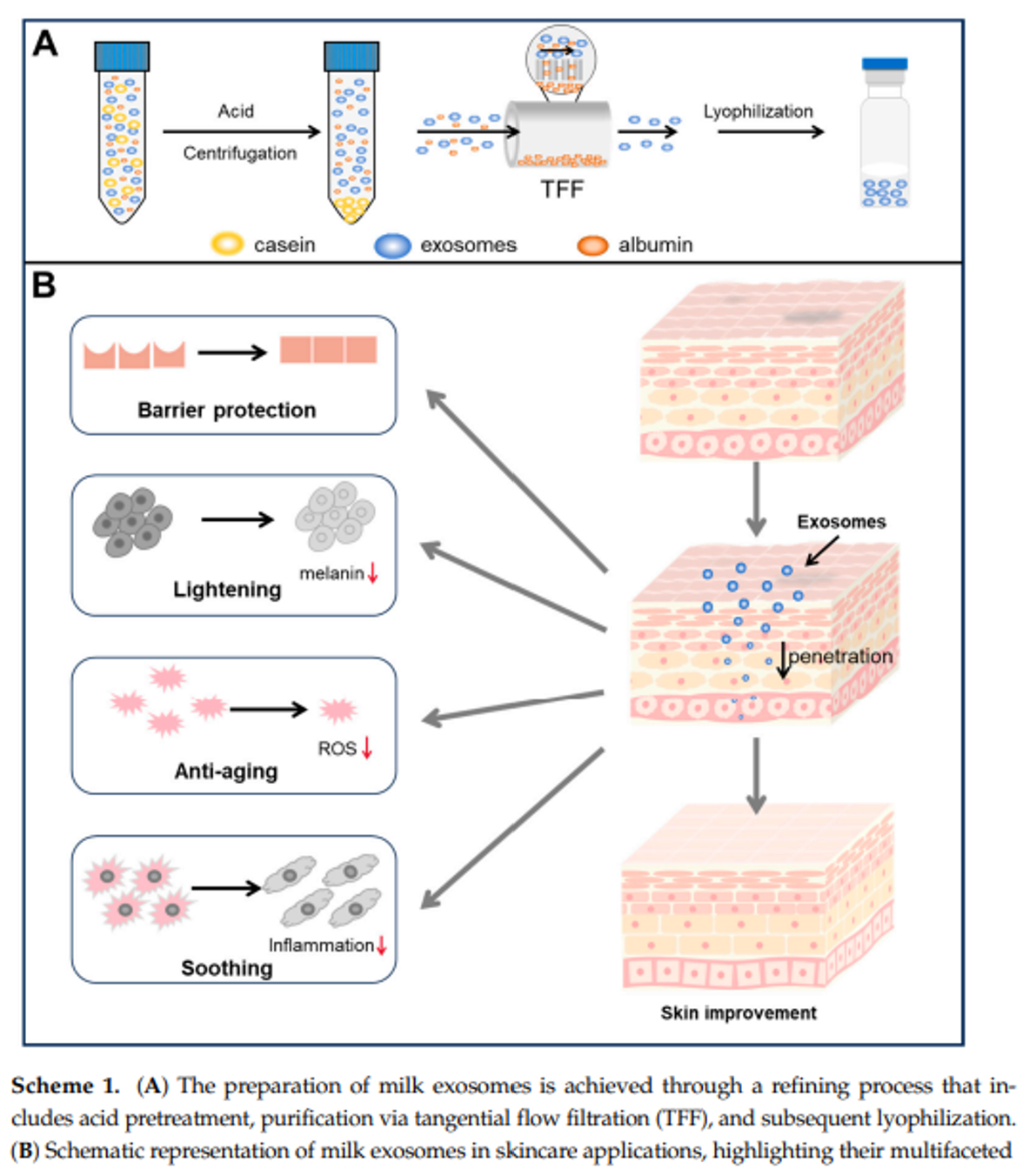
研究进程:
牛奶外泌体的大规模分离与鉴定
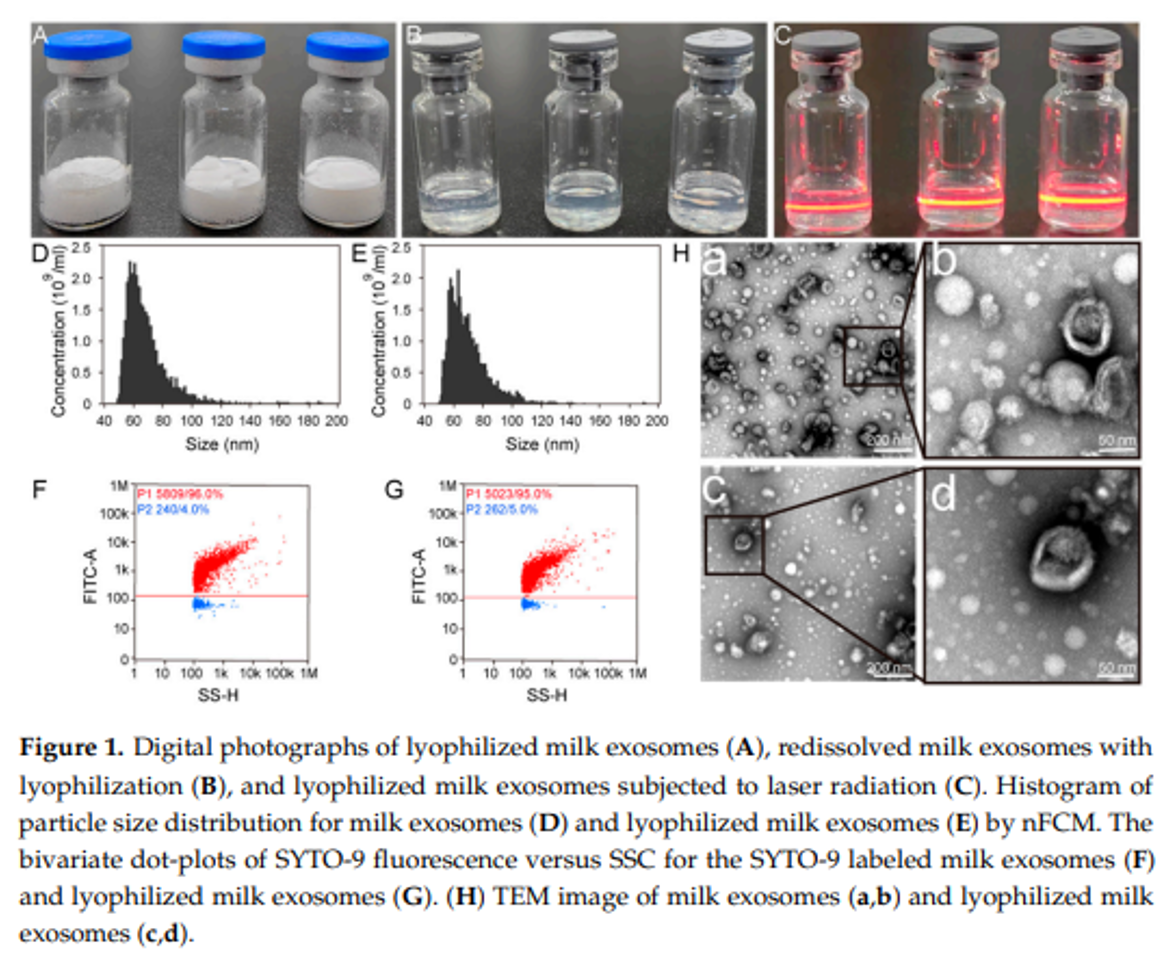
在牛奶外泌体的分离过程中,酪蛋白的去除显得尤为关键。利用冰醋酸进行等电沉淀聚合,成功地清除了酪蛋白的干扰,为后续的外泌体提纯铺平了道路。随后,通过切向流过滤技术,作者得以规模化制备高质量的牛奶外泌体。冻干后的牛奶外泌体呈现出白色蛋糕状,具有高比表面积,这一特性极大地促进了其溶解性。其残余水分含量仅为1.7%,远低于3%的标准,确保了外泌体的稳定性。将冻干的牛奶外泌体重新溶解于水性介质中,它们展现出了典型的丁达尔效应,这一现象不仅证明了牛奶外泌体的高分散性,也彰显了它们出色的水溶性。进一步的纳米流技术评估显示新鲜牛奶外泌体的测量直径约为69.03±13.66nm,而冻干样品的平均直径也仅有细微的变化,为68.07±13.44nm。通过SYTO-9荧光染料的染色检测外泌体的纯度高达96.0%,这证明了该分离方法在大规模生产高纯度牛奶外泌体方面的适用性。此外,从电镜图可以看出冻干处理并未改变外泌体的本质特性。
牛奶外泌体的染色标记及细胞摄取
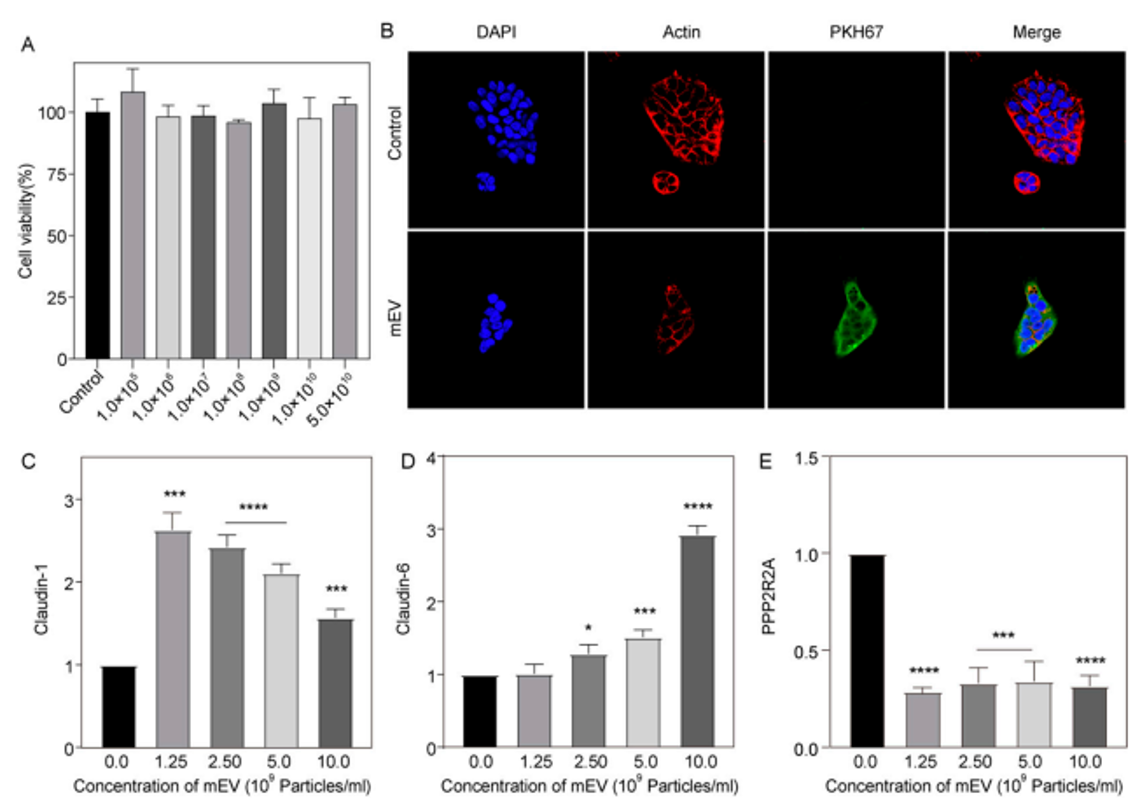
皮肤是我们身体对抗外界侵害的首道防线,它不仅阻挡病原体和异物,还抵御紫外线的侵袭,同时守护着体内水分和电解质的平衡。皮肤的结构复杂而精妙,由单层和多层上皮组织构成,其中紧密连接(TJs)是其关键的组成部分,它们如同细胞间的强力胶,紧密粘合,防止物质的非正常渗透。牛奶外泌体,这些微小的生物纳米颗粒,展现出了对维持皮肤屏障功能的卓越潜力。在永生化的角质形成细胞Hacat细胞的实验中,牛奶外泌体对角质形成细胞的紧密连接功能产生了积极的影响,这一发现为皮肤屏障的保护和修复提供了新的视角。
牛奶外泌体(mEVs)表现出极低的细胞毒性水平,证明了即使在较高浓度下,它们对人体细胞也具有极高的安全性,无有可发现的任何有害影响。共聚焦激光扫描显微镜(CLSM)的图像表明牛奶外泌体被人永生化角质细胞(Hacat)成功摄取,证实了它们在细胞间传递物质的能力。牛奶外泌体对Claudin-1和Claudin-6两种紧密连接蛋白的表达水平具有显著的上调作用。这些蛋白是构成皮肤屏障的关键因素。实验数据显示,经牛奶外泌体处理后,Claudin-1的含量比对照组增加了2.3倍,而Claudin-6的表达也随着外泌体浓度的增加而上调,这表明牛奶外泌体能够通过调节这些蛋白来增强皮肤的屏障功能。通过定量聚合酶链反应(qPCR)技术,牛奶外泌体对Hacat细胞中紧密连接蛋白mRNA表达的影响得到了量化。此外,PPP2R2A的显著下调进一步证实了牛奶外泌体在增强皮肤屏障功能方面的潜力。牛奶外泌体为皮肤屏障的保护和修复开辟了新的途径。
牛奶外泌体的美白功效
黑色素,作为皮肤中的主要色素,扮演着保护肌肤免受紫外线侵害的角色。然而,黑色素生成的异常可能导致色素沉着,影响肌肤的外观和健康。因此,控制黑色素生成的抑制剂在美容和医疗领域显得尤为重要。酪氨酸酶,这一在黑色素合成中发挥关键作用的酶已被广泛研究。它存在于多种生物体中,负责催化酪氨酸羟化和L-多巴的合成,进而形成黑色素。作为黑色素产生的主要调节器,酪氨酸酶成为了美白干预的理想靶点。
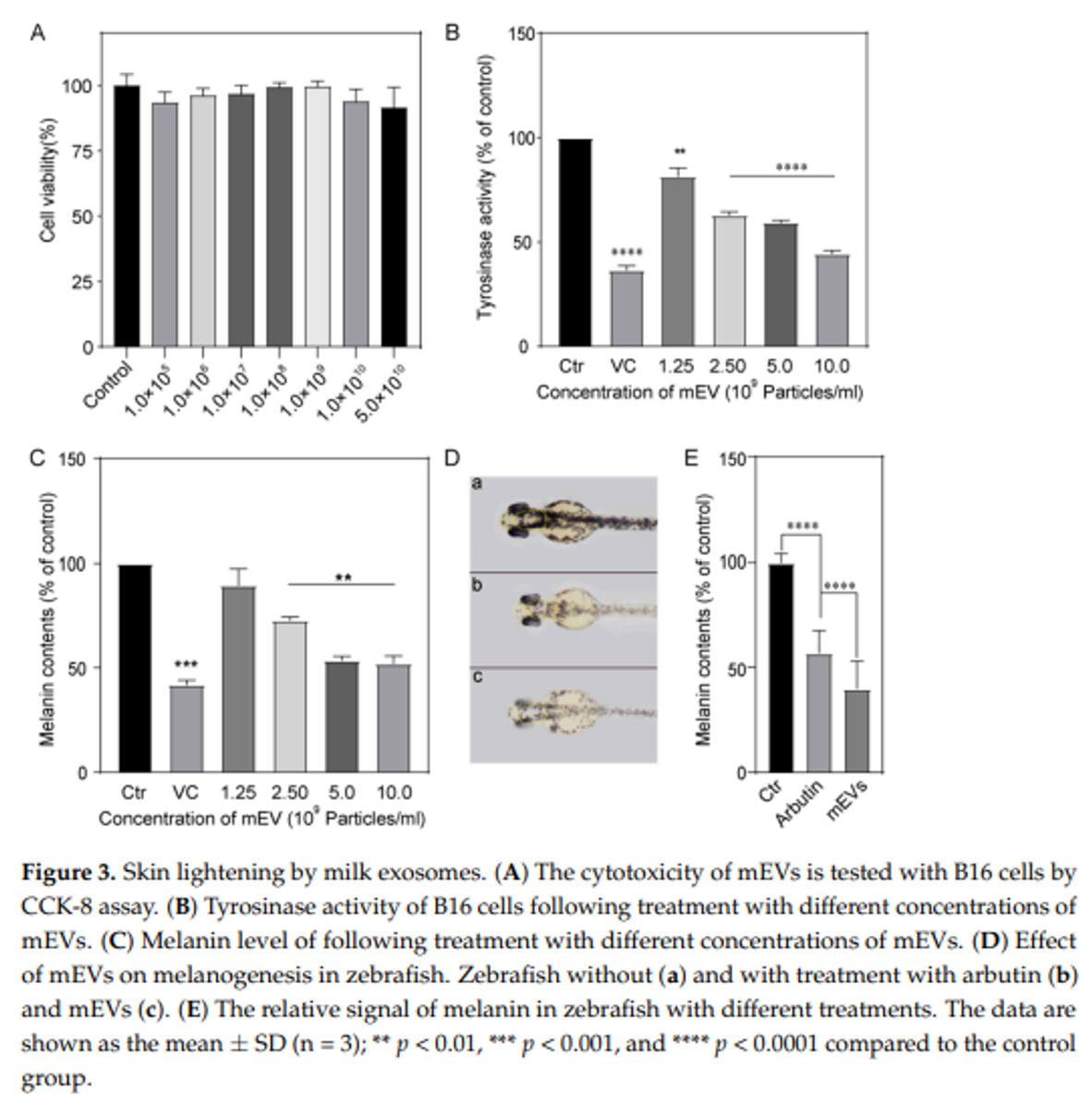
牛奶外泌体,这些来自牛奶的天然纳米粒子展现出了作为酪氨酸酶抑制剂的潜力。它们在小鼠皮肤黑色素瘤B16F10细胞系中的应用,为研究黑色素生成提供了一个强有力的模型。
牛奶外泌体处理能够以剂量依赖性的方式降低黑色素水平,且在浓度超过5.0×109颗粒/mL时效果达到平稳。此外,在对牛奶外泌体的最大耐受浓度进行评估后,使用斑马鱼胚胎进一步验证了其对黑色素含量的影响。结果显示,牛奶外泌体组的黑色素水平比对照组降低了39.9%,证实了其在治疗色素沉着障碍方面的潜在应用。如图3B所示,随着牛奶外泌体浓度的增加,酪氨酸酶活性显著降低,这进一步证实了牛奶外泌体在美白领域的应用潜力。
牛奶外泌体的抗衰老功效
随着岁月的流逝,皮肤不可避免地面临老化的挑战。氧化应激和炎症作为皮肤老化的主要内在原因,它们会对蛋白质、脂质和DNA造成损伤。活性氧(ROS)作为生物体中的主要自由基,一旦过量产生,便成为皮肤老化的催化剂。
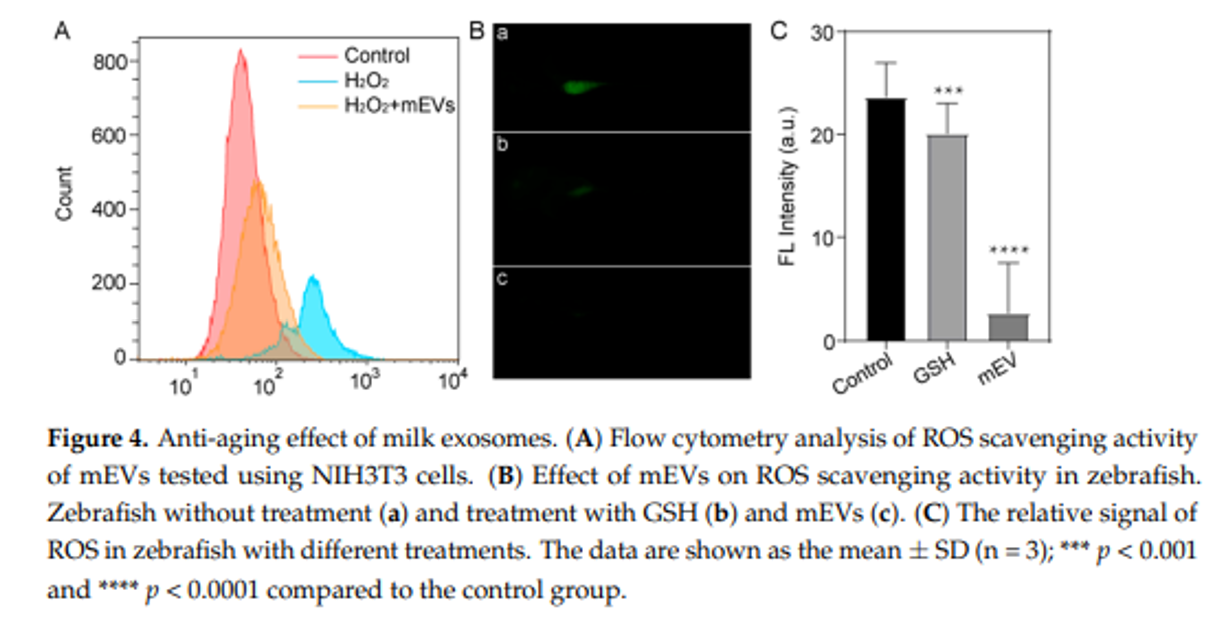
通过在小鼠胚胎成纤维细胞NIH3T3细胞中测定经H2O2预处理后的ROS含量,牛奶外泌体的抗氧化能力得到了科学的验证。实验中,NIH3T3细胞在接受了牛奶外泌体的预处理后,可以抑制H2O2刺激引起的细胞活力下降。这一发现证实了牛奶外泌体在抑制H2O2诱导的细胞毒性方面的强大潜力。通过测定CellROX的荧光强度,牛奶外泌体的ROS清除活性得到了直观的展示。在牛奶外泌体的作用下,NIH3T3细胞的荧光强度显著降低,这一现象在斑马鱼实验中也得到了验证。在斑马鱼实验中,牛奶外泌体的ROS清除活性得到了进一步的证实。与未经处理的斑马鱼相比,经过牛奶外泌体预处理的斑马鱼,其DCF荧光强度显著降低,这表明牛奶外泌体能够有效减轻氧化应激。牛奶外泌体的抗氧化效果不仅在细胞层面得到了证实,更在动物模型中展现出了其保护作用。这些结果揭示了牛奶外泌体在抗衰老领域的应用潜力,为开发新型护肤产品提供了科学依据。
牛奶外泌体在细胞中的舒缓功效
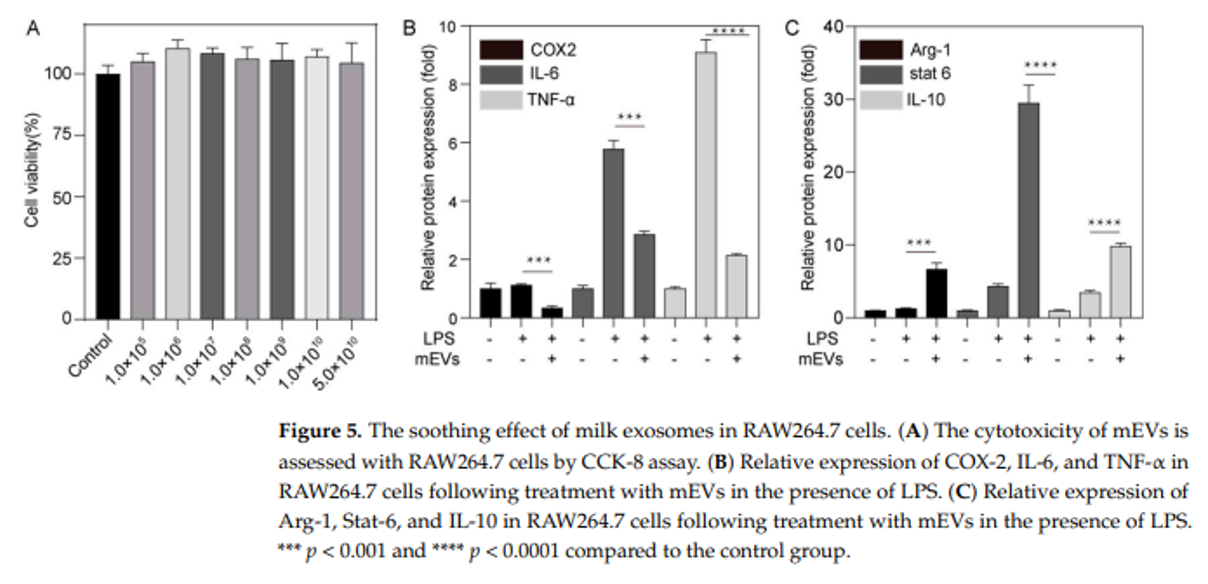
在肌肤的微观世界中,炎症因子如COX-2、IL-6和TNF-α常常威胁着皮肤的健康。它们在炎性刺激因子,如LPS(脂多糖)的刺激下可能导致肌肤出现红肿、刺激等炎症反应。牛奶外泌体(mEVs)以其出色的生物相容性和抗炎特性,展现出在细胞炎症调节的潜力。通过CCK-8评估法,发现mEVs处理小鼠单核巨噬细胞RAW 264.7没有引起细胞活力的明显改变,说明牛奶外泌体对。实验数据显示,LPS刺激显著增加了RAW 264.7细胞中炎症因子的表达。然而,在mEVs的作用下,这些炎症因子的产生被显著抑制,其中COX-2、IL-6和TNF-α的抑制率分别达到了69.9%、50.6%和76.5%。mEVs不仅减少了促炎细胞因子的分泌,还提升了抗炎因子如Arg-1、Stat-6和IL-10的表达水平。这种双向调节作用,进一步证实了mEVs在缓解细胞炎症反应中的卓越能力。牛奶外泌体这一功效的发现,为护肤产品中的舒缓成分提供了新的选择。它们通过降低促炎因子水平并增强抗炎因子含量,为肌肤提供了一种温和而有效的抗炎保护。
动物模型中的外泌体透皮功效
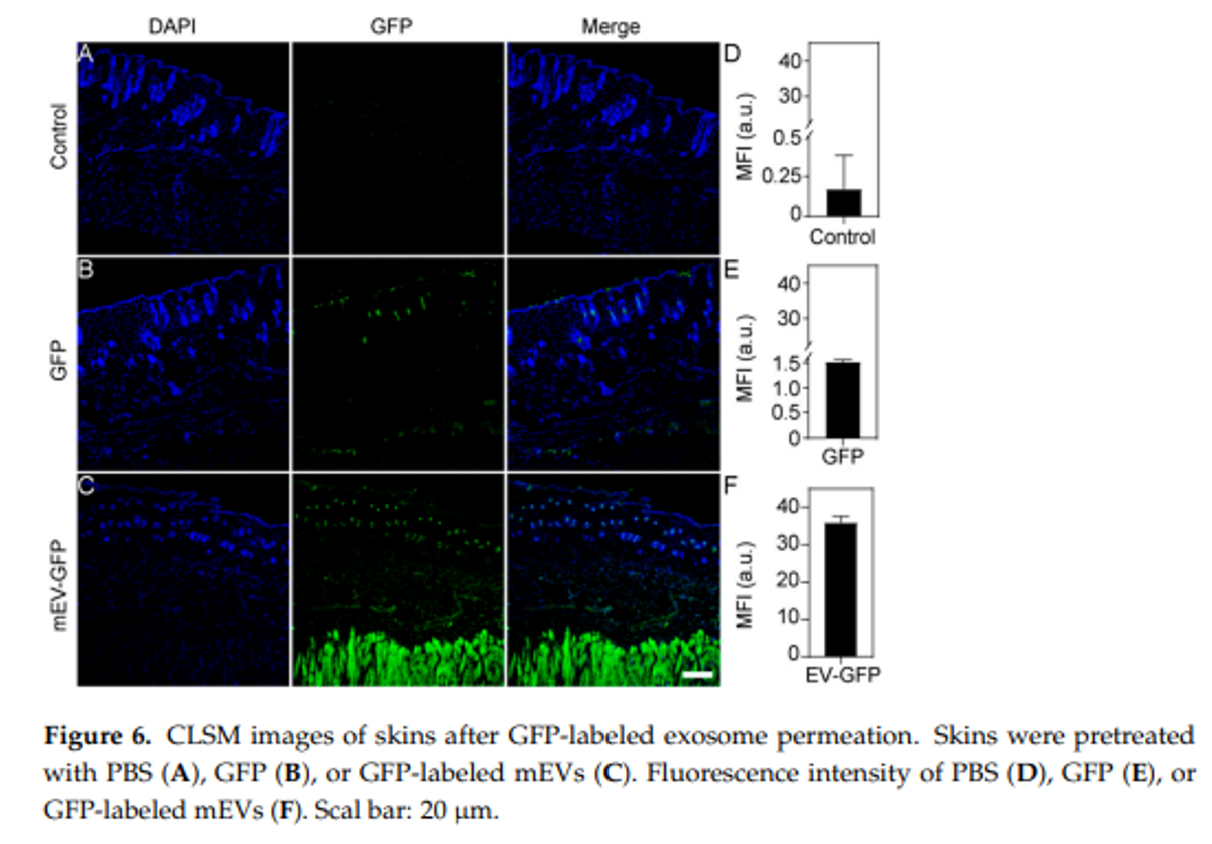
牛奶外泌体(mEVs)以其在调节皮肤功能方面的显著效果,展现出在化妆品应用中的巨大潜力。在实际应用之前,对其皮肤渗透性的研究和mEVs的安全性评估是不可或缺。通过急性经皮毒性测试发现,无论是雄性还是雌性大鼠,它们在实验期间体重逐渐增加,显示出良好的生长趋势。该研究选用了SPF级别的C57小鼠作为实验模型。在去除小鼠皮肤表面的毛发后,分别将将牛奶外泌体(对照组)、GFP蛋白(GFP组)和负载有GFP的牛奶外泌体(mEV-GFP组)涂抹于暴露的皮肤表面,进行了细致地观察和分析。通过共聚焦荧光显微镜成像,我们观察小鼠皮肤全层中绿色荧光蛋白分布,来获得牛奶外泌体携带大分子蛋白穿透皮肤屏障的直观证据。与仅接受绿色荧光蛋白(GFP组)涂抹处理的小鼠皮肤相比,经过负载有GFP的mEVs处理的小鼠皮肤在1小时后,其真皮层中出现了明显的绿色荧光。实验结果表明,牛奶外泌体不仅能够穿透皮肤的表皮层,还能在短短1小时内进入真皮层。这一发现为牛奶外泌体在经皮药物递送系统中的应用提供了有力的科学依据。
牛奶外泌体调控皮肤功能的机制
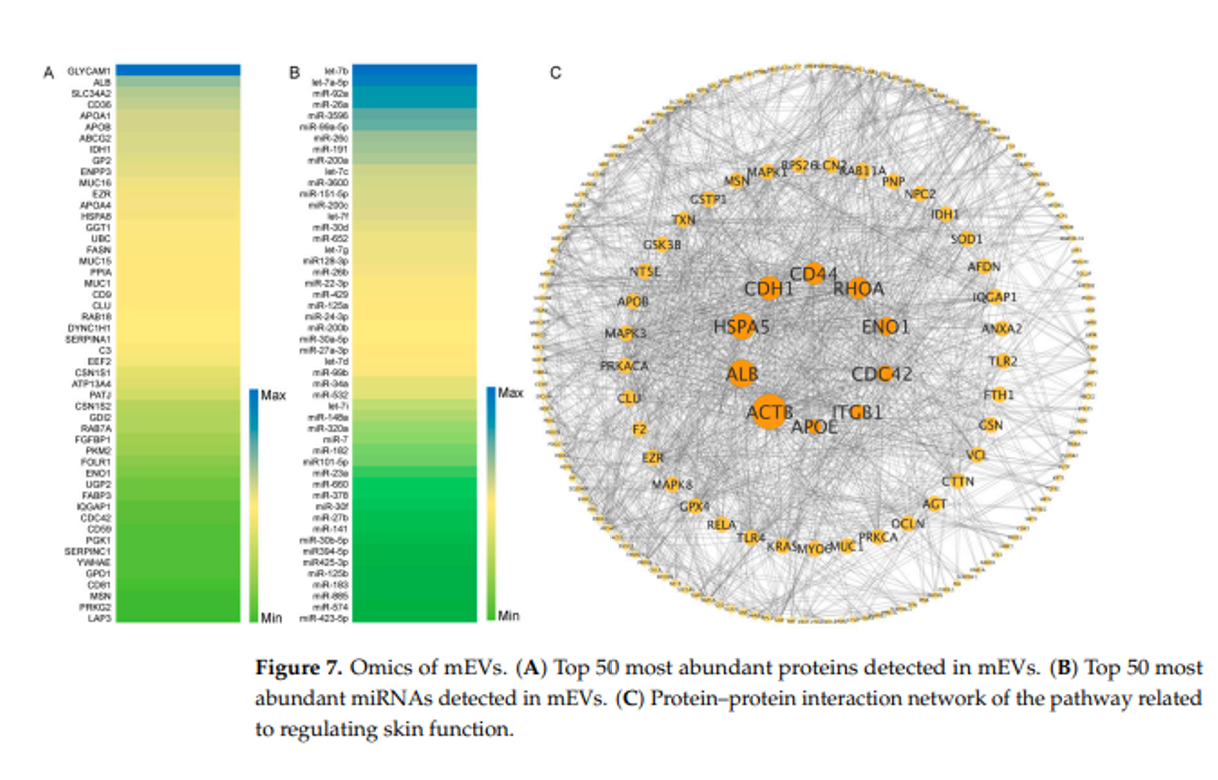
研究者对牛奶外泌体(mEVs)在调节皮肤功能方面的潜力得到了进一步探索。通过蛋白质组学和转录组学的综合分析,研究揭示了其潜在的分子机制和可能的关键活性成分,为进一步开发和应用提供了科学依据。利用液相色谱-串联质谱(LC-MS/MS)技术,在牛奶外泌体中鉴定出1899种蛋白质,其中前50种最丰富的蛋白质如图7所示。这些蛋白质及其相互作用网络的分析揭示了九种关键蛋白质,它们在皮肤功能调控中可能扮演着重要角色。其中,ACTB、RHOA和CDC42等蛋白质被发现聚集在紧密连接和途径中,它们不仅参与了皮肤屏障的维护,还对黑色素生成的调控起到了关键作用。此外,CDH1、ENO1和APOE等蛋白质对活性氧(ROS)的生成具有负向调控作用,而APOE、ALB和CD44等蛋白质通过抗炎作用发挥舒缓效果。除了蛋白质,mEVs中的miRNA也被发现参与了皮肤状况的调控。通过LC-MS/MS鉴定的442miRNA中,牛奶外泌体中的特定miRNA,如miR-130a、miR-125b-5p、miR-133b、miR-144、miR-27b和miR-23b,能够抑制黑色素生成和酪氨酸酶活性,为皮肤美白提供了新的策略。同时,miR-141和miR-181a/b/c能够改变ROS信号通路,降低ROS水平,对抗皮肤老化。 mEVs通过其内在的miRNA,如miR-155、miR-let-7、miR-124a、miR-21、miR-146a和miR-150,展现了减少细胞炎症的能力。这些发现不仅证明了mEVs能够显著改善皮肤状态,还揭示了它们通过直接向皮肤细胞传递miRNAs来发挥生物学功能的能力。牛奶外泌体的这一机制为开发新的皮肤治疗和护理产品提供了广阔的前景。
总结
总之,该研究团队建立了大规模分离制备牛奶外泌体的方法,且天然牛奶外泌体具有较好的生物相容性及护肤潜力。通过研究发现了牛奶外泌体安全无毒性、能够被皮肤角质细胞摄取、在动物模型中有较好的透皮效果。牛奶外泌体在皮肤屏障保护、抗炎、美白和抗氧化方面表现出显著功效,这些研究结果揭示牛奶外泌体在化妆品和皮肤护理领域具有广阔的开发前景。它们能够搭载活性成分,提供定制化护肤方案有效应对各种皮肤问题。牛奶外泌体的透皮效果和生物活性物质的运输能力,为经皮药物递送系统带来了光明。这一特性对于那些传统上皮肤渗透性差的成分尤为关键。研究还揭示了牛奶外泌体在治疗炎症性皮肤病变等方面的潜在用途,它们通过调节免疫反应和促进皮肤屏障的修复,为皮肤健康带来了新的希望。尽管牛奶外泌体在护肤领域的潜力已经显现,但对其长期效果、最佳应用浓度以及分子机制的深入研究仍有很长一段路要走。
外泌体资讯网 Pharmaceutics| 国药集团中国生物研究院 安文林实验室团队:大规模分离制备具有皮肤护理功效的牛奶外泌体





